РЕКЛАМА
Медицинская Республика
НАЙТИ НА САЙТЕ
НОВОСТЬ ДНЯ
"Максимальное снижение заболеваемости ОРИ может быть достигнуто при использовании вакцинации и средств неспецифической иммунопрофилактики”. Заплатников А.Л.
ПОПУЛЯРНЫЕ НОВОСТИ
РЕКЛАМА
Глава 5. Профилактика инфекционных заболеваний (Ющук Н.Д., Мартынов Ю.В., Сафиуллина Н.Х.)
Опубликовано : 15-05-2014, 16:03 | Опубликовал: Nalk | Категория: Здоровый образ жизни и профилактика заболеваний
Теория Луи Пастера о микро-
бах – это лишь смешная фантазия.
Пьер Паше, профессор Универси-
тета Тулузы, 1872
бах – это лишь смешная фантазия.
Пьер Паше, профессор Универси-
тета Тулузы, 1872
5.1. Международные медико-санитарные правила
Международные медико-санитарные правила (ММСП) – документ, выработанный 194 государствами-членами ВОЗ, по усилению безопасности в области общественного здравоохранения на национальном, региональном и глобальном уровне. Целью принятия новых ММСП в 2007г. явилось содействие международному сообществу в предотвращении и принятии ответных мер на критические опасности для здоровья людей, которые потенциально могут пересекать государственные границы.
ММСП, прежде всего, разработаны для профилактики распространения инфекционных заболеваний (табл. 5.1). Однако они применимы и для других чрезвычайных ситуаций, таких как разливы и утечки химических веществ или расплавление активной зоны ядерного реактора.
Таблица 5.1. Инфекционные заболевания, имеющие серьезный риск для общественного здравоохранения
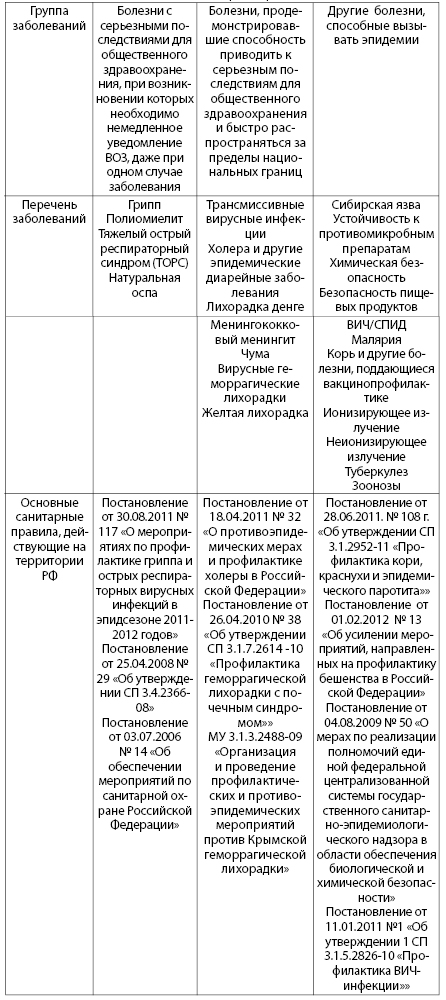
В соответствии с ММСП, страны должны информировать ВОЗ об определенных вспышках болезней. Для осуществления требований ММСП приоритетными являются три задачи:
1. Выделение учреждения-национального координатора по ММСП. В Россию такую роль выполняет Федеральная служба по надзору в сфере прав потребителей и защиты человека (http://rospotrebnadzor.ru). Данная служба самостоятельно или через свои региональные отделения выполняет все функции санитарно-эпидемиологического надзора, т.е. надзор за соблюдением работодателями санитарно-гигиенических и санитарно-противоэпидемиологических норм и правил (см. также главу 1). Новые санитарные правила на территории нашей страны введены Постановлением Главного санитарного врача РФ от 05.03.2008 № 16 «Об утверждении санитарно-эпидемиологических правил СП 3.1.1.2343-08». Данные санитарные правила базируются на Федеральном законе от 30.03.99 № 52-ФЗ (ред. от 18.07.2011) «О санитарно-эпидемиологическом благополучии населения».
На мировом уровне координатором по ММСП является специальное бюро ВОЗ в Лионе (Франция) (http://who.int/ihr/lyon/ru/index.html).
2. Обеспечение предоставления отчетности обо всех событиях в области общественного здравоохранения. ММСП устанавливают универсальные формы и сроки отчетности, что позволяет унифицировать информацию, поступающую из различных источников.
3. Оценка и усиление национальных возможностей по контролю за инфекционными заболеваниями. На территории РФ Постановлениями Главного государственного санитарного врача Российской Федерации вводятся санитарные правила (СП) по контролю за актуальными в настоящий момент времени инфекционными заболеваниями. Как правило, санитарные правила содержат следующую информацию:
• область применения;
• описание особенностей тех заболеваний (включая основные клинические проявления и пути передачи), в отношении которых действуют санитарные правила;
• порядок выявления, учета и регистрация больных;
• особенности лабораторной диагностики заболеваний;
• мероприятия в очагах распространения заболеваний;
• меры по специфической и неспецифической профилактике заболеваний;
• меры по эпидемиологическому надзору;
• при возможности - мероприятия по ликвидации инфекции.
Кроме того, вводятся методические указания (МУ) по контролю за инфекционными заболеваниями. Структура методических указаний, как правило, не отличается от санитарных правил. Но санитарные правила носят регламентирующий характер, а методические указания – рекомендательный. В качестве основного документа в этой сфере укажем МУ 3.4.2552-09 «Организация и проведение первичных противоэпидемических мероприятий в случаях выявления больного, подозрительного на заболевания инфекционными болезнями, вызывающими ЧС в области санэпидблагополучия населения».
ММСП вводят новые подходы к профилактике распространения инфекционных заболеваний, включая следующие:
• особые процедуры для уведомления, консультирования и отчетности в отношении событий в области общественного здравоохранения;
• установление постоянных каналов связи между странами и ВОЗ, функционирующих круглосуточно семь дней в неделю;
• возможность учитывать сообщения из других источников, помимо уведомлений и консультаций;
• запросы ВОЗ о проверке национальными органами здравоохранения сообщений о событиях в области общественного здравоохранения, происходящих на территории стран.
ММСП вводят ряд ограничений на международные перевозки и торговлю для обеспечения здоровья населения за счет предотвращения распространения болезней. Прежде всего, осуществляется контроль людей, багажа, грузов, контейнеров, товаров, почтовых посылок и т.д. в аэропортах, портах и наземных транспортных узлах. В связи с организацией таможенного союза России, Белоруси и Казахстана, Решением Комиссии Таможенного союза от 28 мая 2010 г. № 299 было утверждено Положение «о порядке осуществления государственного санитарно-эпидемиологического надзора (контроля) за лицами и транспортными средствами, пересекающими таможенную границу Таможенного союза, подконтрольными товарами, перемещаемыми через таможенную границу Таможенного союза и на таможенной территории Таможенного союза».
Для пассажиров вводится «Международное свидетельство о вакцинации или профилактике», вид которого устанавливается ММСП. Ответственность за соблюдение установленного графика вакцинаций ложится на человека, выезжающего из/в эндемичной территории, а также на организатора поездки. При отсутствии надлежащих прививок или оформленного свидетельства о вакцинации, у местных властей есть право не пустить пассажира.
Рекомендации по вакцинации приведены в приложениях 18 и 19. Следует обратить внимание на то, что перечень рекомендуемых вакцины может пересматриваться ежегодно с учетом эпидемиологической обстановки. Кроме того, обращаем внимание на то, что вакцинация путешествен-ника может потребоваться не только при выезде за рубеж, но и в ряд территорий РФ. Следует помнить о том, что прививку необходимо сделать заблаговременно, т.к. необходимо время между вакцинацией и началом действия вакцины. Эффективность вакцинации, сделанной непосредственно перед выездом, как правило, близка к нулю.
Также ММСП вводятся специальные судовые санитарные свидетельства. Также в случае подозрения о том, что у пассажира имеется инфекционное заболевание или же пассажир следует из эндемичного района, введена «Карта с контактной информацией о пассажире для органов здравоохранения».
Контрольные вопросы
1. Для чего нужны международные медико-санитарные правила?
2. Каковы особенности реализации международных медико-санитарных правил на территории РФ?
3. Для чего нужна вакцинация путешественников? Как она проводится?
Программы иммунизации в мире
Успешная реализация программы ВОЗ по ликвидации оспы в мире резко повысила престиж программ вакцинации. Еще в ходе завершения этой программы в 1974 году был принят документ, направленный на борьбу с ведущими инфекционными болезнями - «Расширенную программу иммунизации» (РПИ), в ходе выполнения которой все страны мира добились больших успехов в снижении заболеваемости шести инфекционных болезней: дифтерии, столбняка, туберкулеза, полиомиелита коклюша и кори. В ряде стран в течение многих лет отсутствуют случаи заболевания дифтерией; страны Западной Европы и Россия получили Сертификат, подтверждающий, что эти территории свободны от полиомиелита. В рамках РПИ на очереди ликвидация кори и краснухи. В перспективе ВОЗ рассматривает стратегию ликвидацию в Европейском регионе эпидемического паротита, краснухи, ветряной оспы. И эта задача достижима с помощью вакцинации.
Число заболеваний, в борьбе с которыми используются вакцины, сейчас более 20, и это не предел. В последние годы в России появился опыт иммунизации населения против гемофильной инфекции типа В, пневмококковой инфекции, инфекции, вызванной вирусом папилломы человека, вирусного гепатита А, дизентерии Зонне и других инфекций. Интенсивно ведутся исследования по разработке комбинированных препаратов, позволяющих за одну инъекцию вводить 5-6 и более вакцин; по повышению иммуногенности вакцин, в частности по уменьшению числа необходимых для вакцинации доз. Другое направление в вакцинологии – разработкавакцин, введение которых имитировало бы естественный путь проникновения возбудителя в организм человека (вакцины на основе трансгенных растений, липосомальные вакцины, синтетические пептидные вакцины). Современные вакцины характеризуются низкой реактогенностью и повышенной термостабильностью. Всемирная Вакцинная Инициатива поставила своей целью создание «идеальной комбинированной вакцины от 25-30 инфекций», вводимой однократно в самом раннем возрасте и без негативных последствий.
Использование уже применяемых в мире вакцин, а также внедрение новых препаратов, позволило бы спасти ежегодно 350 000 жизней от коклюша; 1,1 млн - от кори; 800 000 - от гепатита; 300 000 - от столбняка; 300 000 - от менингита; 500 000 - от уродств, связанных с врожденной краснухой.
В ближайшие годы будут введены новые вакцины для специфической профилактики ротавирусной инфекции, диарейных болезней, РС-вирусной и пневмококковой инфекции и др.
Правовые аспекты вакцинопрофилактики
Каждый гражданин РФ, в соответствии Конституцией (основным законом) РФ, ст. 55, имеет право на бесплатную медицинскую помощь в государственной системе здравоохранения.
Федеральный Закон «О санитарно-эпидемиологическом благополучии населения» от 12 марта 1999 г. направлен на обеспечение санитарно- эпидемиологического благополучия населения как одного из основных условий реализации конституционных прав граждан на охрану здоровья. В ст. 35 этого закона сказано: «Профилактические прививки проводятся гражданам в соответствии с законодательством РФ для предупреждения возникновения и распространения инфекционных заболеваний».
В 1998 г. принят Федеральный Закон «Об иммунопрофилактике инфекционных болезней», основными положениями которого являются:
1. Гарантия государства в доступности для граждан профилактических прививок.
2. Бесплатное проведение профилактических прививок, включенных в национальный календарь и по эпидемическим показаниям.
3. Социальная защита граждан при возникновении поствакцинальных осложнений.
4. Государственный контроль качества, эффективности и безопасности медицинских иммунобиологических препаратов.
5. Обеспечение современного уровня производства медицинских иммунобиологических препаратов.
Национальный календарь профилактических прививок
Национальный календарь профилактических – нормативно-правовой акт, устанавливающий сроки и порядок проведения гражданам РФ профилактических прививок (приложение 20). Ныне действующий Национальный календарь профилактических прививок включает прививки против 11 инфекционных болезней (вирусного гепатита В, туберкулеза, полиомиелита, дифтерии, коклюша, столбняка, гриппа, гемофильной инфекции, кори, краснухи, эпидемического паротита).
Прививки проводятся с согласия граждан, родителей или других законных представителей несовершеннолетних детей или недееспособных лиц. Граждане имеют право на отказ от профилактических прививок, но обязаны подтвердить его в письменной форме, также как и согласие на прививку (приказ Минздравсоцразвития от 26 января 2009 г. N19н).
В Законе РФ предусматриваются определенные последствия для гражданина, в случае отказа от вакцинации:
• запрет на выезд в страны, пребывание в которых требует конкретных профилактических прививок;
• временный отказ в приеме в образовательные и оздоровительные учреждения в случае возникновения массовых инфекционных заболеваний или угрозы возникновения эпидемий;
• отказ в приеме граждан на работу или отстранение от работ, выполнение которых связано с высоким риском заболевания инфекционными болезнями.
Перечень работ, выполнение которых связано с высоким риском заболевания инфекционными болезнями и требует обязательного про-ведения профилактических прививок, утвержден Постановлением Пра-вительства Российской Федерации от 15 июля 1999 г. № 825.
Специальная глава Закона РФ посвящена социальной защите граждан при возникновении поствакцинальных осложнений - тяжелых или стойких нарушений состояния здоровья вследствие иммунизации. В этих случаях выплачивается государственное единовременное пособие в размере 10 000 рублей, а в случае смерти - 30 000 рублей (в ред. ФЗ от 07.08.2000; от 22.08.2004 №122-ФЗ). Перечень осложнений, дающих право на государственное единовременное пособие утвержден Постановлением Правительства РФ от 2 августа 1999 г. № 885.
Гражданин, признанный инвалидом вследствие поствакцинального осложнения, имеет право на ежемесячную компенсацию в размере 1000 рублей (в ред. ФЗ от 7 августа 2000 г. №122-ФЗ). Гражданин (или один из родителей ребенка), у которого временная нетрудоспособность связана с поствакцинальным осложнением, имеет право на пособие в размере 100% среднего заработка независимо от стажа работы за все время болезни или ухода за ребенком.
1. Выделение учреждения-национального координатора по ММСП. В Россию такую роль выполняет Федеральная служба по надзору в сфере прав потребителей и защиты человека (http://rospotrebnadzor.ru). Данная служба самостоятельно или через свои региональные отделения выполняет все функции санитарно-эпидемиологического надзора, т.е. надзор за соблюдением работодателями санитарно-гигиенических и санитарно-противоэпидемиологических норм и правил (см. также главу 1). Новые санитарные правила на территории нашей страны введены Постановлением Главного санитарного врача РФ от 05.03.2008 № 16 «Об утверждении санитарно-эпидемиологических правил СП 3.1.1.2343-08». Данные санитарные правила базируются на Федеральном законе от 30.03.99 № 52-ФЗ (ред. от 18.07.2011) «О санитарно-эпидемиологическом благополучии населения».
На мировом уровне координатором по ММСП является специальное бюро ВОЗ в Лионе (Франция) (http://who.int/ihr/lyon/ru/index.html).
2. Обеспечение предоставления отчетности обо всех событиях в области общественного здравоохранения. ММСП устанавливают универсальные формы и сроки отчетности, что позволяет унифицировать информацию, поступающую из различных источников.
3. Оценка и усиление национальных возможностей по контролю за инфекционными заболеваниями. На территории РФ Постановлениями Главного государственного санитарного врача Российской Федерации вводятся санитарные правила (СП) по контролю за актуальными в настоящий момент времени инфекционными заболеваниями. Как правило, санитарные правила содержат следующую информацию:
• область применения;
• описание особенностей тех заболеваний (включая основные клинические проявления и пути передачи), в отношении которых действуют санитарные правила;
• порядок выявления, учета и регистрация больных;
• особенности лабораторной диагностики заболеваний;
• мероприятия в очагах распространения заболеваний;
• меры по специфической и неспецифической профилактике заболеваний;
• меры по эпидемиологическому надзору;
• при возможности - мероприятия по ликвидации инфекции.
Кроме того, вводятся методические указания (МУ) по контролю за инфекционными заболеваниями. Структура методических указаний, как правило, не отличается от санитарных правил. Но санитарные правила носят регламентирующий характер, а методические указания – рекомендательный. В качестве основного документа в этой сфере укажем МУ 3.4.2552-09 «Организация и проведение первичных противоэпидемических мероприятий в случаях выявления больного, подозрительного на заболевания инфекционными болезнями, вызывающими ЧС в области санэпидблагополучия населения».
ММСП вводят новые подходы к профилактике распространения инфекционных заболеваний, включая следующие:
• особые процедуры для уведомления, консультирования и отчетности в отношении событий в области общественного здравоохранения;
• установление постоянных каналов связи между странами и ВОЗ, функционирующих круглосуточно семь дней в неделю;
• возможность учитывать сообщения из других источников, помимо уведомлений и консультаций;
• запросы ВОЗ о проверке национальными органами здравоохранения сообщений о событиях в области общественного здравоохранения, происходящих на территории стран.
ММСП вводят ряд ограничений на международные перевозки и торговлю для обеспечения здоровья населения за счет предотвращения распространения болезней. Прежде всего, осуществляется контроль людей, багажа, грузов, контейнеров, товаров, почтовых посылок и т.д. в аэропортах, портах и наземных транспортных узлах. В связи с организацией таможенного союза России, Белоруси и Казахстана, Решением Комиссии Таможенного союза от 28 мая 2010 г. № 299 было утверждено Положение «о порядке осуществления государственного санитарно-эпидемиологического надзора (контроля) за лицами и транспортными средствами, пересекающими таможенную границу Таможенного союза, подконтрольными товарами, перемещаемыми через таможенную границу Таможенного союза и на таможенной территории Таможенного союза».
Для пассажиров вводится «Международное свидетельство о вакцинации или профилактике», вид которого устанавливается ММСП. Ответственность за соблюдение установленного графика вакцинаций ложится на человека, выезжающего из/в эндемичной территории, а также на организатора поездки. При отсутствии надлежащих прививок или оформленного свидетельства о вакцинации, у местных властей есть право не пустить пассажира.
Рекомендации по вакцинации приведены в приложениях 18 и 19. Следует обратить внимание на то, что перечень рекомендуемых вакцины может пересматриваться ежегодно с учетом эпидемиологической обстановки. Кроме того, обращаем внимание на то, что вакцинация путешествен-ника может потребоваться не только при выезде за рубеж, но и в ряд территорий РФ. Следует помнить о том, что прививку необходимо сделать заблаговременно, т.к. необходимо время между вакцинацией и началом действия вакцины. Эффективность вакцинации, сделанной непосредственно перед выездом, как правило, близка к нулю.
Также ММСП вводятся специальные судовые санитарные свидетельства. Также в случае подозрения о том, что у пассажира имеется инфекционное заболевание или же пассажир следует из эндемичного района, введена «Карта с контактной информацией о пассажире для органов здравоохранения».
Контрольные вопросы
1. Для чего нужны международные медико-санитарные правила?
2. Каковы особенности реализации международных медико-санитарных правил на территории РФ?
3. Для чего нужна вакцинация путешественников? Как она проводится?
5.2. Основы иммунопрофилактики
Программы иммунизации в мире
Успешная реализация программы ВОЗ по ликвидации оспы в мире резко повысила престиж программ вакцинации. Еще в ходе завершения этой программы в 1974 году был принят документ, направленный на борьбу с ведущими инфекционными болезнями - «Расширенную программу иммунизации» (РПИ), в ходе выполнения которой все страны мира добились больших успехов в снижении заболеваемости шести инфекционных болезней: дифтерии, столбняка, туберкулеза, полиомиелита коклюша и кори. В ряде стран в течение многих лет отсутствуют случаи заболевания дифтерией; страны Западной Европы и Россия получили Сертификат, подтверждающий, что эти территории свободны от полиомиелита. В рамках РПИ на очереди ликвидация кори и краснухи. В перспективе ВОЗ рассматривает стратегию ликвидацию в Европейском регионе эпидемического паротита, краснухи, ветряной оспы. И эта задача достижима с помощью вакцинации.
Число заболеваний, в борьбе с которыми используются вакцины, сейчас более 20, и это не предел. В последние годы в России появился опыт иммунизации населения против гемофильной инфекции типа В, пневмококковой инфекции, инфекции, вызванной вирусом папилломы человека, вирусного гепатита А, дизентерии Зонне и других инфекций. Интенсивно ведутся исследования по разработке комбинированных препаратов, позволяющих за одну инъекцию вводить 5-6 и более вакцин; по повышению иммуногенности вакцин, в частности по уменьшению числа необходимых для вакцинации доз. Другое направление в вакцинологии – разработкавакцин, введение которых имитировало бы естественный путь проникновения возбудителя в организм человека (вакцины на основе трансгенных растений, липосомальные вакцины, синтетические пептидные вакцины). Современные вакцины характеризуются низкой реактогенностью и повышенной термостабильностью. Всемирная Вакцинная Инициатива поставила своей целью создание «идеальной комбинированной вакцины от 25-30 инфекций», вводимой однократно в самом раннем возрасте и без негативных последствий.
Использование уже применяемых в мире вакцин, а также внедрение новых препаратов, позволило бы спасти ежегодно 350 000 жизней от коклюша; 1,1 млн - от кори; 800 000 - от гепатита; 300 000 - от столбняка; 300 000 - от менингита; 500 000 - от уродств, связанных с врожденной краснухой.
В ближайшие годы будут введены новые вакцины для специфической профилактики ротавирусной инфекции, диарейных болезней, РС-вирусной и пневмококковой инфекции и др.
Правовые аспекты вакцинопрофилактики
Каждый гражданин РФ, в соответствии Конституцией (основным законом) РФ, ст. 55, имеет право на бесплатную медицинскую помощь в государственной системе здравоохранения.
Федеральный Закон «О санитарно-эпидемиологическом благополучии населения» от 12 марта 1999 г. направлен на обеспечение санитарно- эпидемиологического благополучия населения как одного из основных условий реализации конституционных прав граждан на охрану здоровья. В ст. 35 этого закона сказано: «Профилактические прививки проводятся гражданам в соответствии с законодательством РФ для предупреждения возникновения и распространения инфекционных заболеваний».
В 1998 г. принят Федеральный Закон «Об иммунопрофилактике инфекционных болезней», основными положениями которого являются:
1. Гарантия государства в доступности для граждан профилактических прививок.
2. Бесплатное проведение профилактических прививок, включенных в национальный календарь и по эпидемическим показаниям.
3. Социальная защита граждан при возникновении поствакцинальных осложнений.
4. Государственный контроль качества, эффективности и безопасности медицинских иммунобиологических препаратов.
5. Обеспечение современного уровня производства медицинских иммунобиологических препаратов.
Национальный календарь профилактических прививок
Национальный календарь профилактических – нормативно-правовой акт, устанавливающий сроки и порядок проведения гражданам РФ профилактических прививок (приложение 20). Ныне действующий Национальный календарь профилактических прививок включает прививки против 11 инфекционных болезней (вирусного гепатита В, туберкулеза, полиомиелита, дифтерии, коклюша, столбняка, гриппа, гемофильной инфекции, кори, краснухи, эпидемического паротита).
Прививки проводятся с согласия граждан, родителей или других законных представителей несовершеннолетних детей или недееспособных лиц. Граждане имеют право на отказ от профилактических прививок, но обязаны подтвердить его в письменной форме, также как и согласие на прививку (приказ Минздравсоцразвития от 26 января 2009 г. N19н).
В Законе РФ предусматриваются определенные последствия для гражданина, в случае отказа от вакцинации:
• запрет на выезд в страны, пребывание в которых требует конкретных профилактических прививок;
• временный отказ в приеме в образовательные и оздоровительные учреждения в случае возникновения массовых инфекционных заболеваний или угрозы возникновения эпидемий;
• отказ в приеме граждан на работу или отстранение от работ, выполнение которых связано с высоким риском заболевания инфекционными болезнями.
Перечень работ, выполнение которых связано с высоким риском заболевания инфекционными болезнями и требует обязательного про-ведения профилактических прививок, утвержден Постановлением Пра-вительства Российской Федерации от 15 июля 1999 г. № 825.
Специальная глава Закона РФ посвящена социальной защите граждан при возникновении поствакцинальных осложнений - тяжелых или стойких нарушений состояния здоровья вследствие иммунизации. В этих случаях выплачивается государственное единовременное пособие в размере 10 000 рублей, а в случае смерти - 30 000 рублей (в ред. ФЗ от 07.08.2000; от 22.08.2004 №122-ФЗ). Перечень осложнений, дающих право на государственное единовременное пособие утвержден Постановлением Правительства РФ от 2 августа 1999 г. № 885.
Гражданин, признанный инвалидом вследствие поствакцинального осложнения, имеет право на ежемесячную компенсацию в размере 1000 рублей (в ред. ФЗ от 7 августа 2000 г. №122-ФЗ). Гражданин (или один из родителей ребенка), у которого временная нетрудоспособность связана с поствакцинальным осложнением, имеет право на пособие в размере 100% среднего заработка независимо от стажа работы за все время болезни или ухода за ребенком.
Постановлением Правительства РФ от 27 декабря 2000 г. № 1013 определен порядок выплаты государственных единовременных пособий и ежеме-сячных компенсаций гражданам при возникновении поствакцинальных осложнений. Выплаты осуществляются органами социальной защиты населения субъектов РФ за счет средств Федерального бюджета. Учет поствакцинальных осложнений поручено обеспечить Министерству здравоохранения и социального развития РФ.
Права граждан, как потребителей медицинских услуг, защищает также Закон РФ «О защите прав потребителей» от 07 февраля 1992 г. (ст. 4, 5, 6, 7, 8, 10, 11, 12, 13, 16). В этих статьях закреплена ответственность за предоставляемые услуги, их качество, ненадлежащую информацию, причиненный ущерб, в том числе здоровью. Потребитель же имеет права на безопасность предоставляемых услуг, полную информацию о предоставляемых услугах, возмещение ущерба, льготы и судебную защиту.
Виды иммунобиологических препаратов
В практике здравоохранения для иммунопрофилактики инфекционных болезней используют следующие типы вакцин.
1. Живые вакцины – микроорганизмы с ослабленной или утраченной вирулентностью (вакцинные штаммы).
2. Инактивированны (корпускулярные) вакцины – микроорганизмы, инактивированные химическим (фенол, формалин, спирт и др.) или физическим (нагревание, ультрафиолетовое излучение) способом.
3. Химические (молекулярные) вакцины – протективные антигены микроорганизмов, выделенные с помощью физико-химических и/или иммунохимических методов.
4. Анатоксины – обезвреженные экзотоксины микроорганизмов.
5. Рекомбинантные вакцины – полученные при использовании генно-инженерной технологии.
Иммунопрофилактика коклюша, дифтерии, столбняка
Специфическая профилатика коклюша, дифтерии и столбняка про-водится АКДС-вакциной.
Отечественная коклюшно-дифтерийно-столбнячная вакцина соответствует международным требованиям. Она применяется в рамках Национального календаря профилактических прививок. АКДС-вакцина состоит из убитых коклюшных микробов и очищенных дифтерийного и столбнячного анатоксинов, адсорбированных на гидроокиси алюминия. В 1 мл препарата содержится 20 млрд коклюшных клеток, 30 единиц дифтерийного и 10 единиц столбнячного анатоксина.
Прививки АКДС начинают с 3-месячного возраста. Курс вакцинации состоит из трех прививок с интервалом 1,5 месяца. Сокращение интервалов не допускается, а при необходимости увеличивается, но по возможности прививку проводят в ближайший срок, определяемый состоянием здоровья детей. Переболевшим коклюшем детям делают прививку АДС-анатоксином. АКДС возможно совмещать с прививкой против полиомиелита и вирусного гепатита В. Последующие прививки поводят не ранее чем через 1 месяц. Ревакцинацию АКДС проводят через 12 месяцев после окончания курса вакцинации. Если вакцинация АКДС не проведена до 4-летнего возраста, то иммунизацию проводят АДС-анатоксином (от 4 до 5 лет 11 мес.) или АДС-М-анатоксином (в возрасте 6 лет и старше).
Противопоказания к введению АКДС: прогрессирующие заболевания нервной системы, афебрильные судороги в анамнезе, сильная общая реакция (температура 40оС и выше в первые двое суток) или осложнение на АКДС-вакцину.
Если ребенок привит АКДС-вакциной двукратно, курс вакцинации против дифтерии и столбняка считают законченным. Если получена одна прививка АКДС, можно продолжить курс вакцинации АДС-анатоксином через 1,5 месяца в ближайший возможный день после последней прививки и 1-ю ревакцинацию провести АДС-анатоксином через 12 месяцев после законченного вакцинального курса. Если осложнение развилось после третьей вакцинации АКДС, первую ревакцинацию проводят АДС-анатоксином через 12 месяцев. Последующие ревакцинации проводят в 7, 14 лет и каждые последующие 10 лет АДС-М-анатоксином.
Дети с противопоказаниями к применению АКДС-вакцины могут прививаться АДС-анатоксином в соответствии с инструкцией по его применению.
После перенесенных острых заболеваний прививают по выздоровлению. Хронических больных - по достижении ремиссии.
АКДС-вакцину выпускают в ампулах по 1 мл (две прививочные дозы) и хранят при температуре от +2 до +80С. Препарат, подвергшийся замораживанию, к использованию не пригоден.
Иммунопрофилактика кори
Для специфической профилактики кори используется вакцина коревая культуральная живая сухая. Прививочная доза содержит не менее 1000 ТЦД50 вируса кори и не более 20 единиц антибиотика (гентамицин).
Вакцина применяется для плановой и экстренной профилактики кори.
Плановые прививки проводят двукратно (в 12 месяцев и 6 лет) детям, не болевшим корью. Интервал между вакцинацией и ревакцинацией- не менее 6 месяцев. Иммунизации также подлежат подростки и взрослые в возрасте до 35 лет, не болевшие, не привитые и не имеющие сведений о профилактических прививках против кори; контактные лица из очагов заболевания, не болевшие, не привитые и не имеющие сведений о про-филактических прививках против кори - без ограничения возраста - иммунизация против кори.
Экстренную профилактику проводят детям с 12-месячного возраста и старше, не привитым, не болевшим корью, имевшим контакт с больным корью, не позднее чем через 72 часа после контакта. Вакцину вводят подкожно, в объеме 0,5 мл под лопатку или в область плеча. Обычно поствакцинальной реакции не бывает.
Противопоказания:
1. Тяжелые формы аллергии на аминогликозиды (гентамицин, мономицин, неомицин и др.) и перепелиные (куриные) яйца.
2. Первичный иммунодефицит, злокачественные заболевания крови и новообразования.
3. Сильная реакция (температура выше 400С, отек, гиперемия 8 см в месте инъекции) или осложнения на предыдущую дозу.
4. Беременность.
5. Анафилактическая реакция на паротитную вакцину.
ВИЧ-инфекция не является противопоказанием. При временных противопоказаниях прививают после их отмены.
Вакцинацию против кори можно проводить одновременно с другими календарными прививками. В Национальном календаре профилактических прививок предусмотрено одновременная вакцинация вакцин против кори, эпидемического паротита, краснухи.
После введения препаратов иммуноглобулина человека прививки против кори проводятся не ранее чем через 3 месяца.
Иммунопрофилактика эпидемического паротита
Национальный календарь профилактических прививок устанавливает проведение двукратной иммунизации: в возрасте 12 месяцев и 6 лет. С целью профилактики используется живая вакцина паротитная (ЖВП).
Живая паротитная вакцина готовится из аттенуированного штамма вируса паротита Л-3, выращенного на культуре клеток эмбрионов япон-ских перепелов. Выпускается в сухом виде в ампулах или флаконах. Прививочная доза содержит не менее 10 000 ТЦД50 аттенуированного вируса паротита, следы неомицина или канамицина, белок сыворотки крупного рогатого скота.
Прививки против эпидемического паротита проводят ранее не болевшим детям дважды - в 12 месяцев и 6 лет. Моновакцину вводят од-новременно с вакцинами против кори и краснухи в разные участки тела. ЖВП вводят по 0,5 мл подкожно под лопатку или в наружную область плеча.
У большинства привитых паротитной вакциной поствакцинальных реакций не наблюдается.
Противопоказания:
1. Иммунодефицитные состояния (первичные и, как следствие иммуносупрессии), лейкозы, лимфомы, другие злокачественные болезни, сопровождающиеся снижением клеточного иммунитета.
2. Тяжелые формы аллергичеких реакций на аминогликозиды и яичный белок.
3. Анафилактическая реакция на коревую вакцину.
4. Беременность (ввиду теоретического риска для плода).
Прививки проводят по окончании острого заболевания или после обострения хронического. Вакцинированных женщин следует предупредить о необходимости избегать беременности в течение трех месяцев; наступление беременности в этот период, однако, не требует ее прерывания. Кормление грудью не является противопоказанием к прививке.
Иммунопрофилактика краснухи
Иммунопрофилактика краснухи введена в Национальный календарь профилактических прививок в 1997 г. Однако, массовая вакцинация началась только с 2002-2003 гг., а заболеваемость краснухой начала снижаться с 2005 года.
Вакцинацию против краснухи проводят детям от года до 18 лет и девушкам от 18 до 25 лет, не болевшим, не привитым, привитым однократно.
Противопоказания к вакцинации:
1. Иммунодефицитные состояния.
2. Аллергия к аминогликозидам, белку куриных яиц.
3. Беременность.
Прививки проводят по окончании острого или обострения хронического заболевания, не ранее чем через 3 месяца после иммуносупрессивной терапии и не ранее чем через 3 месяца после введения иммуноглобулинов человека. При введении иммуноглобулина ранее чем через 14 дней после вакцинации прививку против краснухи надо повторить. Вакцинируемых женщин предупреждают, что надо избегать беременности в течение 3 месяцев, однако если беременность в эти сроки наступит, то не прерывают ее, так как не зарегистрировано ни одного случая заболевания плода. Кормление грудью не является противопоказанием.
В случае контакта беременной с больным краснухой, ее восприимчивость должна определяться серологически. В случае наличия IgG противокраснушных антител женщина считается иммунной. При отсутствии антител пробу крови берут повторно через 4-5 недель. При положительном результате (инфицирование вирусом краснухи произошло) женщине предлагают прерывание беременности. Если вторая проба не содержит антител, берут еще 1 пробу через 1 месяц - интерпретация такая же.
Использование иммуноглобулина человека в целях постэкспозиционной профилактики при беременности не рекомендуется, его вводят только в тех случаях, когда женщина не желает прерывать беременность. Ограниченные наблюдения показали, что введение 16%-го раствора им-муноглобулина в дозе 0,55 мл/кг может предотвратить инфицирование или изменить течение заболевания. Однако определенный процент женщин остается незащищенным, а дети имеют СВК.
Вакцинация в первые три дня от начала контакта снижает риск развития клинически выраженных форм болезни. Вакцинация в более поздние сроки неэффективна.
Иммунопрофилактика полиомиелита
Отечественная оральная полиомиелитная вакцина (ОПВ) включает в себя аттенуированные штаммы вирусов полиомиелита трех типов. Препарат содержит в одной прививочной дозе инфекционных единиц:
• тип 1 - не менее 1 000 000,
• тип 2 - не менее 100 000,
• тип 3 - не менее 300 000
и представляет собой жидкость красно-оранжевого цвета, без осадка и посторонних примесей.
ОПВ имитирует инфекционный процесс и формирует длительный гуморальный и местный иммунитет у 90-95% привитых уже после первой вакцинации. Необходимость повторных прививок обусловлена возможной интерференцией между тремя типами вирусов и, как следствие, недостаточным иммунным ответом на один из них.
ОПВ обычно не вызывает реакций. Инактивированная полиомиелитная вакцина (ИПВ) зарубежного производства может содержать следы стрептомицина и неомицина, поэтому возможны реакции у лиц с аллергией к этим препаратам.
Первая и вторая вакцинация в курсе прививок против полиомиелита проводится ИПВ, а третья вакцинация и последующие ревакцинации ОПВ.
Реакции на введение ОПВ крайне редки. Могут быть сыпь, крапивница, отек Квинке. У ослабленных и иммунодефицитных детей введение живой полиомиелитной вакцины может спровоцировать развитие вакцин-ассоциированного паралитического полиомиелита.
В очаге полиомиелита все невакцинированные должны получить вакцину, а при наличии противопоказаний к ее введению, им вводят иммуноглобулин человечека нормальный.
Иммунопрофилактика гепатита В
В России вакцинация против ВГВ введена Приказом МЗ РФ № 226 от 8 июня 1996 г., предусматривающим прививки как детей первого года жизни, так и лиц группы риска. Плановая иммунизация детей первого года жизни осуществляется по двум схемам с учетом риска заражения новорожденно го от матери. Первая схема – трехкратная вакцинация в возрасте 0-1-6 мес. Вторая схема – четырехкратная вакцинация в возрасте 0-1-2-12 мес. Дети от 1 года до 18 лет и взрослые от 18 до 55 лет не привитые ранее подлежат трехкратной вакцинации по схеме – 0-1-6 мес.
Контактные лица из очагов вирусного гепатита В не болевшие, не привитые и не имеющие сведений о профилактических прививках против гепатита В тоже подлежат вакцинации.
Вакцину вводят внутримышечно, детям и подросткам - в передне- латеральную поверхность бедра, взрослым - в дельтовидную мышцу.
Вакцины высоко иммуногенны, их трехкратное введение сопрово-ждается образованием антител в защитном титре у 95-99% привитых сроком 8 лет и более. Ревакцинация не проводится.
Вакцинопрофилактика туберкулеза
В России используют вакцины БЦЖ и БЦЖ-М, которые представляют собой живые микобактерии штамма БЦЖ-1, лиофильно высушенные в 1,5%-м растворе глютамата натрия.
Одна ампула вакцины БЦЖ содержит 1,00+0,01 мг вакцины (20 доз по 0,05 мг), одна ампула вакцины БЦЖ-М - 0,50+0,01 мг вакцины (20 доз по 0,025 мг). В упаковке 5 ампул вакцины и 5 ампул растворителя - 0,9%-го раствора натрия хлорида по 2 мл.
БЦЖ и БЦЖ-М применяют как для вакцинации, так и для ревакци-нации. В неблагополучных по туберкулезу регионах лучше использовать БЦЖ.
Вакцину БЦЖ-М прививают новорожденным детям. Однако, на территориях с показателем заболеваемости туберкулезом более 80.000 населения и в случае, если в семье новорожденного очаг туберкулеза, ему вводят вакцину БЦЖ. Новорожденных с патологией, не привитых на 4-й день жизни, вакцинируют перед выпиской. Дети, не вакцинированные в роддоме, должны быть привиты БЦЖ-М в течение 1-6 месяцев жизни. Дети старше 2 месяцев, не привитые в роддоме, вакцинируются в поликлинике после постановки пробы Манту при ее отрицательном результате.
БЦЖ и БЦЖ-М вводят внутрикожно в дозе 0,050 и 0,025 мг соответственно в объеме 0,1 мл и при первичной вакцинации, и при ревакцинации. Вакцинацию здоровых новорожденных проводят на 4-й день жизни в утренние часы после осмотра педиатром. В день вакцинации другие манипуляции не проводятся. Введение подкожно недопустимо, так как возможен «холодный» абсцесс. Запрещаются наложение повязки и обработка места введения вакцины йодом и другими дезинфицирующими растворами.
Ревакцинации подлежат дети в декретированных возрастах, имеющие отрицательный результат пробы Манту с 2 туберкулезными единицами (ТЕ) очищенного туберкулина. Интервал между постановкой пробы Манту и ревакцинацией должен быть не менее 3 дней и не более 2 недель.
1-я ревакцинация проводится в 7 лет, 2-я ревакцинация - в 14 лет.
Вакцина БЦЖ обладает достаточно высокой профилактической активностью, при правильной вакцинации новорожденных она составляет 60-90% в отношении диссеминированного туберкулеза и туберкулинового менингита, несколько ниже - в отношении других форм туберкулеза.
Как правило, на месте внутрикожного введения БЦЖ и БЦЖ-М раз-вивается специфическая реакция в виде инфильтрата размером 5-10 мм с небольшим узелком в центре и с образованием корочки по типу оспенной; в ряде случаев - пустуляция. Иногда в центре инфильтрата может быть небольшой некроз с незначительным серозным отделяемым. У новорожденных прививочная реакция появляется на 4-6-й неделе после прививки; после ревакцинации - уже на первой неделе. Обратное развитие обычно происходит в течение 2-4 месяцев, иногда позднее. После этого при хорошей технике у 90-95% привитых остается поверхностный рубчик (3-10 мм).
Осложнениями могут быть подкожные холодные абсцессы; язвы величиной 10 мм и более на месте введения; регионарный лимфаденит, келлоидные рубцы величиной >10 мм. Очень редко - БЦЖ-остеиты и диссеминированные формы БЦЖ-инфекции (обычно у детей с дефектом клеточного иммунитета).
Противопоказаниями к вакцинации БЦЖ и БЦЖ-М являются вес новорожденных менее 2000 г, острые инфекционные заболевания и обострение хронических. Не прививаются дети, в семье которых имелись больные иммунодефицитом или генерализованной формой БЦЖ-инфекции.
Противопоказаниями также являются:
1. Иммунодефицитные состояния, злокачественные заболевания крови и новообразования. При назначении иммунодепрессантов и лучевой терапии, прививку проводят не ранее, чем через 12 месяцев после окончания лечения.
2. Активный или перенесенный туберкулез и инфицирование микобактериями.
3. Положительная или сомнительная реакция Манту с 2ТЕ очищенного туберкулина.
4. Осложнение на предыдущее введение БЦЖ или БЦЖ-М (киллоидные рубцы, лимфаденит и др.).
Вакцинопрофилактика гриппа
Вакцинопрофилактика снижает заболеваемость гриппом. У привитых инфекция протекает легко, уменьшается частота осложнений и из-быточной.
Правильно организованная иммунопрофилактика гриппа сопрово-ждается снижением заболеваемости другими ОРВИ, по данным различных исследователей, до 65%.
Вакцинация против гриппа дает высокий экономический эффект. Один рубль, вложенный в прививки, дает до 25 рублей экономии за счет сокращения затрат на лечение, оплату больничных листов и т.д.
Существует система международного наблюдения за изменчиво-
стью вируса, позволяющая ежегодно определять, какие штаммы являются актуальными и должны войти в состав вакцины, предназначенной для иммунопрофилактики в новом сезоне.
Выраженный противогриппозный иммунитет сохраняется у подавляющего большинства привитых в течение 1 года.
Для иммунизации против гриппа применяют трехкомпонентные расщепленные инактивированные вакцины, содержащие очищенные гемагглютинины и нейраминидазы вирусов гриппа подтипов A(H1N1), A(H3N2) и типа В. Для повышения иммуногенности вакцин добавляется иммуномодулятор (полиоксидоний).
Кратность введения вакцин против гриппа определяется возрастом и композиционным составом вакцины.
Организация профилактических прививок
Вся работа по организации и проведению профилактических прививок регламентирована действующими санитарно-эпидемиологическими правилами (СП3.3.2667-08).
Прививки проводятся в прививочном кабинете. Перед проведением прививок необходимо тщательно проверить качество препарата, его маркировку, целостность ампулы (флакона).
Нельзя использовать вакцины:
• с несоответствующими физическими свойствами (изменившийся цвет, наличие примесей и т.п.);
• нарушением целостности ампул;
• неясной или отсутствующей маркировкой на ампуле (флаконе);
• сорбированные вакцины (АКДС, АДС, АДС-М, против вирусного гепатита В), подвергшиеся замораживанию;
• живые вакцины (коревая, паротитная, краснушная и др.), под-вергшиеся действию температуры выше +8°С;
• любые вакцины, хранившиеся и транспортировавшиеся с нару-шением принципа «холодовой цепи».
Вскрытие ампул, растворение вакцин, выпускающихся в сухом виде (лиофилизированных), парентеральную вакцинацию осуществляют в соответствии с инструкцией при соблюдении правил асептики.
Флакон (ампулу) с вакциной необходимо уничтожить, если:
• были нарушены правила стерильности;
• есть подозрения о контаминации открытого мультидозного флакона;
• изменен внешний вид вакцины (хлопья, плавающие частицы, изменена окраска и т.п.);
• нарушены правила транспортировки или хранения вакцины;
• истек срок годности вакцины.
Транспортировка и хранение вакцин
Соблюдение правил хранения и транспортировки медицинских иммунобиологических препаратов (МИБП) является необходимым услови-
ем сохранения качества этих препаратов, их эффективности и безопасности применения.
«Холодовая цепь» - это бесперебойно функционирующая система, обеспечивающая оптимальный температурный режим хранения и транспортировки вакцин и других МИБП на всех этапах их следования от предприятия-изготовителя до вакцинируемого.
В системе «холодовой цепи» выделяют следующие уровни:
1-й уровень - предприятие-изготовитель МИБП;
2-й уровень - областные (республиканские, краевые) центры Гос-санэпиднадзора (ЦГСЭН) или аптечные склады;
3-й уровень - городские и районные ЦГСЭН или аптечные склады;
4-й уровень - лечебно-профилактические учреждения, осуществляющие иммунопрофилактику.
Основными компонентами «холодовой цепи» являются:
• специально обученный персонал, обеспечивающий обслуживание холодильного оборудования и правильное хранение вакцин;
• холодильное оборудование, обеспечивающее хранение и транс-портирование вакцин в оптимальных температурных условиях;
• система контроля за соблюдением требуемого температурного режима на всех этапах «холодовой цепи».
На всех этапах «холодовой цепи» должна строго проводиться регистрация поступления и дальнейшего отправления вакцин, при этом фиксируются их полное наименование, количество, номер серии, контрольный номер, срок годности, дата поступления, фамилия выдавшего и получившего вакцину работника.
Все виды препаратов на 4-м уровне «холодовой цепи» должны храниться в холодильнике при температуре от +2 до +800 С в строгом соответствии с инструкциями по их применению. Растворитель для вакцины также должен храниться в холодильнике, чтобы в случае подготовки к применению не вызвать повышения её температуры. Длительность хранения вакцины на 4-м уровне не должна превышать 1 месяца.
В каждом учреждении, где хранятся вакцины, должен иметься план экстренных мероприятий на случай возникновения аварийных ситуаций в холодовой цепи. План утверждает руководитель учреждения.
В каждом учреждении необходимо иметь достаточное количество термоконтейнеров, сумок-холодильников и хладоэлементов для транс-портирования вакцин. Разгрузка и загрузка термоконтейнеров должна осуществляться в течение не более 10 минут.
Уничтожение неиспользованных вакцин
Подлежат уничтожению МИБП:
• с истекшим сроком годности;
• хранившиеся и транспортировавшиеся с нарушением «холодовой цепи»;
• с изменившимися внешними свойствами, не обозначенными в инструкции (наличие хлопьев, инородных включений, изменение цветности, прозрачности и т.д.);
• с признаками нарушения упаковки (неплотно прилегающая пробка, раскол на ампуле и т.д.);
• с неясной или стертой маркировкой.
Уничтожение МИБП производится в том же помещении, где они хранятся.
Ампулы и флаконы с инактивированными и рекомбинантными вакцинами, иммуноглобулинами, гетерологическими сыворотками вскрываются, содержимое выливается в раковину, стекло выбрасывается в емкость для мусора без дополнительного обеззараживания.
Ампулы и флаконы с остатками живых вакцин, а также использованные тампоны, шприцы и иглы обеззараживают в соответствии с ус-тановленными требованиями.
Для обеззараживания живых вакцин и загрязненных ими поверхностей используют дезинфекционные средства в соответствии с инструкцией по применению.
Контрольные вопросы
1. Какие инфекции ликвидированы в Российской Федерации? Стратегию на ликвидацию каких инфекций рассматривает ВОЗ?
2. Какой документ определяет вопросы взаимоотношений медработника и пациента по вопросам иммунизации?
3. Можно ли продолжить иммунизацию пациента после развития обычной (нормальной) местной и общей реакции на вакцину?
4. Каковы условия хранения иммунобиологических препаратов в лечебно-профилактическом учреждении?
5. Может ли быть использована вакцина в ампуле со стертой мар-кировкой?
Инфекции дыхательных путей в структуре инфекционной (паразитарной) патологии занимают первое место. Среди инфекций дыхательных путей доминируют заболевания гриппом и другими острыми респираторными вирусными инфекциями (ОРВИ), удельный вес которых превышает 90%. Эти инфекции имеют наибольшую социально-экономическую значимость, так как во время сезонных подъемов заболеваемости ими переболевает более 50% трудоспособного населения. В связи с этим, проблема профилактики сезонных эпидемий гриппа и других ОРВИ представляется весьма актуальной. Высокий уровень заболеваемости ОРВИ связан с исключительной легкостью распространения вирусов среди восприимчивых контингентов и в организованных коллективах людей (детские дошкольные учреждения, учащиеся, в транспорте, внутри семьи и т.д.).
Инфекции дыхательных путей относят к антропонозам. Источником инфекции является больной человек, носитель. Многим инфекциям дыхательных путей присуща заразительность в конце инкубации. Велика опасность больных как источника инфекции в продромальном периоде, гораздо больше, чем в период разгара болезни. Легкость и быстрота распространения возбудителя этих инфекций приводит в условиях восприимчивого коллектива к высокому уровню заболеваемости. Наиболее поражаемые возрастные группы – дети. Сезонная неравномерность заболеваемости этими инфекциями в значительной степени определена неодинаковыми возможностями общения людей на протяжении разных сезонов года.
У беременных заболевание гриппом и ОРВИ наиболее опасно, т.к. вирусы могут проходить через плацентарный барьер, что может привести к не вынашиванию беременности, аномалиям или отставании плода в развитии.
Профилактические и противоэпидемические мероприятия при этих инфекциях направлены как на источник возбудителя, механизм передачи, так и восприимчивый контингент. Наибольшая эпидемиологическая эффективность достигается при комплексе мероприятий в отношении восприимчивых контингентов, а именно, проведение иммунопрофилактики. Наличие в настоящее время эффективных вакцин и рациональное их применение, позволяет выделить инфекции, управляемые средствами иммунопрофилактики.
Кроме вакцинации, для профилактики гриппа и ОРВИ используют медикаментозные препараты, обладающие противовирусным действием: интерфероны, индукторы эндогенного интерферона и ингибиторы нейраминидазы (препятствующие проникновению вируса в клетку).
Вакцинация. Для специфической профилактики гриппа используют живые, инактивированные и химические вакцины. Вакцинацию проводят в осеннее-зимний период. Вакцинация снижает уровень заболеваемости и способствует более легкому, не осложненному течению инфекции. Национальный календарь профилактических прививок предусматривает ежегодную вакцинацию против гриппа с 6 месячного возраста.
Неспецифическая профилактика: химиопрепараты, и иммунопрепараты (препараты интерферона и индукторы интерферона). Применяют методы и средства, предупреждающие заражение: адаптогены, витамины, закаливание (табл. 5.2).
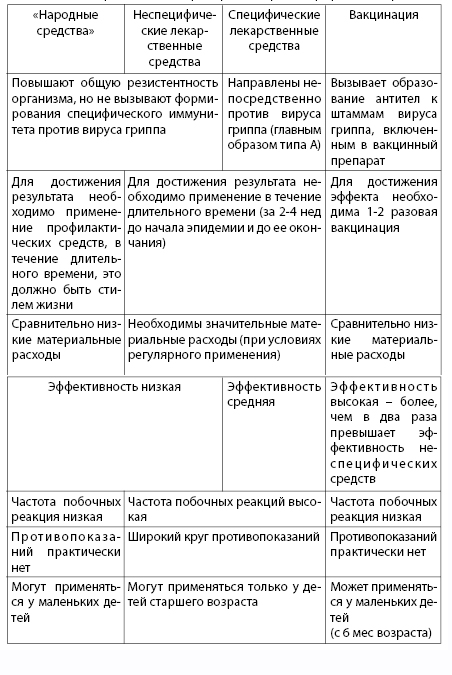
Таблица 5.2. Сравнительная характеристика средств профилактики гриппа
Права граждан, как потребителей медицинских услуг, защищает также Закон РФ «О защите прав потребителей» от 07 февраля 1992 г. (ст. 4, 5, 6, 7, 8, 10, 11, 12, 13, 16). В этих статьях закреплена ответственность за предоставляемые услуги, их качество, ненадлежащую информацию, причиненный ущерб, в том числе здоровью. Потребитель же имеет права на безопасность предоставляемых услуг, полную информацию о предоставляемых услугах, возмещение ущерба, льготы и судебную защиту.
Виды иммунобиологических препаратов
В практике здравоохранения для иммунопрофилактики инфекционных болезней используют следующие типы вакцин.
1. Живые вакцины – микроорганизмы с ослабленной или утраченной вирулентностью (вакцинные штаммы).
2. Инактивированны (корпускулярные) вакцины – микроорганизмы, инактивированные химическим (фенол, формалин, спирт и др.) или физическим (нагревание, ультрафиолетовое излучение) способом.
3. Химические (молекулярные) вакцины – протективные антигены микроорганизмов, выделенные с помощью физико-химических и/или иммунохимических методов.
4. Анатоксины – обезвреженные экзотоксины микроорганизмов.
5. Рекомбинантные вакцины – полученные при использовании генно-инженерной технологии.
Иммунопрофилактика коклюша, дифтерии, столбняка
Специфическая профилатика коклюша, дифтерии и столбняка про-водится АКДС-вакциной.
Отечественная коклюшно-дифтерийно-столбнячная вакцина соответствует международным требованиям. Она применяется в рамках Национального календаря профилактических прививок. АКДС-вакцина состоит из убитых коклюшных микробов и очищенных дифтерийного и столбнячного анатоксинов, адсорбированных на гидроокиси алюминия. В 1 мл препарата содержится 20 млрд коклюшных клеток, 30 единиц дифтерийного и 10 единиц столбнячного анатоксина.
Прививки АКДС начинают с 3-месячного возраста. Курс вакцинации состоит из трех прививок с интервалом 1,5 месяца. Сокращение интервалов не допускается, а при необходимости увеличивается, но по возможности прививку проводят в ближайший срок, определяемый состоянием здоровья детей. Переболевшим коклюшем детям делают прививку АДС-анатоксином. АКДС возможно совмещать с прививкой против полиомиелита и вирусного гепатита В. Последующие прививки поводят не ранее чем через 1 месяц. Ревакцинацию АКДС проводят через 12 месяцев после окончания курса вакцинации. Если вакцинация АКДС не проведена до 4-летнего возраста, то иммунизацию проводят АДС-анатоксином (от 4 до 5 лет 11 мес.) или АДС-М-анатоксином (в возрасте 6 лет и старше).
Противопоказания к введению АКДС: прогрессирующие заболевания нервной системы, афебрильные судороги в анамнезе, сильная общая реакция (температура 40оС и выше в первые двое суток) или осложнение на АКДС-вакцину.
Если ребенок привит АКДС-вакциной двукратно, курс вакцинации против дифтерии и столбняка считают законченным. Если получена одна прививка АКДС, можно продолжить курс вакцинации АДС-анатоксином через 1,5 месяца в ближайший возможный день после последней прививки и 1-ю ревакцинацию провести АДС-анатоксином через 12 месяцев после законченного вакцинального курса. Если осложнение развилось после третьей вакцинации АКДС, первую ревакцинацию проводят АДС-анатоксином через 12 месяцев. Последующие ревакцинации проводят в 7, 14 лет и каждые последующие 10 лет АДС-М-анатоксином.
Дети с противопоказаниями к применению АКДС-вакцины могут прививаться АДС-анатоксином в соответствии с инструкцией по его применению.
После перенесенных острых заболеваний прививают по выздоровлению. Хронических больных - по достижении ремиссии.
АКДС-вакцину выпускают в ампулах по 1 мл (две прививочные дозы) и хранят при температуре от +2 до +80С. Препарат, подвергшийся замораживанию, к использованию не пригоден.
Иммунопрофилактика кори
Для специфической профилактики кори используется вакцина коревая культуральная живая сухая. Прививочная доза содержит не менее 1000 ТЦД50 вируса кори и не более 20 единиц антибиотика (гентамицин).
Вакцина применяется для плановой и экстренной профилактики кори.
Плановые прививки проводят двукратно (в 12 месяцев и 6 лет) детям, не болевшим корью. Интервал между вакцинацией и ревакцинацией- не менее 6 месяцев. Иммунизации также подлежат подростки и взрослые в возрасте до 35 лет, не болевшие, не привитые и не имеющие сведений о профилактических прививках против кори; контактные лица из очагов заболевания, не болевшие, не привитые и не имеющие сведений о про-филактических прививках против кори - без ограничения возраста - иммунизация против кори.
Экстренную профилактику проводят детям с 12-месячного возраста и старше, не привитым, не болевшим корью, имевшим контакт с больным корью, не позднее чем через 72 часа после контакта. Вакцину вводят подкожно, в объеме 0,5 мл под лопатку или в область плеча. Обычно поствакцинальной реакции не бывает.
Противопоказания:
1. Тяжелые формы аллергии на аминогликозиды (гентамицин, мономицин, неомицин и др.) и перепелиные (куриные) яйца.
2. Первичный иммунодефицит, злокачественные заболевания крови и новообразования.
3. Сильная реакция (температура выше 400С, отек, гиперемия 8 см в месте инъекции) или осложнения на предыдущую дозу.
4. Беременность.
5. Анафилактическая реакция на паротитную вакцину.
ВИЧ-инфекция не является противопоказанием. При временных противопоказаниях прививают после их отмены.
Вакцинацию против кори можно проводить одновременно с другими календарными прививками. В Национальном календаре профилактических прививок предусмотрено одновременная вакцинация вакцин против кори, эпидемического паротита, краснухи.
После введения препаратов иммуноглобулина человека прививки против кори проводятся не ранее чем через 3 месяца.
Иммунопрофилактика эпидемического паротита
Национальный календарь профилактических прививок устанавливает проведение двукратной иммунизации: в возрасте 12 месяцев и 6 лет. С целью профилактики используется живая вакцина паротитная (ЖВП).
Живая паротитная вакцина готовится из аттенуированного штамма вируса паротита Л-3, выращенного на культуре клеток эмбрионов япон-ских перепелов. Выпускается в сухом виде в ампулах или флаконах. Прививочная доза содержит не менее 10 000 ТЦД50 аттенуированного вируса паротита, следы неомицина или канамицина, белок сыворотки крупного рогатого скота.
Прививки против эпидемического паротита проводят ранее не болевшим детям дважды - в 12 месяцев и 6 лет. Моновакцину вводят од-новременно с вакцинами против кори и краснухи в разные участки тела. ЖВП вводят по 0,5 мл подкожно под лопатку или в наружную область плеча.
У большинства привитых паротитной вакциной поствакцинальных реакций не наблюдается.
Противопоказания:
1. Иммунодефицитные состояния (первичные и, как следствие иммуносупрессии), лейкозы, лимфомы, другие злокачественные болезни, сопровождающиеся снижением клеточного иммунитета.
2. Тяжелые формы аллергичеких реакций на аминогликозиды и яичный белок.
3. Анафилактическая реакция на коревую вакцину.
4. Беременность (ввиду теоретического риска для плода).
Прививки проводят по окончании острого заболевания или после обострения хронического. Вакцинированных женщин следует предупредить о необходимости избегать беременности в течение трех месяцев; наступление беременности в этот период, однако, не требует ее прерывания. Кормление грудью не является противопоказанием к прививке.
Иммунопрофилактика краснухи
Иммунопрофилактика краснухи введена в Национальный календарь профилактических прививок в 1997 г. Однако, массовая вакцинация началась только с 2002-2003 гг., а заболеваемость краснухой начала снижаться с 2005 года.
Вакцинацию против краснухи проводят детям от года до 18 лет и девушкам от 18 до 25 лет, не болевшим, не привитым, привитым однократно.
Противопоказания к вакцинации:
1. Иммунодефицитные состояния.
2. Аллергия к аминогликозидам, белку куриных яиц.
3. Беременность.
Прививки проводят по окончании острого или обострения хронического заболевания, не ранее чем через 3 месяца после иммуносупрессивной терапии и не ранее чем через 3 месяца после введения иммуноглобулинов человека. При введении иммуноглобулина ранее чем через 14 дней после вакцинации прививку против краснухи надо повторить. Вакцинируемых женщин предупреждают, что надо избегать беременности в течение 3 месяцев, однако если беременность в эти сроки наступит, то не прерывают ее, так как не зарегистрировано ни одного случая заболевания плода. Кормление грудью не является противопоказанием.
В случае контакта беременной с больным краснухой, ее восприимчивость должна определяться серологически. В случае наличия IgG противокраснушных антител женщина считается иммунной. При отсутствии антител пробу крови берут повторно через 4-5 недель. При положительном результате (инфицирование вирусом краснухи произошло) женщине предлагают прерывание беременности. Если вторая проба не содержит антител, берут еще 1 пробу через 1 месяц - интерпретация такая же.
Использование иммуноглобулина человека в целях постэкспозиционной профилактики при беременности не рекомендуется, его вводят только в тех случаях, когда женщина не желает прерывать беременность. Ограниченные наблюдения показали, что введение 16%-го раствора им-муноглобулина в дозе 0,55 мл/кг может предотвратить инфицирование или изменить течение заболевания. Однако определенный процент женщин остается незащищенным, а дети имеют СВК.
Вакцинация в первые три дня от начала контакта снижает риск развития клинически выраженных форм болезни. Вакцинация в более поздние сроки неэффективна.
Иммунопрофилактика полиомиелита
Отечественная оральная полиомиелитная вакцина (ОПВ) включает в себя аттенуированные штаммы вирусов полиомиелита трех типов. Препарат содержит в одной прививочной дозе инфекционных единиц:
• тип 1 - не менее 1 000 000,
• тип 2 - не менее 100 000,
• тип 3 - не менее 300 000
и представляет собой жидкость красно-оранжевого цвета, без осадка и посторонних примесей.
ОПВ имитирует инфекционный процесс и формирует длительный гуморальный и местный иммунитет у 90-95% привитых уже после первой вакцинации. Необходимость повторных прививок обусловлена возможной интерференцией между тремя типами вирусов и, как следствие, недостаточным иммунным ответом на один из них.
ОПВ обычно не вызывает реакций. Инактивированная полиомиелитная вакцина (ИПВ) зарубежного производства может содержать следы стрептомицина и неомицина, поэтому возможны реакции у лиц с аллергией к этим препаратам.
Первая и вторая вакцинация в курсе прививок против полиомиелита проводится ИПВ, а третья вакцинация и последующие ревакцинации ОПВ.
Реакции на введение ОПВ крайне редки. Могут быть сыпь, крапивница, отек Квинке. У ослабленных и иммунодефицитных детей введение живой полиомиелитной вакцины может спровоцировать развитие вакцин-ассоциированного паралитического полиомиелита.
В очаге полиомиелита все невакцинированные должны получить вакцину, а при наличии противопоказаний к ее введению, им вводят иммуноглобулин человечека нормальный.
Иммунопрофилактика гепатита В
В России вакцинация против ВГВ введена Приказом МЗ РФ № 226 от 8 июня 1996 г., предусматривающим прививки как детей первого года жизни, так и лиц группы риска. Плановая иммунизация детей первого года жизни осуществляется по двум схемам с учетом риска заражения новорожденно го от матери. Первая схема – трехкратная вакцинация в возрасте 0-1-6 мес. Вторая схема – четырехкратная вакцинация в возрасте 0-1-2-12 мес. Дети от 1 года до 18 лет и взрослые от 18 до 55 лет не привитые ранее подлежат трехкратной вакцинации по схеме – 0-1-6 мес.
Контактные лица из очагов вирусного гепатита В не болевшие, не привитые и не имеющие сведений о профилактических прививках против гепатита В тоже подлежат вакцинации.
Вакцину вводят внутримышечно, детям и подросткам - в передне- латеральную поверхность бедра, взрослым - в дельтовидную мышцу.
Вакцины высоко иммуногенны, их трехкратное введение сопрово-ждается образованием антител в защитном титре у 95-99% привитых сроком 8 лет и более. Ревакцинация не проводится.
Вакцинопрофилактика туберкулеза
В России используют вакцины БЦЖ и БЦЖ-М, которые представляют собой живые микобактерии штамма БЦЖ-1, лиофильно высушенные в 1,5%-м растворе глютамата натрия.
Одна ампула вакцины БЦЖ содержит 1,00+0,01 мг вакцины (20 доз по 0,05 мг), одна ампула вакцины БЦЖ-М - 0,50+0,01 мг вакцины (20 доз по 0,025 мг). В упаковке 5 ампул вакцины и 5 ампул растворителя - 0,9%-го раствора натрия хлорида по 2 мл.
БЦЖ и БЦЖ-М применяют как для вакцинации, так и для ревакци-нации. В неблагополучных по туберкулезу регионах лучше использовать БЦЖ.
Вакцину БЦЖ-М прививают новорожденным детям. Однако, на территориях с показателем заболеваемости туберкулезом более 80.000 населения и в случае, если в семье новорожденного очаг туберкулеза, ему вводят вакцину БЦЖ. Новорожденных с патологией, не привитых на 4-й день жизни, вакцинируют перед выпиской. Дети, не вакцинированные в роддоме, должны быть привиты БЦЖ-М в течение 1-6 месяцев жизни. Дети старше 2 месяцев, не привитые в роддоме, вакцинируются в поликлинике после постановки пробы Манту при ее отрицательном результате.
БЦЖ и БЦЖ-М вводят внутрикожно в дозе 0,050 и 0,025 мг соответственно в объеме 0,1 мл и при первичной вакцинации, и при ревакцинации. Вакцинацию здоровых новорожденных проводят на 4-й день жизни в утренние часы после осмотра педиатром. В день вакцинации другие манипуляции не проводятся. Введение подкожно недопустимо, так как возможен «холодный» абсцесс. Запрещаются наложение повязки и обработка места введения вакцины йодом и другими дезинфицирующими растворами.
Ревакцинации подлежат дети в декретированных возрастах, имеющие отрицательный результат пробы Манту с 2 туберкулезными единицами (ТЕ) очищенного туберкулина. Интервал между постановкой пробы Манту и ревакцинацией должен быть не менее 3 дней и не более 2 недель.
1-я ревакцинация проводится в 7 лет, 2-я ревакцинация - в 14 лет.
Вакцина БЦЖ обладает достаточно высокой профилактической активностью, при правильной вакцинации новорожденных она составляет 60-90% в отношении диссеминированного туберкулеза и туберкулинового менингита, несколько ниже - в отношении других форм туберкулеза.
Как правило, на месте внутрикожного введения БЦЖ и БЦЖ-М раз-вивается специфическая реакция в виде инфильтрата размером 5-10 мм с небольшим узелком в центре и с образованием корочки по типу оспенной; в ряде случаев - пустуляция. Иногда в центре инфильтрата может быть небольшой некроз с незначительным серозным отделяемым. У новорожденных прививочная реакция появляется на 4-6-й неделе после прививки; после ревакцинации - уже на первой неделе. Обратное развитие обычно происходит в течение 2-4 месяцев, иногда позднее. После этого при хорошей технике у 90-95% привитых остается поверхностный рубчик (3-10 мм).
Осложнениями могут быть подкожные холодные абсцессы; язвы величиной 10 мм и более на месте введения; регионарный лимфаденит, келлоидные рубцы величиной >10 мм. Очень редко - БЦЖ-остеиты и диссеминированные формы БЦЖ-инфекции (обычно у детей с дефектом клеточного иммунитета).
Противопоказаниями к вакцинации БЦЖ и БЦЖ-М являются вес новорожденных менее 2000 г, острые инфекционные заболевания и обострение хронических. Не прививаются дети, в семье которых имелись больные иммунодефицитом или генерализованной формой БЦЖ-инфекции.
Противопоказаниями также являются:
1. Иммунодефицитные состояния, злокачественные заболевания крови и новообразования. При назначении иммунодепрессантов и лучевой терапии, прививку проводят не ранее, чем через 12 месяцев после окончания лечения.
2. Активный или перенесенный туберкулез и инфицирование микобактериями.
3. Положительная или сомнительная реакция Манту с 2ТЕ очищенного туберкулина.
4. Осложнение на предыдущее введение БЦЖ или БЦЖ-М (киллоидные рубцы, лимфаденит и др.).
Вакцинопрофилактика гриппа
Вакцинопрофилактика снижает заболеваемость гриппом. У привитых инфекция протекает легко, уменьшается частота осложнений и из-быточной.
Правильно организованная иммунопрофилактика гриппа сопрово-ждается снижением заболеваемости другими ОРВИ, по данным различных исследователей, до 65%.
Вакцинация против гриппа дает высокий экономический эффект. Один рубль, вложенный в прививки, дает до 25 рублей экономии за счет сокращения затрат на лечение, оплату больничных листов и т.д.
Существует система международного наблюдения за изменчиво-
стью вируса, позволяющая ежегодно определять, какие штаммы являются актуальными и должны войти в состав вакцины, предназначенной для иммунопрофилактики в новом сезоне.
Выраженный противогриппозный иммунитет сохраняется у подавляющего большинства привитых в течение 1 года.
Для иммунизации против гриппа применяют трехкомпонентные расщепленные инактивированные вакцины, содержащие очищенные гемагглютинины и нейраминидазы вирусов гриппа подтипов A(H1N1), A(H3N2) и типа В. Для повышения иммуногенности вакцин добавляется иммуномодулятор (полиоксидоний).
Кратность введения вакцин против гриппа определяется возрастом и композиционным составом вакцины.
Организация профилактических прививок
Вся работа по организации и проведению профилактических прививок регламентирована действующими санитарно-эпидемиологическими правилами (СП3.3.2667-08).
Прививки проводятся в прививочном кабинете. Перед проведением прививок необходимо тщательно проверить качество препарата, его маркировку, целостность ампулы (флакона).
Нельзя использовать вакцины:
• с несоответствующими физическими свойствами (изменившийся цвет, наличие примесей и т.п.);
• нарушением целостности ампул;
• неясной или отсутствующей маркировкой на ампуле (флаконе);
• сорбированные вакцины (АКДС, АДС, АДС-М, против вирусного гепатита В), подвергшиеся замораживанию;
• живые вакцины (коревая, паротитная, краснушная и др.), под-вергшиеся действию температуры выше +8°С;
• любые вакцины, хранившиеся и транспортировавшиеся с нару-шением принципа «холодовой цепи».
Вскрытие ампул, растворение вакцин, выпускающихся в сухом виде (лиофилизированных), парентеральную вакцинацию осуществляют в соответствии с инструкцией при соблюдении правил асептики.
Флакон (ампулу) с вакциной необходимо уничтожить, если:
• были нарушены правила стерильности;
• есть подозрения о контаминации открытого мультидозного флакона;
• изменен внешний вид вакцины (хлопья, плавающие частицы, изменена окраска и т.п.);
• нарушены правила транспортировки или хранения вакцины;
• истек срок годности вакцины.
Транспортировка и хранение вакцин
Соблюдение правил хранения и транспортировки медицинских иммунобиологических препаратов (МИБП) является необходимым услови-
ем сохранения качества этих препаратов, их эффективности и безопасности применения.
«Холодовая цепь» - это бесперебойно функционирующая система, обеспечивающая оптимальный температурный режим хранения и транспортировки вакцин и других МИБП на всех этапах их следования от предприятия-изготовителя до вакцинируемого.
В системе «холодовой цепи» выделяют следующие уровни:
1-й уровень - предприятие-изготовитель МИБП;
2-й уровень - областные (республиканские, краевые) центры Гос-санэпиднадзора (ЦГСЭН) или аптечные склады;
3-й уровень - городские и районные ЦГСЭН или аптечные склады;
4-й уровень - лечебно-профилактические учреждения, осуществляющие иммунопрофилактику.
Основными компонентами «холодовой цепи» являются:
• специально обученный персонал, обеспечивающий обслуживание холодильного оборудования и правильное хранение вакцин;
• холодильное оборудование, обеспечивающее хранение и транс-портирование вакцин в оптимальных температурных условиях;
• система контроля за соблюдением требуемого температурного режима на всех этапах «холодовой цепи».
На всех этапах «холодовой цепи» должна строго проводиться регистрация поступления и дальнейшего отправления вакцин, при этом фиксируются их полное наименование, количество, номер серии, контрольный номер, срок годности, дата поступления, фамилия выдавшего и получившего вакцину работника.
Все виды препаратов на 4-м уровне «холодовой цепи» должны храниться в холодильнике при температуре от +2 до +800 С в строгом соответствии с инструкциями по их применению. Растворитель для вакцины также должен храниться в холодильнике, чтобы в случае подготовки к применению не вызвать повышения её температуры. Длительность хранения вакцины на 4-м уровне не должна превышать 1 месяца.
В каждом учреждении, где хранятся вакцины, должен иметься план экстренных мероприятий на случай возникновения аварийных ситуаций в холодовой цепи. План утверждает руководитель учреждения.
В каждом учреждении необходимо иметь достаточное количество термоконтейнеров, сумок-холодильников и хладоэлементов для транс-портирования вакцин. Разгрузка и загрузка термоконтейнеров должна осуществляться в течение не более 10 минут.
Уничтожение неиспользованных вакцин
Подлежат уничтожению МИБП:
• с истекшим сроком годности;
• хранившиеся и транспортировавшиеся с нарушением «холодовой цепи»;
• с изменившимися внешними свойствами, не обозначенными в инструкции (наличие хлопьев, инородных включений, изменение цветности, прозрачности и т.д.);
• с признаками нарушения упаковки (неплотно прилегающая пробка, раскол на ампуле и т.д.);
• с неясной или стертой маркировкой.
Уничтожение МИБП производится в том же помещении, где они хранятся.
Ампулы и флаконы с инактивированными и рекомбинантными вакцинами, иммуноглобулинами, гетерологическими сыворотками вскрываются, содержимое выливается в раковину, стекло выбрасывается в емкость для мусора без дополнительного обеззараживания.
Ампулы и флаконы с остатками живых вакцин, а также использованные тампоны, шприцы и иглы обеззараживают в соответствии с ус-тановленными требованиями.
Для обеззараживания живых вакцин и загрязненных ими поверхностей используют дезинфекционные средства в соответствии с инструкцией по применению.
Контрольные вопросы
1. Какие инфекции ликвидированы в Российской Федерации? Стратегию на ликвидацию каких инфекций рассматривает ВОЗ?
2. Какой документ определяет вопросы взаимоотношений медработника и пациента по вопросам иммунизации?
3. Можно ли продолжить иммунизацию пациента после развития обычной (нормальной) местной и общей реакции на вакцину?
4. Каковы условия хранения иммунобиологических препаратов в лечебно-профилактическом учреждении?
5. Может ли быть использована вакцина в ампуле со стертой мар-кировкой?
5.3. Профилактика сезонных эпидемий гриппа и других острых респираторных вирусных инфекций
Инфекции дыхательных путей в структуре инфекционной (паразитарной) патологии занимают первое место. Среди инфекций дыхательных путей доминируют заболевания гриппом и другими острыми респираторными вирусными инфекциями (ОРВИ), удельный вес которых превышает 90%. Эти инфекции имеют наибольшую социально-экономическую значимость, так как во время сезонных подъемов заболеваемости ими переболевает более 50% трудоспособного населения. В связи с этим, проблема профилактики сезонных эпидемий гриппа и других ОРВИ представляется весьма актуальной. Высокий уровень заболеваемости ОРВИ связан с исключительной легкостью распространения вирусов среди восприимчивых контингентов и в организованных коллективах людей (детские дошкольные учреждения, учащиеся, в транспорте, внутри семьи и т.д.).
| Наибольший риск осложнений в период сезонной заболеваемости гриппом и ОРВИ наблюдается среди следующих уязвимых контингентов: • дети; • люди преклонного возраста; • больные с различными видами иммунодефицитов, бронхолегочными заболеваниями, болезнями почек, сахарным диабетом, раком, гемофилией; • беременные женщины. |
Инфекции дыхательных путей относят к антропонозам. Источником инфекции является больной человек, носитель. Многим инфекциям дыхательных путей присуща заразительность в конце инкубации. Велика опасность больных как источника инфекции в продромальном периоде, гораздо больше, чем в период разгара болезни. Легкость и быстрота распространения возбудителя этих инфекций приводит в условиях восприимчивого коллектива к высокому уровню заболеваемости. Наиболее поражаемые возрастные группы – дети. Сезонная неравномерность заболеваемости этими инфекциями в значительной степени определена неодинаковыми возможностями общения людей на протяжении разных сезонов года.
У беременных заболевание гриппом и ОРВИ наиболее опасно, т.к. вирусы могут проходить через плацентарный барьер, что может привести к не вынашиванию беременности, аномалиям или отставании плода в развитии.
Профилактические и противоэпидемические мероприятия при этих инфекциях направлены как на источник возбудителя, механизм передачи, так и восприимчивый контингент. Наибольшая эпидемиологическая эффективность достигается при комплексе мероприятий в отношении восприимчивых контингентов, а именно, проведение иммунопрофилактики. Наличие в настоящее время эффективных вакцин и рациональное их применение, позволяет выделить инфекции, управляемые средствами иммунопрофилактики.
Кроме вакцинации, для профилактики гриппа и ОРВИ используют медикаментозные препараты, обладающие противовирусным действием: интерфероны, индукторы эндогенного интерферона и ингибиторы нейраминидазы (препятствующие проникновению вируса в клетку).
| Профилактику гриппа и ОРВИ проводят по следующим основным направлениям: • Вакцинация. • Использование химиопрепаратов. • Использование иммуномодуляторов. • Использование индукторов интерферонов. • Применение препаратов интерферонов. |
Вакцинация. Для специфической профилактики гриппа используют живые, инактивированные и химические вакцины. Вакцинацию проводят в осеннее-зимний период. Вакцинация снижает уровень заболеваемости и способствует более легкому, не осложненному течению инфекции. Национальный календарь профилактических прививок предусматривает ежегодную вакцинацию против гриппа с 6 месячного возраста.
Неспецифическая профилактика: химиопрепараты, и иммунопрепараты (препараты интерферона и индукторы интерферона). Применяют методы и средства, предупреждающие заражение: адаптогены, витамины, закаливание (табл. 5.2).
Таблица 5.2. Сравнительная характеристика средств профилактики гриппа
Препараты интерферона. Интерфероновая система является естественной защитной системой организма. Ее основная роль — ингибирование репликации вирусов. Тем самым интерфероновая система противостоит вирусным инфекциям. Достаточно часто наблюдается супрессия выработки интерферона, приводящая к пониженной сопротивляемости вирусным инфекциям, к их частым рецидивам. Даже среди популяции условно здоровых жителей г. Москвы до 20% имеют продукцию интерферона ниже нормы. Существует несколько причин уменьшения биосинтеза интерферона:
• генетические (II группа крови, синдром Дауна),
• стресс,
• недостаток витаминов и/или микроэлементов и др.
Назначение препаратов интерферонов в случае сниженной естественной продукции этого цитокина играет роль заместительной терапии, что может быть использовано как для профилактики, так и для лечения сезонных эпидемий ОРВИ вне зависимости от штамма вируса, вызвавшего эпидемию, что выгодно отличает препараты интерферонов от вакцин, которые эффективны только против конкретных штаммов.
Изначально в клинической практике применялся человеческий лейкоцитарный интерферон. Однако использование интерферона, полученного в культуре клеток человека, даже при использовании самых совершенных систем контроля не может позволить со 100% вероятностью гарантировать, что полученный препарат не содержит вирусы иммунодефицита человека, гепатитов В, С, D и др. Кроме того, несмотря на высокоэффективные методы отчистки получаемого сырья, полностью избавиться от баластных белков невозможно. Поэтому препараты человеческого лейкоцитарного интерферона потенциально являются сильными аллергенами.
Между тем, сам интерферон не является аллергеном. Поэтому, в связи с развитием генной инженерии, в последние годы чрезвычайно широко используются препараты рекомбинантного интерферона. Так как интерфероны разрушаются в желудочно-кишечном тракте, основным путем их введения является интраназальный.
Эффективность интраназального применения препаратов интерферонов сильно зависит от их лекарственной формы выпуска. Так, препараты в виде капель быстро удаляются из носовых ходов за счет сокращений ресничек эпителия, что снижает эффективность действия препарата. Более перспективным является использование интерферонов на мазевой или гелевой основе, т.к. из нее наблюдается полное всасывание препарата за счет его длительного пребывания в носовых ходах.
В настоящее время клинические и доклинические исследования показали высокую лечебную и профилактическую эффективность мази и геля рекомбинантного интерферона при гриппе и ОРВИ. Доказано отсутствие влияния препаратов на плод и потомство первого и второго поколения. С нашей точки зрения, именно мазевые и гелевые формы рекомбинантных интерферонов должны использоваться в качестве средства профилактики при контакте с пациентом с ОРВИ или гриппом, а также при первых симптомах этого заболевания – вне зависимости от того, проводилась вакцинопрофилактика или нет.
Интересно отметить, что препараты на основе рекомбинатного интерферона подавляют репликацию РНК- и ДНК-содержащих вирусов. Иммуномодулирующие свойства интерферона, такие как усиление фагоцитарной активности макрофагов, увеличение специфической цитотоксичности лимфоцитов к клеткам-мишеням обусловливают его опосредованную антибактериальную активность. Препараты рекомбинантных интерферонов на мазевой или гелевой основе обладают выраженным местным иммуномодулирующим действием и способствуют увеличению локально образующихся антител класса секреторных IgA, препятствующих фиксации и размножению патогенных микроорганизмов на слизистых оболочках, что обеспечивает профилактический эффект для профилактики вирусных и других заболеваний.
Контрольные вопросы:
1. Почему важно проводить профилактику ОРВИ?
2. Какие методы профилактики ОРВИ Вы знаете?
Кишечные инфекции – группа полиэтиологичных болезней с различиями как в эпидемиологии, так и в клинических проявлениях, но объединенные общей чертой - первичной локализацией возбудителя в желудочно-кишечном тракте.
В структуре кишечных инфекционных болезней с учетом резервуара и источника возбудителя выделяют кишечные антропонозы, зоонозы и сапронозы, что необходимо учитывать при планировании и проведении профилактической и противоэпидемической работы.
Возбудитель. Этиологическими агентами кишечных инфекций могут быть: бактерии, вирусы, простейшие и гельминты. Например, бактериальные кишечные инфекции включают: шигеллёзы, эшерихиозы, холеру, сальмонеллёзы и другие острые кишечные инфекции, вызываемые энтеробактериями родов Citrobacter, Enterobacter, Hafnia, Serratia, Proteus, Erwinia, Morganella, Prowidencia, Klebsiella и др. К вирусным кишечным инфекциям отнесены: ротавирусный гастроэнтерит, гастроэнтерит, вызываемый вирусом Норволк, энтеровирусные инфекции, полиомиелит, вирусные гепатиты А и Е. Выборка протозойных инфекций может быть представлена амебиазом, лямблиозом (гиардиоз) и др.
Резервуар и источники возбудителя: человек, больной острой или хронической формой кишечной инфекции, а также носитель – реконвалесцент или транзиторный. Источником кишечной инфекции для человека могут быть многие виды животных и птиц, в том числе сельскохозяйственных и диких. Кроме того резервуар сохранения возбудителя кишечных инфекций - абиотические объекты (почва и вода).
Механизм передачи возбудителя фекально-оральный: пути передачи – водный, пищевой (факторы передачи – разнообразные пищевые продукты, особенно молоко и молочные продукты) и бытовой (факторы передачи – контаминированные возбудителем руки, посуда, игрушки и др.).
Естественная восприимчивость людей к кишечным инфекциям высокая. Клинические проявления заболевания могут варьировать от стертых до тяжело протекающих форм.
Основные эпидемиологические и клинические признаки. Ежегодно на территории Российской Федерации регистрируют около 700-800 тыс. заболеваний кишечными инфекциями установленной и неустановленной этиологии.
Более половины из них (400-500 тыс. случаев) составляют острые кишечные инфекции (ОКИ) и пищевые токсикоинфекции неустановленной этиологии, на втором месте - ОКИ и пищевые токсикоинфекции с установленной этиологией, на третьем месте по уровню заболеваемости находятся сальмонеллезы, четвертое и пятое места занимают шигеллезы и вирусный гепатит А. Упомянутые пять нозологических форм и групп инфекций составляют подавляющее большинство (80-90%) в сумме кишечных инфекций.
Острые кишечные инфекции по своей распространенности уступают только острым респираторным (простудным) заболеваниям. Обычно пик заболеваемости кишечных инфекций приходится на летне-осенний сезон года, но и в холодное время часто встречаются кишечные инфекции, вызываемые преимущественно вирусами – то, что называют «кишечный грипп» или «ОРЗ с кишечным синдромом».
Кишечные инфекции проявляются: диареей (поносом), метеоризмом (повышенным газообразованием в кишечнике), болями в кишечнике, тошнотой, рвотой, слабостью, потливостью, повышенной температурой. От пищевого отравления кишечную инфекцию отличают более выраженные симптомы интоксикации, которые не проходят при назначении диеты в течение 2-3 дней. Наиболее тяжело кишечные инфекции протекают у детей и лиц пожилого возраста.
Некоторые кишечные инфекции имеют яркую клиническую картину. Например, для ротавирусной инфекции характерно относительно легкое течение с рвотой, водянистым стулом, сопутствующими явлениями в виде катаральных проявлений и характером эпидемии (заболевают взрослые и дети, бывшие в контакте). Дизентерия характеризуется тяжелым течением, слизистым стулом с кровью, сильными болями и спазмами в животе. Для сальмонеллеза типичен стул в виде «болотной тины» - жидкий, насыщенно зеленый.
Однако чаще всего, возбудителя ОКИ выявить не удается, поэтому диагноз может звучать: кишечная инфекция неустановленной этиологии (КИНЭ) с указанием ведущего синдрома – гастрит (рвота), энтерит (водянистый стул), колит (жидкие каловые массы). Могут быть и сочетания: гастроэнтерит, энтероколит.
Ни одна кишечная инфекция не проходит самостоятельно, при наличии подозрений на нее необходимо обращение к врачу. Только врач может подобрать адекватное лечение. Самолечение кишечных инфекций недопустимо.
Вероятность развития кишечных инфекций возрастает летом и осенью, когда появляется много овощей и фруктов, которые употребляют без термической обработки в сыром виде. Кроме того, в летнюю жару создаются благоприятные условия для накопления и размножения мик-роорганизмов, что приводит к порче продуктов питания. Не надо забывать, что у испорченных продуктов не всегда изменены их вкусовых качества. Контаминирование (обсеменение) пищевых продуктов возбудителями кишечных инфекций может происходить как в ходе приготовления тех или иных блюд, так и на этапе их реализации. Особо следует выделить возможность заражения продуктов питания возбудителями кишечных инфекций на этапе их переработки (молокозаводы, мясокомбинаты и др.).
В теплый сезон года в средних широтах активизируется «мушиный фактор» - механический перенос возбудителей кишечных инфекций. Объективный анализ значения, так называемого, «мушиного фактора» показал, что:
• мухи не являются биологическими хозяевами возбудителей кишечных инфекций;
• мухи-копрофилы за счет челночных перемещений могут на лапках и брюшке механически перенести возбудителей кишечных инфекций на пищевые продукты, но количество возбудителя при этом не может быть значительным;
• обилие мух может привести к тому, что механический перенос возбудителей на пищевые продукты может приобрести эпидемическое значение;
• активность мух детерминирована природными и социальными факторами.
Суммируя вышеприведенное, следует отметить, что при высокой плотности мушиной популяции, роль мух в переносе возбудителей кишечных инфекций имеет определенное значение, но в условиях средних широт и при малом числе мух в любых климатических зонах их значение в распространении кишечных инфекций ничтожно мало.
Попав тем или иным способом на(в) продукт питания, возбудитель может некоторое время сохраняться в нем, что зависит, с одной стороны, от физико-химических характеристик продукта, температуры его хранения, а с другой – от свойств (устойчивости) самого возбудителя во внешней среде. Как правило, при хранении продукта питания происходит понижение концентрации возбудителя, а затем и его гибель. Однако, в некоторых случаях, если продукт питания представляет собой благоприятную среду для размножения возбудителя, обладающего достаточной ферментативной активностью, то при хранении готовой продукции возможно накопление возбудителя при определённых температурных условиях. Это касается только бактериальных кишечных инфекций, вирусы в продукте питания могут только сохраняться, но не размножаться.
При пищевом пути распространения кишечных инфекций заболеваемость может проявляться в виде спорадических случаев и(или) локальных вспышек.
Распространению кишечных инфекций также способствует купание в открытых водоемах. Следует отметить, что многие из возбудителей кишечных инфекций не только могут успешно противостоять процессам самоочищения объектов внешней среды, но и способны при определенных условиях вегетировать в воде или почве (например, лептоспиры, листерии, иерсинии псевдотуберкулеза и др.).
Водный путь распространения кишечных инфекций реализуется в том случае, если происходит контаминация воды возбудителями кишечных инфекций. Например, подсос фекально загрязненной воды в централизованные сети водоснабжения при аварии на канализационном коллекторе. Этот процесс заражения воды может быть либо кратковременным (моментным), либо длительным (постоянным). Соответственно, различают острые или хронические водные эпидемии и вспышки.
Контактно-бытовой путь передачи возбудителей кишечных инфекций реализуется за счет контаминированных предметов обихода (игрушки, посуда и т. д.) прежде всего в организованных детских коллективах, в которых не соблюдается предусмотренный необходимый санитарно-гигиенический режим.
Варианты реализации пищевого и водного путей заражений весьма разнообразны и зависят также от эколого-биологических свойств возбудителя (прежде всего от его вирулентности и устойчивости во внешней среде), способа контаминации пищевых продуктов и воды. Вместе с тем эколого-биологические особенности возбудителей кишечных инфекций и особенности их взаимодействия с организмом человека определяют формы клинического течения болезни и её эпидемиологические проявления.
Профилактические мероприятия
Кишечные инфекции относят к категории болезней, управляемых санитарно-гигиеническими мероприятиями.
Реализация фекально-орального механизма передачи возбудителя при кишечных инфекциях во многом зависит от активности путей и факторов, детерминированных социальными, биологическими и природными условиями, что определяет распространение этих инфекций среди людей.
Понимание этих процессов делает главным объектом в организации и проведении профилактических и противоэпидемических мероприятий воздействие на пути и факторы распространения кишечных инфекций. Эти мероприятия включат санитарно-гигиенический мониторинг за эпидемиологически значимыми объектами: источниками водоснабжения и водопроводной сетью, канализационной сетью и очистными сооружениями. Особого внимания требует надзор за соблюдением санитарных правил и норм на предприятиях, связанных с заготовкой, хранением, транспортировкой, переработкой и реализацией пищевых продуктов (общественное питание, торговля), а также в дошкольных детских учреждениях, учебных и лечебных учреждениях.
Большое значение имеет санитарно-гигиеническое образование населения, в том числе детей и подростков, по вопросам профилактики острых кишечных инфекций, а также гигиеническое обучение работников эпидемиологически значимых профессий (декретированный контингент). Работников этих профессий с целью выявления среди них больных и носителей острых кишечных инфекций при поступлении на работу подвергают клинико-лабораторным обследованиям с оформлением медицинских книжек.
Для выявления источников кишечных инфекций среди детей, посещающих дошкольные образовательные учреждения, школы-интернаты и летние оздоровительные учреждения в период формирования детских коллективов (конец лета – начало осени) и после любого перенесенного заболевания или длительного отсутствия (5 и более дней) их обследуют бактериологически и устанавливают за ними медицинское наблюдение в течение 7 дней.
Иммунопрофилактика кишечных инфекций имеет дополнительное значение; вопрос о её проведении решают в зависимости от эпидемиологической ситуации и возможности заражения для определённых профессиональных и возрастных групп населения (например, брюшной тиф, холера, вирусный гепатит А).
Профилактика кишечных инфекций практически полностью зависит от соблюдения санитарно-гигиенических правил. Если соблюдать правила гигиены, то кишечных инфекций быть не должно!
Эти инфекции часто называют «болезнями грязных рук», поэтому их профилактика целиком и полностью зависит от санитарно - гигиенической культуры каждого из нас!
Экспертами Всемирной Организации Здравоохранения для эффективного санитарного просвещения населения всей планеты по профилактике ОКИ были разработаны десять «золотых» правил для предотвращения пищевых отравлений (инфекций).
• генетические (II группа крови, синдром Дауна),
• стресс,
• недостаток витаминов и/или микроэлементов и др.
Назначение препаратов интерферонов в случае сниженной естественной продукции этого цитокина играет роль заместительной терапии, что может быть использовано как для профилактики, так и для лечения сезонных эпидемий ОРВИ вне зависимости от штамма вируса, вызвавшего эпидемию, что выгодно отличает препараты интерферонов от вакцин, которые эффективны только против конкретных штаммов.
Изначально в клинической практике применялся человеческий лейкоцитарный интерферон. Однако использование интерферона, полученного в культуре клеток человека, даже при использовании самых совершенных систем контроля не может позволить со 100% вероятностью гарантировать, что полученный препарат не содержит вирусы иммунодефицита человека, гепатитов В, С, D и др. Кроме того, несмотря на высокоэффективные методы отчистки получаемого сырья, полностью избавиться от баластных белков невозможно. Поэтому препараты человеческого лейкоцитарного интерферона потенциально являются сильными аллергенами.
Между тем, сам интерферон не является аллергеном. Поэтому, в связи с развитием генной инженерии, в последние годы чрезвычайно широко используются препараты рекомбинантного интерферона. Так как интерфероны разрушаются в желудочно-кишечном тракте, основным путем их введения является интраназальный.
Эффективность интраназального применения препаратов интерферонов сильно зависит от их лекарственной формы выпуска. Так, препараты в виде капель быстро удаляются из носовых ходов за счет сокращений ресничек эпителия, что снижает эффективность действия препарата. Более перспективным является использование интерферонов на мазевой или гелевой основе, т.к. из нее наблюдается полное всасывание препарата за счет его длительного пребывания в носовых ходах.
В настоящее время клинические и доклинические исследования показали высокую лечебную и профилактическую эффективность мази и геля рекомбинантного интерферона при гриппе и ОРВИ. Доказано отсутствие влияния препаратов на плод и потомство первого и второго поколения. С нашей точки зрения, именно мазевые и гелевые формы рекомбинантных интерферонов должны использоваться в качестве средства профилактики при контакте с пациентом с ОРВИ или гриппом, а также при первых симптомах этого заболевания – вне зависимости от того, проводилась вакцинопрофилактика или нет.
Интересно отметить, что препараты на основе рекомбинатного интерферона подавляют репликацию РНК- и ДНК-содержащих вирусов. Иммуномодулирующие свойства интерферона, такие как усиление фагоцитарной активности макрофагов, увеличение специфической цитотоксичности лимфоцитов к клеткам-мишеням обусловливают его опосредованную антибактериальную активность. Препараты рекомбинантных интерферонов на мазевой или гелевой основе обладают выраженным местным иммуномодулирующим действием и способствуют увеличению локально образующихся антител класса секреторных IgA, препятствующих фиксации и размножению патогенных микроорганизмов на слизистых оболочках, что обеспечивает профилактический эффект для профилактики вирусных и других заболеваний.
Контрольные вопросы:
1. Почему важно проводить профилактику ОРВИ?
2. Какие методы профилактики ОРВИ Вы знаете?
5.3 Профилактика кишечных инфекций
Кишечные инфекции – группа полиэтиологичных болезней с различиями как в эпидемиологии, так и в клинических проявлениях, но объединенные общей чертой - первичной локализацией возбудителя в желудочно-кишечном тракте.
В структуре кишечных инфекционных болезней с учетом резервуара и источника возбудителя выделяют кишечные антропонозы, зоонозы и сапронозы, что необходимо учитывать при планировании и проведении профилактической и противоэпидемической работы.
Возбудитель. Этиологическими агентами кишечных инфекций могут быть: бактерии, вирусы, простейшие и гельминты. Например, бактериальные кишечные инфекции включают: шигеллёзы, эшерихиозы, холеру, сальмонеллёзы и другие острые кишечные инфекции, вызываемые энтеробактериями родов Citrobacter, Enterobacter, Hafnia, Serratia, Proteus, Erwinia, Morganella, Prowidencia, Klebsiella и др. К вирусным кишечным инфекциям отнесены: ротавирусный гастроэнтерит, гастроэнтерит, вызываемый вирусом Норволк, энтеровирусные инфекции, полиомиелит, вирусные гепатиты А и Е. Выборка протозойных инфекций может быть представлена амебиазом, лямблиозом (гиардиоз) и др.
Резервуар и источники возбудителя: человек, больной острой или хронической формой кишечной инфекции, а также носитель – реконвалесцент или транзиторный. Источником кишечной инфекции для человека могут быть многие виды животных и птиц, в том числе сельскохозяйственных и диких. Кроме того резервуар сохранения возбудителя кишечных инфекций - абиотические объекты (почва и вода).
Механизм передачи возбудителя фекально-оральный: пути передачи – водный, пищевой (факторы передачи – разнообразные пищевые продукты, особенно молоко и молочные продукты) и бытовой (факторы передачи – контаминированные возбудителем руки, посуда, игрушки и др.).
Естественная восприимчивость людей к кишечным инфекциям высокая. Клинические проявления заболевания могут варьировать от стертых до тяжело протекающих форм.
Основные эпидемиологические и клинические признаки. Ежегодно на территории Российской Федерации регистрируют около 700-800 тыс. заболеваний кишечными инфекциями установленной и неустановленной этиологии.
Более половины из них (400-500 тыс. случаев) составляют острые кишечные инфекции (ОКИ) и пищевые токсикоинфекции неустановленной этиологии, на втором месте - ОКИ и пищевые токсикоинфекции с установленной этиологией, на третьем месте по уровню заболеваемости находятся сальмонеллезы, четвертое и пятое места занимают шигеллезы и вирусный гепатит А. Упомянутые пять нозологических форм и групп инфекций составляют подавляющее большинство (80-90%) в сумме кишечных инфекций.
Острые кишечные инфекции по своей распространенности уступают только острым респираторным (простудным) заболеваниям. Обычно пик заболеваемости кишечных инфекций приходится на летне-осенний сезон года, но и в холодное время часто встречаются кишечные инфекции, вызываемые преимущественно вирусами – то, что называют «кишечный грипп» или «ОРЗ с кишечным синдромом».
Кишечные инфекции проявляются: диареей (поносом), метеоризмом (повышенным газообразованием в кишечнике), болями в кишечнике, тошнотой, рвотой, слабостью, потливостью, повышенной температурой. От пищевого отравления кишечную инфекцию отличают более выраженные симптомы интоксикации, которые не проходят при назначении диеты в течение 2-3 дней. Наиболее тяжело кишечные инфекции протекают у детей и лиц пожилого возраста.
Некоторые кишечные инфекции имеют яркую клиническую картину. Например, для ротавирусной инфекции характерно относительно легкое течение с рвотой, водянистым стулом, сопутствующими явлениями в виде катаральных проявлений и характером эпидемии (заболевают взрослые и дети, бывшие в контакте). Дизентерия характеризуется тяжелым течением, слизистым стулом с кровью, сильными болями и спазмами в животе. Для сальмонеллеза типичен стул в виде «болотной тины» - жидкий, насыщенно зеленый.
Однако чаще всего, возбудителя ОКИ выявить не удается, поэтому диагноз может звучать: кишечная инфекция неустановленной этиологии (КИНЭ) с указанием ведущего синдрома – гастрит (рвота), энтерит (водянистый стул), колит (жидкие каловые массы). Могут быть и сочетания: гастроэнтерит, энтероколит.
Ни одна кишечная инфекция не проходит самостоятельно, при наличии подозрений на нее необходимо обращение к врачу. Только врач может подобрать адекватное лечение. Самолечение кишечных инфекций недопустимо.
Вероятность развития кишечных инфекций возрастает летом и осенью, когда появляется много овощей и фруктов, которые употребляют без термической обработки в сыром виде. Кроме того, в летнюю жару создаются благоприятные условия для накопления и размножения мик-роорганизмов, что приводит к порче продуктов питания. Не надо забывать, что у испорченных продуктов не всегда изменены их вкусовых качества. Контаминирование (обсеменение) пищевых продуктов возбудителями кишечных инфекций может происходить как в ходе приготовления тех или иных блюд, так и на этапе их реализации. Особо следует выделить возможность заражения продуктов питания возбудителями кишечных инфекций на этапе их переработки (молокозаводы, мясокомбинаты и др.).
В теплый сезон года в средних широтах активизируется «мушиный фактор» - механический перенос возбудителей кишечных инфекций. Объективный анализ значения, так называемого, «мушиного фактора» показал, что:
• мухи не являются биологическими хозяевами возбудителей кишечных инфекций;
• мухи-копрофилы за счет челночных перемещений могут на лапках и брюшке механически перенести возбудителей кишечных инфекций на пищевые продукты, но количество возбудителя при этом не может быть значительным;
• обилие мух может привести к тому, что механический перенос возбудителей на пищевые продукты может приобрести эпидемическое значение;
• активность мух детерминирована природными и социальными факторами.
Суммируя вышеприведенное, следует отметить, что при высокой плотности мушиной популяции, роль мух в переносе возбудителей кишечных инфекций имеет определенное значение, но в условиях средних широт и при малом числе мух в любых климатических зонах их значение в распространении кишечных инфекций ничтожно мало.
Попав тем или иным способом на(в) продукт питания, возбудитель может некоторое время сохраняться в нем, что зависит, с одной стороны, от физико-химических характеристик продукта, температуры его хранения, а с другой – от свойств (устойчивости) самого возбудителя во внешней среде. Как правило, при хранении продукта питания происходит понижение концентрации возбудителя, а затем и его гибель. Однако, в некоторых случаях, если продукт питания представляет собой благоприятную среду для размножения возбудителя, обладающего достаточной ферментативной активностью, то при хранении готовой продукции возможно накопление возбудителя при определённых температурных условиях. Это касается только бактериальных кишечных инфекций, вирусы в продукте питания могут только сохраняться, но не размножаться.
При пищевом пути распространения кишечных инфекций заболеваемость может проявляться в виде спорадических случаев и(или) локальных вспышек.
Распространению кишечных инфекций также способствует купание в открытых водоемах. Следует отметить, что многие из возбудителей кишечных инфекций не только могут успешно противостоять процессам самоочищения объектов внешней среды, но и способны при определенных условиях вегетировать в воде или почве (например, лептоспиры, листерии, иерсинии псевдотуберкулеза и др.).
Водный путь распространения кишечных инфекций реализуется в том случае, если происходит контаминация воды возбудителями кишечных инфекций. Например, подсос фекально загрязненной воды в централизованные сети водоснабжения при аварии на канализационном коллекторе. Этот процесс заражения воды может быть либо кратковременным (моментным), либо длительным (постоянным). Соответственно, различают острые или хронические водные эпидемии и вспышки.
Контактно-бытовой путь передачи возбудителей кишечных инфекций реализуется за счет контаминированных предметов обихода (игрушки, посуда и т. д.) прежде всего в организованных детских коллективах, в которых не соблюдается предусмотренный необходимый санитарно-гигиенический режим.
Варианты реализации пищевого и водного путей заражений весьма разнообразны и зависят также от эколого-биологических свойств возбудителя (прежде всего от его вирулентности и устойчивости во внешней среде), способа контаминации пищевых продуктов и воды. Вместе с тем эколого-биологические особенности возбудителей кишечных инфекций и особенности их взаимодействия с организмом человека определяют формы клинического течения болезни и её эпидемиологические проявления.
Профилактические мероприятия
Кишечные инфекции относят к категории болезней, управляемых санитарно-гигиеническими мероприятиями.
Реализация фекально-орального механизма передачи возбудителя при кишечных инфекциях во многом зависит от активности путей и факторов, детерминированных социальными, биологическими и природными условиями, что определяет распространение этих инфекций среди людей.
Понимание этих процессов делает главным объектом в организации и проведении профилактических и противоэпидемических мероприятий воздействие на пути и факторы распространения кишечных инфекций. Эти мероприятия включат санитарно-гигиенический мониторинг за эпидемиологически значимыми объектами: источниками водоснабжения и водопроводной сетью, канализационной сетью и очистными сооружениями. Особого внимания требует надзор за соблюдением санитарных правил и норм на предприятиях, связанных с заготовкой, хранением, транспортировкой, переработкой и реализацией пищевых продуктов (общественное питание, торговля), а также в дошкольных детских учреждениях, учебных и лечебных учреждениях.
Большое значение имеет санитарно-гигиеническое образование населения, в том числе детей и подростков, по вопросам профилактики острых кишечных инфекций, а также гигиеническое обучение работников эпидемиологически значимых профессий (декретированный контингент). Работников этих профессий с целью выявления среди них больных и носителей острых кишечных инфекций при поступлении на работу подвергают клинико-лабораторным обследованиям с оформлением медицинских книжек.
Для выявления источников кишечных инфекций среди детей, посещающих дошкольные образовательные учреждения, школы-интернаты и летние оздоровительные учреждения в период формирования детских коллективов (конец лета – начало осени) и после любого перенесенного заболевания или длительного отсутствия (5 и более дней) их обследуют бактериологически и устанавливают за ними медицинское наблюдение в течение 7 дней.
Иммунопрофилактика кишечных инфекций имеет дополнительное значение; вопрос о её проведении решают в зависимости от эпидемиологической ситуации и возможности заражения для определённых профессиональных и возрастных групп населения (например, брюшной тиф, холера, вирусный гепатит А).
Профилактика кишечных инфекций практически полностью зависит от соблюдения санитарно-гигиенических правил. Если соблюдать правила гигиены, то кишечных инфекций быть не должно!
Эти инфекции часто называют «болезнями грязных рук», поэтому их профилактика целиком и полностью зависит от санитарно - гигиенической культуры каждого из нас!
Экспертами Всемирной Организации Здравоохранения для эффективного санитарного просвещения населения всей планеты по профилактике ОКИ были разработаны десять «золотых» правил для предотвращения пищевых отравлений (инфекций).
| 1. Выбор безопасных пищевых продуктов. Многие продукты, такие как фрукты и овощи, едят в сыром виде, в то время как другие продукты рискованно употреблять без предварительной термической обработки. Например, всегда рекомендуется покупать пастеризованное, а не сырое молоко. Во время покупки продуктов необходимо иметь в виду, что цель их последующей обработки — сделать пищу безопасной и удлинить срок ее хранения. Определенные продукты, которые потребляются сырыми, требуют тщательной мойки, например, салат. 2. Тщательное приготовление пищи. Многие сырые продукты, главным образом, птица, мясо и сырое молоко, часто обсеменены патогенными микроорганизмами. В процессе варки (жарки) бактерии уничтожаются, но нужно помнить, что температура во всех частях пищевого продукта должна достигнуть +70° С. Если мясо цыпленка все еще сырое у кости, то поместите его снова в духовку до достижения полной готовности. Замороженное мясо, рыба и птица должны тщательно оттаиваться перед кулинарной обработкой. 3. Употребление приготовленной пищи без промедления. Когда приготовленная пища охлаждается до комнатной температуры, микро-организмы в ней могут начинать размножаться. Чем дольше она остается в таком состоянии, тем больше риск получить пищевое отравление. Поэтому, в целях безопасности, необходимо употреблять пищу сразу после ее приготовления. 4. Тщательно хранение пищевых продуктов. Если пища приготовлена впрок или необходимо после употребления сохранить оставшуюся ее часть, надо иметь в виду, что она должна храниться либо горячей (около или выше +60° С) либо холодной (около или ниже +10° С). Это исключительно важное правило, особенно если пищу нужно хранить более 4-5 часов.
Приготовленную пищу для детей лучше вообще не подвергать хранению. Общая ошибка, приводящая к бесчисленным случаям пищевых отравлений — хранение в холодильнике большого количества приготовленной пищи, которая в холодильнике не может быстро полностью остыть. Когда в середине пищевого продукта слишком долго сохраняется повышенная температура (свыше +10° С), микроорганизмы могут сохранять жизнеспособность и размножаться до опасного для здоровья человека уровня. 5. Приготовленную заранее пищу необходимо тщательно подогревать. Это наилучшая мера защиты от микроорганизмов, которые могли размножиться в пищевом продукте в процессе хранения (правильное хранение угнетает рост микробов, но не уничтожает их). Еще раз, перед едой, необходимо тщательно прогреть пищу, температура в ее толще должна быть не менее +70° С. 6. Предотвращение контакта между сырыми и готовыми пищевыми продуктами. Правильно приготовленная пища может быть загрязнена путем соприкосновения с сырыми продуктами, контаминированными возбудителями кишечных инфекций. Это перекрестное (экзогенное) заражение может быть явным, когда например, сырая тушка соприкасается с готовым блюдом, или может быть скрытым, например, когда используют одну и ту же разделочную доску и нож для приготовления сырой и вареной (жареной) птицы. Подобная практика может привести к потенциальному риску экзогенного заражения продуктов и накоплению в них микроорганизмов. 7. Частое мытье рук. Необходимо тщательно мыть руки перед приготовлением еды и после каждого перерыва в процессе готовки. После разделки сырых продуктов, таких как рыба, мясо или птица, нужно опять вымыть руки, прежде чем приступить к обработке других продуктов. А если у человека, приготовляющего пищу, имеется инфицированная царапина (ранка) на руке, то ее необходимо перевязать или наложить пластырь прежде, чем приступить к приготовлению пищи. Также нужно помнить, что домашние животные — собаки, птицы и особенно, черепахи — часто являются носителями возбудителей кишечных инфекций, которые могут попасть в пищу через загрязненные руки. 8. Соблюдение в местах приготовления пищи максимально возможной чистоты. Продукты питания легко загрязняются, любая поверхность, используемая для их приготовления, должна быть чистой. Необходимо рассматривать каждый пищевой обрезок, крошки или грязные пятна (например, на разделочной доске/столе) как потенциальный резервуар сохранения и накопления микробов. Полотенца для протирания посуды должны меняться каждый день. Тряпки для мытья полов также требуют частой стирки. 9. Хранение пищи в местах, защищенных от насекомых, грызунов и других животных. Животные часто являются источниками патогенных микроорганизмов, которые вызывают пищевые отравления. Для надежной защиты продуктов необходимо хранить их в плотно закрывающихся банках (контейнерах). 10. Использование чистой воды. Чистая вода исключительно важна как для питья, так и для приготовления пищи. Если имеются сомнения в отношении качества воды, то необходимо прокипятить ее перед добавлением к пищевым продуктам или перед использованием. |
Контрольные вопросы:
1. Какие методы профилактики кишечных инфекций Вы знаете?
2. Существует ли вакцинопрофилактика кишечных инфекций?
1. Какие методы профилактики кишечных инфекций Вы знаете?
2. Существует ли вакцинопрофилактика кишечных инфекций?
5.5. Профилактика инфекций, передающихся половым путем
По оценкам ВОЗ, ежегодно в мире регистрируется около 25 млн. новых случаев инфекций, передающихся половым путем (ИППП).
Представления об этих инфекциях за последние годы претерпели большие изменения, так как уровень заболеваемости ими остается дос-таточно высоким, а при некоторых нозологических формах отмечается рост этого показателя, особенно среди лиц репродуктивного возраста. Увеличению числа больных ИППП в современных условиях способствуют различные причины (факторы):
• раннее начало половой жизни;
• большое число сексуальных партнеров;
• либерализация сексуальных отношений;
• отказ от использования барьерных методов контрацепции;
• бесконтрольное применение антибактериальных препаратов;
• самолечение;
• неэффективная система полового воспитания;
• урбанизация
и другие социальные факторы (проституция, наркомания, алкоголизация населения и др.). В тоже время абсолютное число бессимптомных случаев ИППП точно неизвестно, и в связи с этим проблема недооценивается. Следовательно, такие не выявленные и неучтенные случаи заболеваний служат естественным резервуаром сохранения и передачи возбудителей половым партнерам и новорожденным детям.
В настоящее время насчитывается более 20 ИППП, условно их можно разделить на три группы (таблица 5.3).
Таблица 5.3. Классификации ИППП
На рубеже веков частота встречаемости инфекций, передающихся половым путем, в России составила в среднем 220 на 100 тыс. населения. Особенно высокий уровень заболеваемости отмечен в возрастной группе 15-30 лет.
Все заболевания из группы данных инфекций передаются преимущественно половым путем, т.е. возможность заразиться ИППП реальна при незащищенных половых контактах, причем инфицирование может произойти при любой форме сексуальной активности (вагинальной, оральной, анальной). Кроме того, в той или иной мере все эти болезни могут передаваться от матери к ребенку - как во время беременности и родов, так и при грудном вскармливании (например, ВИЧ-инфекция).
Возникающие после ИППП осложнения, такие как хронические боли, в области малого таза, трубное бесплодие, мертворождение, вы-кидыши, аборты, врожденные инфекции, хронические рецидивирующие генитальные симптомы, злокачественные опухоли генитального тракта, определяют социально-экономическую значимость данной патологии. В связи с этим необходимо осознать всю важность профилактики ИППП для здоровья нации в целом.
Регистрация ИППП, лечение больных и выявление половых партнеров регулируются законодательно.
Коварство ИППП заключается в том, что основная масса пациентов считает себя здоровыми (в связи с отсутствием выраженных проявлений инфекции) и поэтому сохраняет привычный стиль жизни. Одинаково часто болеют мужчины и женщины, хотя, в некоторых случаях, наибольшую опасность эти заболевания представляют для мужчин. Нередко ИППП протекают совместно, например, в 70% случаев, уреаплазмоз (микоплазмоз) встречается в сочетании с трихомонозом, гонореей, хламидиозом и т.д.
Генитальные микоплазмозы (уреаплазмоз). Возбудитель - микоплазмы, семейства Mycoplasmataceae (порядок Mycoplasmatales класса Mollicutes). Известно, что человек является хозяином 16 видов микоплазм, 6 из которых выделяют в органах урогенитальной системы. Наиболее значимыми для патологии органов мочеполовой системы человека являются три представителя генитальных микоплазм: M. hominis, M. Genitalium, U. urealyticum. По результатам проведенных в последние десятилетия исследований, M. hominis и U. urealyticum относятся к условно-патогенным микроорганизмам, так как они могут быть выделены у здоровых женщин, M. genitalium - к абсолютным патогенам.
Микоплазмы играют важную роль в патогенезе острых и хронических заболеваний человека, в частности репродуктивной сферы, и связаны с различными осложнениями, которые могут развиваться спустя длительное время после инфекционно-воспалительного процесса (рев-матоидные поражения кожи, нервной системы, органов дыхательной и сердечной системы).
Бактериальный вагиноз (БВ) - общий не воспалительный синдром связанный с дисбиозом влагалищного биотопа и сопровождающийся чрезмерно высокой концентрацией облигатно и факультативно анаэробных условно-патогенных микроорганизмов и резким снижением или полным отсутствием молочнокислых бактерий во влагалищном секрете.
Частота встречаемости БВ в популяции колеблется от 4 до 64% в зависимости от обследуемого контингента. Клинико-лабораторные критерии диагностики БВ введены R. Amsel в 1983 году:
• патологические выделения из влагалища с характерным «рыбным» запахом;
• рН вагинального содержимого >4,5;
• положительный аминный тест;
• «ключевые» клетки в вагинальном отделяемом.
Эти 4 теста являются скрининговыми при проведении массовых обследований.
Неспецифический вульвовагинит (аэробный, бактериальный) - воспалительное заболевание влагалища, вызванное аэробной микрофлорой при резком снижении или отсутствии нормальной лактофлоры влагалища. Первые упоминания об этом заболевании относятся к 70-м годам прошлого столетия.
Клинические проявления при вульвовагините не имеют строгой специфичности. Примерно в 50% случаев он протекает без выраженных клинических проявлений, хотя влияние малосимптомных форм заболевания на репродуктивное здоровье едва ли не более значимо, чем при наличии жалоб, так как они остаются не выявленными и, следовательно, не леченными. Наиболее тяжелая форма проявляется десквамативным воспалительным эндокольпитом.
Диагностика неспецифического вульвовагинита включает инте-гральную характеристику состава вагинального микрофлоры, а наиболее информативными являются микроскопические и микробиологическое исследования.
Бактериальный вагиноз и неспецифический вульвовагинит - заболевания, которые сами по себе не представляют прямой угрозы здоровью женщины, но могут приводить к восходящему уретриту, воспалительным заболеваниям органов малого таза, увеличивают риск нагноений и воспаления культи шейки матки после гистерэктомии, вероятность заражения ИППП и активации латентной вирусной инфекции, могут быть ко-фактором развития злокачественных поражений гениталий, в частности шейки матки. Многими исследователями отмечена их связь с неблагоприятным исходом беременности. Риск преждевременных родов и преждевременного излития околоплодных вод возрастает в 2,6-3,8 раза. Послеродовые гнойно-воспалительные осложнения у родильниц возни-кают в 3,5-5,8 раза чаще.
Осложнения беременности: невынашивание, инфекция амниотической жидкости, хроническая внутриутробная гипоксия плода, обострение хронического пиелонефрита, анемия, несвоевременное излитие вод, хориамнионит, преждевременная отслойка нормально расположенной плаценты, патологическая кровопотеря в родах, увеличение частоты оперативного родоразрешения и гнойно-септические осложнения. Данные заболевания являются фактором риска преждевременных родов и рождения детей с низкой массой тела. Ранний ненатальный период чаще осложняется «синдромом внутриутробного инфицирования», может быть причиной церебрального паралича новорожденных.
Кандидоз является наиболее распространенным грибковым забо-леванием. Заболеваемость вагинальным кандидозом за 20 лет резко воз-росла, а в последнее десятилетие почти удвоилась и составляет 30-45% в структуре инфекционных поражений вульвы и влагалища. По данным современной литературы, 75% женщин репродуктивного возраста имеют, по крайней мере, один эпизод урогенитального кандидоза. Значительный рост заболеваемости обусловлен тем, что эта инфекция оппортунистическая и поражает прежде всего ослабленный макроорганизм, например при ВИЧ-инфекции и СПИДе.
Клинические проявления кандидоза разнообразны и зависят от характера предшествующих заболеваний, стадии патологического про-цесса, сопутствующей микробной флоры и т.д. Для урогенитального кандидоза характерны обильные или умеренные творожистые выделения из влагалища, зуд и жжение в области наружных половых органов, усиление зуда во второй половине дня, во время сна, после водных процедур, полового акта, во время менструации, неприятный запах, усиливающийся после половых контактов, частое сочетание с поражением кожных покровов наружных половых органов, зудом в области гениталий, наличием мацерированного эпидермиса.
Наиболее распространенным и доступным методом диагностики урогенитального кандидоза является микроскопическое исследование. В качестве подтверждающего диагностического метода рассматривается культуральное исследование, позволяющее выполнять количественный учет выросших колоний, видовую идентификацию и определять чувствительность выделенной культуры к антимикотикам.
Вирус папилломы человека (ВПЧ) является одним из наиболее распространенных и важных этиологических агентов ИППП. Эпидемиологические и вирусологические исследования подтверждают, что около 95% всех плоскоклеточных раков шейки матки содержат ДНК ВПЧ. Максимум заражений ВПЧ-инфекцией приходится на возраст 18-25 лет и снижается после 30 лет, когда существенно возрастает частота дисплазий и рака шейки матки, пик которого приходится на 45 лет.
Наиболее частым клиническим проявлением ВПЧ-инфекции являются генитальные бородавки. У женщин поражаются: уздечка половых губ, половые губы, клитор, уретра, лобок, промежность, перианальная область, преддверие влагалища, вход во влагалище, влагалище, шейка матки.
У мужчин поражаются: головка полового члена, внутренний листок крайней плоти, венечная борозда, уздечка, тело полового члена, мошонка, паховые области, лобок, промежность, перианальная область.
Клиническая симптоматика ИППП
При заражении ИППП клиническая симптоматика появляется не всегда и не сразу. Каждая инфекция из этой группы имеет свою про-должительность «скрытого периода» (инкубации), в течение которого нет клинической симптоматики, и заразившийся продолжает быть сексуально активным, т.е. ведет привычный образ жизни и служит источником инфекции для своего полового партнера. Даже если заболевание проявляется, клинические признаки могут быть не очень четкими или быстро исчезают. Для этих инфекций характерен полиморфизм клинических симптомов с сочетанием комплекса синдромов.
Чаще всего при ИППП могут появляться:
• симптомы и признаки уретрита, сопровождающиеся выделениями из уретры и жжением при мочеиспускании;
• белые, слизистые, зеленые, пенистые, с запахом и без него, выделения из мочеиспускательного канала (уретры);
• зуд и боль в мочеиспускательном канале;
• учащенные позывы на мочеиспускание;
• острый орхоэпиндидимит;
• баланит;
• фимоз;
• дизурия;
• боли внизу живота;
• боли в паховой области;
• изменение характера влагалищных выделений и признаки цервицита (слизисто-гнойные выделения из шейки матки, контактные кровотечения);
• повышение температуры тела;
• возможные нарушения менструального цикла;
• петехиальная, пустулезная или полиморфные сыпи;
• асимметричная артралгия, септический артрит или тензосиновит;
• конъюнктивит.
Более специфичные симптомы некоторых ИППП:
• при сифилисе на месте внедрения бледной трепонемы в кожу или слизистую оболочку через 4-5 недель с момента заражения образуется твердый шанкр. Он представляет собой эрозию или язву округлой или овальной формы с четкими границами, с покатыми краями и плотным основанием, безболезненной при дотрагивании. У женщин язва может находиться на шейке матки, что затрудняет самодиагностику. Заболевший человек не всегда может обнаружить язвы, кроме того, их возникновение может быть обусловлено другими причинами. Диагноз сифилиса под-тверждается исследованием крови. На 5-9 день после появления твердого шанкра у большинства больных формируется второй клинический симптом первичного сифилиса - регионарный склераденит. Этот симптом проявляется увеличением близлежащих лимфатических узлов, безболезненных при пальпации и не спаянных между собой и окружающими тканями. Существует также третий клинический признак первичного сифилиса- специфический лимфангиит (воспаление лимфатических сосудов), однако, по мнению большинства современных авторов, в настоящее время этот симптом не имеет диагностической значимости. Через 10-12 недель после заражения на коже и слизистых оболочках больного появляется сыпь, может начаться выпадение волос (вторичный сифилис). Третичный сифилис развивается после вторичного периода, по данным большинства авторов, спустя 3-4 года с момента заражения. Однако на современном этапе у большинства больных между вторичным и третичным периодами наблюдается скрытый период. При третичном сифилисе наблюдаются дермальные бугорковые элементы, либо формируются гиподермальные узлы - гуммы;
• генитальный герпес характеризуется периодическим появлени-ем на коже и слизистых оболочках пузырьков, которые при расчесывании или во время полового акта лопаются и превращаются в эрозии. Появление высыпаний сопровождается жжением, зудом, болями в области половых органов. Некоторые больные во время обострений ощущают недомогание, головную боль, небольшое повышение температуры.
ИППП могут протекать как в острой, так и в хронической форме, с появлением различных симптомов и синдромов.
Проблема, связанная с ИППП, намного серьезнее, чем только боль и дискомфорт, вызываемые инфекцией. Основная опасность таится в их осложнениях. Например, возбудитель сифилиса - бледная трепонема- проникает в различные органы и системы (нервную систему, сердце, печень, желудок, почки, легкие), вызывая нарушения их функции, что в далеко зашедших случаях может привести к инвалидности и смерти. Хламидийная инфекция может вызвать синдром Рейтера, характеризующийся серонегативным асимметричным олигоартритом с уретритом и/или цервицитом и глазными проявлениями (конъюнктивит, увеит).
У мужчин хроническое воспаление при нелеченных инфекциях мочеполовой системы может стать основой развития сужений (стриктур) мочеиспускательного канала. Проникая в простату, яичко и его придаток, возбудитель вызывает воспаление, что может стать причиной бесплодия и нарушения сексуальной функции. Микоплазмы и уреаплазмы прикрепляются к сперматозоидам, уменьшают их подвижность, что приводит к снижению фертильности.
Находящиеся на поверхности мужских половых клеток микроорганизмы перемещаются вместе с ними из нижележащих участков мочеполовой системы женщины (влагалище) в вышележащие (матка, маточные трубы), вызывая их воспаление. Воспаление эндометрия (слизистой матки) может привести к его атрофии и развитию в дальнейшем осложнений при беременности и родах: к аномалиям прикрепления плаценты, приращению плаценты, преждевременной ее отслойке. Перечисленные состояния могут приводить к выкидышам и преждевременным родам.
Если инфекция проникает в фаллопиевы трубы, в них развивается воспаление, которое со временем ведет к атрофии эпителия, непроходи-мости маточных труб, а это чревато внематочной беременностью, бес-плодием. При атрофии реснитчатого эпителия маточных труб (реснички не в состоянии продвигать яйцеклетку к матке), сужении их просвета яйцеклетка не попадает в полость матки, оплодотворение происходит в маточной трубе и наступает трубная беременность. При значительном сужении просвета маточных труб может развиться бесплодие.
Если беременная женщина больна, то высок риск внутриутробного инфицирования. В тяжелых случаях это приводит к прерыванию беременности на разных сроках, заболеванию новорожденного и даже смерти ребенка в ближайший после рождения период.
Существуют прямые доказательства того, что ИППП повышают риск передачи ВИЧ-инфекции половым путем, так как являются причиной поражения слизистой оболочки генитального тракта, увеличивая вероятность проникновения ВИЧ через них.
Клиническое обследование включает осмотр аногенитальной области у мужчин и женщин; обследование женщин с помощью влагалищного зеркала; бимануальное исследование органов малого таза у женщин при наличии клинических симптомов в верхних отделах генитального тракта; проктоскопия у мужчин и женщин при наличии соответствующей симптоматики или соответствующего сексуального анамнеза; обследование других органов и систем, если это необходимо при наличии определенных клинических симптомов.
Лабораторная диагностика ИППП: микробиологические (посев на питательные среды патологического материала с последующим выделением возбудителя); микроскопические (микроскопия патологического материала из уретры, шейки матки или прямой кишки, например микроскопия в темном поле, микроскопия окрашенных по Грамму, метиленовым синим); серологические и/или иммунологические методы (определение в сыворотке крови антител к возбудителю, антигенного материала или самих возбудителей, например ИФА, иммунофлуоресценция, ПЦР-диагностика и др.).
При решении вопроса о проведении того или иного исследования необходимо учитывать сложившуюся эпидемиологическую ситуацию в отношении ИППП на конкретной территории.
Клинический диагноз должен быть подтвержден тем или иным методом лабораторной диагностики по следующим причинам:
• бессимптомные формы ИППП достаточно широко распростра-нены, и их можно исключить или подтвердить только с помощью соответствующих методов лабораторной диагностики;
• постановка клинического диагноза ВИЧ-инфекции требует по-следующего обязательного лабораторного подтверждения, так как имеет очень серьезные последствия для пациентов, их половых партнеров и/или детей;
• для выбора наиболее рациональной этиотропной терапии, особенно в тех случаях, когда есть возможность определения лекарственной устойчивости микроорганизмов;
• с целью принятия решения о необходимости проведения дополнительного тестирования (так называемого теста на излеченность);
• для повышения достоверности при регистрации ИППП и подаче экстренного извещения в территориальные центры Госсанэпиднадзора.
Лабораторное исследование может быть проведено в присутствии пациента (например микроскопия мазков, отделяемого из уретры). Однако эти методы являются ориентировочными, и практически всегда требуются дополнительные лабораторные исследования. Причем любой лабораторный метод имеет свои ограничения, о чем следует предупреждать пациентов. Кроме этого, необходимо проинформировать их о возможности получения ложноположительных и ложноотрицательных результатов.
В некоторых случаях (например, ВИЧ-инфекция) при постановке диагноза необходимо проведение предтестового и послетестового кон-сультирования для принятия решения пациентом. Консультирования проводит клинический психолог, который объясняет суть проведенного тестирования в понятной и доступной для пациента форме; пациент, в свою очередь, имеет возможность задать все интересующие его вопросы. Помощь клинического психолога требуется и тогда, когда диагноз ИППП поставлен.
Самопроизвольное излечение от ИППП невозможно, а самолечение может быть недостаточным и способно привести к развитию хро-нических форм инфекции.
В настоящее время существуют лекарственные препараты, с по-мощью которых можно достигнуть клинического и микробиологического излечения при большинстве ИППП, вызванных бактериями, простейшими и эктопаразитами. Для вирусных ИППП ситуация иная: терапия противовирусными препаратами помогает уменьшить клинические проявления заболевания, достигнуть клинического излечения, но не приводит к эрадикации вируса из организма. Поэтому для снижения уровня заболеваемости вирусными ИППП рекомендуется использовать вакцины (например вакцины против гепатита В, ВПЧ), однако реально сдерживает распространение ИППП только первичная профилактика, направленная на повышение санитарной грамотности населения, формирование приверженности к здоровому образу жизни.
Профилактика. ИППП, являясь причиной разнообразных сексуальных дисгармоний, нарушения половой и репродуктивной функций, оказывают значительное влияние на ритм жизни и трудоспособность наиболее активной части населения. В связи с этим в современных условиях возрастает роль первичного уровня профилактики ИППП, направленного в первую очередь на выявление факторов риска возможного заболевания с последующим устранением действия этих факторов через принятие решения и изменение модели поведения.
Основные усилия при организации и проведении первичной профилактики ИППП должны быть направлены на половое воспитание молодежи. Строя интимные отношения на принципе взаимного доверия и уважения, следует помнить: если человек имеет более одного полового партнера, то он попадает в группу риска заражения ИППП. Чем больше половых партнеров, тем выше вероятность заражения ИППП. Если один из половых партнеров ведет упорядоченную половую жизнь, а другой - нет, то вероятность заражения ИППП велика для обоих партнеров. Необходимо отметить, что «специфически почувствовать» момент передачи возбудителя инфекции невозможно. Более того, без проведения специальных лабораторных исследований на ИППП даже медикам часто бывает трудно поставить диагноз лишь по внешнему виду наружных половых органов. Поэтому на первое место в профилактике выходит культура сексуального поведения, применение презервативов во время каждого полового акта. Латексные мужские или полиуретановые женские презервативы не только предохраняют от нежелательной беременности, но и служат надежным барьерным средством профилактики ИППП, включая ВИЧ/СПИД.
В связи со всем вышеуказанным система профилактики ИППП включает в себя следующие направления:
• раннее, полное и активное выявление больных ИППП;
• предупреждение перинатальной передачи возбудителей ИППП;
• уменьшение числа половых партнеров;
 • повышение частоты использования презервативов с увеличением степени их доступности и их пропаганда;
• повышение частоты использования презервативов с увеличением степени их доступности и их пропаганда;
• предупреждение инфицирования при переливании крови и ее препаратов (гепатиты В, С, ВИЧ-инфекция);
• разработка средств специфической профилактики; организация и проведение лабораторного (серологического, микробиологического, вирусологического, иммунологического) обследования определенных групп населения, имеющих факторы риска заболевания ИППП;
• доступность анонимного обследования на ИППП;
• информирование и просвещение населения о ведущих путях и факторах передачи возбудителей ИППП, возможных осложнениях и последствиях после перенесения ИППП.
Избежать ИППП значительно проще, чем избавиться от них. По-этому не следует пренебрегать правилами профилактики венерических заболеваний и регулярно проходить необходимое обследование, а при малейших подозрениях сразу же обращаться к врачу.
Контрольные вопросы
1. Почему так важно соблюдать меры профилактики и вовремя лечить ИППП?
2. Какие симптомы появляются у человека, заразившегося ИППП?
3. Перечислите основные осложнения ИППП.
4. Какие болезни относятся к заболеваниям, передающимся половым путем?
ВИЧ-инфекция – антропонозная вирусная хроническая инфекционная болезнь с преобладанием контактного механизма передачи. Характеризуется медленно прогрессирующим дефектом иммунной системы с развитием синдрома приобретенного иммунодефицита (СПИД), который приводит к смерти больного от оппортунистических (вторичных) инфекций, злокачественных новообразований и аутоиммунных процессов.
Возбудитель – РНК-содержащий вирус иммунодефицита человека (ВИЧ) из семейства Retroviridae. Описано два серотипа – ВИЧ-1 и ВИЧ-2. На территории Российской Федерации эпидемиологическое значение имеет ВИЧ-1. ВИЧ-2 распространен преимущественно в странах Запардой и Центральной Африки. ВИЧ- отличается высокой антигенной изменчивостью.
В естественных условиях ВИЧ может сохраняться в высушенном биосубстрате в течение нескольких часов, в жидкостях, содержащих большое количество вирусных частиц, таких как кровь и эякулят, в течение нескольких дней, а в замороженной сыворотке крови сохра няется до нескольких лет.
Нагревание до 560 С в течение 30 минут приводит к снижению инфекционного титра вируса в 100 раз, при 70-800 С вирус гибнет через 10 минут; н инактивируется под воздействием 70% этилового спират, 0,5% гипохлорита натрия. ВИЧ устойчив к высушиванию, относительно мало чувствителен к УФ-облучению, ионизирующей радиации.
инактивируется под воздействием 70% этилового спират, 0,5% гипохлорита натрия. ВИЧ устойчив к высушиванию, относительно мало чувствителен к УФ-облучению, ионизирующей радиации.
Резервуар и источники возбудителя: особенностью ВИЧ-инфекции является ее длительное бессимптомное течение. Большинство инфицированных ВИЧ могут в течение длительного времени оставаться здоровыми, не иметь каких-либо симптомов иммунодефицита или иметь лишь незначительные, маловыраженные симптомы. Эти люди лишь инфицированы ВИЧ, но не больны СПИДом. Но как ВИЧ-инфицированные, так и больные СПИДом являются источником ВИЧ и потенциально способны заражать им окружающих, т.е. источник — ВИЧ-инфицированные люди, находящиеся на любой стадии болезни, независимо от наличия или отсутствия клинических проявлений, в том числе и в период инкубации.
Механизм передачи возбудителя контактный, вертикальный и искусственный (артифициальный); путь передачи – половой, однако возможен и парентеральный; факторами передачи служат инфицированная кровь, семенная жидкость, влагалищный секрет, грудное молоко.
Вирус иммунодефицита человека может находиться во всех биологических жидкостях (кровь, сперма, вагинальный секрет, грудное молоко, слюна, слезы, спинномозговая жидкость, пот и др.), он преодолевает трансплацентарный барьер. Однако содержание вирусных частиц в биологических жидкостях различно, что и определяет их неодинаковое эпидемиологическое значение.
Пути реализации механизмов передачи возбудителя разнообразны: половой, трансплацентарный, парентеральный (инъекционный, трансфузионный, трансплантационный).
Таким образом, выделяют четыре пути передачи ВИЧ, которые могут реализоваться за счет различных факторов:
1. При половом акте (риск инфицирования варьирует от типа контакта и роли партнера); потенциально любой половой акт без использования презерватива может привести к инфицированию ВИЧ; (вероятность инфицирования при поцелуях практически равна нулю);
2. Через кровь (в т.ч. при порезах, инъекциях, через ранки и трещины на коже), кровепродукты (плазма, цельная кровь, нерекомбинантные факторы свертываемости крови, человеческие интерфероны и т.д.), ткани и органы;
3. Через колющий инструментарий (иглы, шприцы, ножницы, пирсинг и т.д.), контаминированный вирусом;
4. От матери к ребенку, как во время беременности, так и при кормлении грудью.
Естественная восприимчивость людей к ВИЧ практически стопроцентная. Фактором невосприимчивости к заражению ВИЧ может быть отсутствие определенных специфических рецепторов. В настоящее время выделяют гены (CCR5, CCR2 и SDF1), контролирующие синтез молекул, участвующих в проникновении ВИЧ в клетки хозяина.
Люди, имеющие гомозиготный генотип по этим генам устойчивы к заражению ВИЧ половым путем, а люди с гетерозиготным генотипом – менее устойчивы. Экспрессия корецептора CCR5 на поверхности лимфоцитов обнаружена только у 1% европейцев. Однако этот признак не ассоциируют с невосприимчивостью к ВИЧ при переливании крови или при внутривенном введении психоактивных веществ.
Основные эпидемиологические и клинические признаки.
ВИЧ/СПИД остается одной из серьезнейших и значительных проблем общественного здравоохранения в мире, особенно в странах с низким и средним уровнем дохода. Распространение ВИЧ-инфекции носит характер пандемии, однако в наибольшей степени поражено население стран Африки и США.
Во всех странах заболеваемость регистрируется преимущественно в крупных городах. Среди заболевших преобладают лица сексуально активного возраста.
В России эпидемиологическая ситуация в отношении ВИЧ-инфекции стала осложняться с конца 90-х годов прошедшего столетия, когда показатели заболеваемости приобрели экспоненциальный характер.
Период до 1995 г. характеризовался стабильными, но очень низкими показателями заболеваемости и пораженности. Начиная с 1996 г. в России отмечалось стремительное увеличение числа новых случаев заражения ВИЧ, связанное с распространением вируса среди потребителей внутривенных психоактивных веществ.
Показатель заболеваемости ВИЧ-инфекцией достиг своего пика в 2001 г., и ВИЧ-инфекция стала выявляться во всех территориальных образованиях Российской Федерации.
В развитии эпидемического процесса ВИЧ-инфекции важное значение принадлежит смене ведущих путей и факторов передачи возбудителя. Факторы заражения и пути передачи возбудителя в основном (90% и более) можно свести к половым контактам и внутривенному введению психоактивных веществ, доля которых в структуре установленных причин инфицирования ВИЧ на протяжении 20 лет имеет тенденцию к изменению.
Среди всех зарегистрированных ВИЧ-инфицированных, фактором заражения в 79,8% случаев было внутривенное употребление наркотиков, что явилось следствием резко возросших темпов наркотизации населения. До настоящего времени ведущим путем распространения ВИЧ-инфекции продолжает оставаться инфицирование при парентеральном употреблении наркотиков.
Последующий период с 2002 по 2004 гг. характеризовался снижением уровня заболеваемости. В 2005 г. снова зарегистрирован рост заболеваемости ВИЧ-инфекцией и увеличилась доля передачи ВИЧ-инфекции половым путем.
Сложившаяся тенденция к увеличению числа смешанного пути передачи ВИЧ делает прогноз дальнейшего развития эпидемии ВИЧ/СПИД достаточно сложным. В течение последнего десятилетия ВИЧ-инфекция в России распространялась преимущественно в нескольких группах, которые имеют факторы повышенного риска инфицирования ВИЧ. В значительной степени эти группы риска (инъекционные потребители наркотиков, работники секса и заключенные) «накладываются» друг на друга и определяют современные тенденции хода эпидемического процесса ВИЧ-инфекции на территории России. Дополнительными группами населения с высокой концентрацией ВИЧ-инфекции являются мужчины, имеющие сексуальные контакты с мужчинами и рабочие-мигранты, особенно выходцы из Центральной Азии. Будущее российской эпидемии ВИЧ-инфекции будет во многом зависеть от того, в какой степени эти группы повышенного риска послужат «мостом» для передачи вируса в гетеросексуальное население, не потребляющее наркотики.
Ежедневно в России диагностируется до 100 новых случаев заражения ВИЧ. Подавляющее число инфицированных ВИЧ россиян моложе 35 лет. Распространение ВИЧ-инфекции до настоящего времени в 80% случаев связано с внутривенным введением психоактивных веществ.
Созданная система эпидемиологического надзора за ВИЧ-инфекцией в России характеризуется:
Все заболевания из группы данных инфекций передаются преимущественно половым путем, т.е. возможность заразиться ИППП реальна при незащищенных половых контактах, причем инфицирование может произойти при любой форме сексуальной активности (вагинальной, оральной, анальной). Кроме того, в той или иной мере все эти болезни могут передаваться от матери к ребенку - как во время беременности и родов, так и при грудном вскармливании (например, ВИЧ-инфекция).
Возникающие после ИППП осложнения, такие как хронические боли, в области малого таза, трубное бесплодие, мертворождение, вы-кидыши, аборты, врожденные инфекции, хронические рецидивирующие генитальные симптомы, злокачественные опухоли генитального тракта, определяют социально-экономическую значимость данной патологии. В связи с этим необходимо осознать всю важность профилактики ИППП для здоровья нации в целом.
Регистрация ИППП, лечение больных и выявление половых партнеров регулируются законодательно.
Коварство ИППП заключается в том, что основная масса пациентов считает себя здоровыми (в связи с отсутствием выраженных проявлений инфекции) и поэтому сохраняет привычный стиль жизни. Одинаково часто болеют мужчины и женщины, хотя, в некоторых случаях, наибольшую опасность эти заболевания представляют для мужчин. Нередко ИППП протекают совместно, например, в 70% случаев, уреаплазмоз (микоплазмоз) встречается в сочетании с трихомонозом, гонореей, хламидиозом и т.д.
Генитальные микоплазмозы (уреаплазмоз). Возбудитель - микоплазмы, семейства Mycoplasmataceae (порядок Mycoplasmatales класса Mollicutes). Известно, что человек является хозяином 16 видов микоплазм, 6 из которых выделяют в органах урогенитальной системы. Наиболее значимыми для патологии органов мочеполовой системы человека являются три представителя генитальных микоплазм: M. hominis, M. Genitalium, U. urealyticum. По результатам проведенных в последние десятилетия исследований, M. hominis и U. urealyticum относятся к условно-патогенным микроорганизмам, так как они могут быть выделены у здоровых женщин, M. genitalium - к абсолютным патогенам.
Микоплазмы играют важную роль в патогенезе острых и хронических заболеваний человека, в частности репродуктивной сферы, и связаны с различными осложнениями, которые могут развиваться спустя длительное время после инфекционно-воспалительного процесса (рев-матоидные поражения кожи, нервной системы, органов дыхательной и сердечной системы).
Бактериальный вагиноз (БВ) - общий не воспалительный синдром связанный с дисбиозом влагалищного биотопа и сопровождающийся чрезмерно высокой концентрацией облигатно и факультативно анаэробных условно-патогенных микроорганизмов и резким снижением или полным отсутствием молочнокислых бактерий во влагалищном секрете.
Частота встречаемости БВ в популяции колеблется от 4 до 64% в зависимости от обследуемого контингента. Клинико-лабораторные критерии диагностики БВ введены R. Amsel в 1983 году:
• патологические выделения из влагалища с характерным «рыбным» запахом;
• рН вагинального содержимого >4,5;
• положительный аминный тест;
• «ключевые» клетки в вагинальном отделяемом.
Эти 4 теста являются скрининговыми при проведении массовых обследований.
Неспецифический вульвовагинит (аэробный, бактериальный) - воспалительное заболевание влагалища, вызванное аэробной микрофлорой при резком снижении или отсутствии нормальной лактофлоры влагалища. Первые упоминания об этом заболевании относятся к 70-м годам прошлого столетия.
Клинические проявления при вульвовагините не имеют строгой специфичности. Примерно в 50% случаев он протекает без выраженных клинических проявлений, хотя влияние малосимптомных форм заболевания на репродуктивное здоровье едва ли не более значимо, чем при наличии жалоб, так как они остаются не выявленными и, следовательно, не леченными. Наиболее тяжелая форма проявляется десквамативным воспалительным эндокольпитом.
Диагностика неспецифического вульвовагинита включает инте-гральную характеристику состава вагинального микрофлоры, а наиболее информативными являются микроскопические и микробиологическое исследования.
Бактериальный вагиноз и неспецифический вульвовагинит - заболевания, которые сами по себе не представляют прямой угрозы здоровью женщины, но могут приводить к восходящему уретриту, воспалительным заболеваниям органов малого таза, увеличивают риск нагноений и воспаления культи шейки матки после гистерэктомии, вероятность заражения ИППП и активации латентной вирусной инфекции, могут быть ко-фактором развития злокачественных поражений гениталий, в частности шейки матки. Многими исследователями отмечена их связь с неблагоприятным исходом беременности. Риск преждевременных родов и преждевременного излития околоплодных вод возрастает в 2,6-3,8 раза. Послеродовые гнойно-воспалительные осложнения у родильниц возни-кают в 3,5-5,8 раза чаще.
Осложнения беременности: невынашивание, инфекция амниотической жидкости, хроническая внутриутробная гипоксия плода, обострение хронического пиелонефрита, анемия, несвоевременное излитие вод, хориамнионит, преждевременная отслойка нормально расположенной плаценты, патологическая кровопотеря в родах, увеличение частоты оперативного родоразрешения и гнойно-септические осложнения. Данные заболевания являются фактором риска преждевременных родов и рождения детей с низкой массой тела. Ранний ненатальный период чаще осложняется «синдромом внутриутробного инфицирования», может быть причиной церебрального паралича новорожденных.
Кандидоз является наиболее распространенным грибковым забо-леванием. Заболеваемость вагинальным кандидозом за 20 лет резко воз-росла, а в последнее десятилетие почти удвоилась и составляет 30-45% в структуре инфекционных поражений вульвы и влагалища. По данным современной литературы, 75% женщин репродуктивного возраста имеют, по крайней мере, один эпизод урогенитального кандидоза. Значительный рост заболеваемости обусловлен тем, что эта инфекция оппортунистическая и поражает прежде всего ослабленный макроорганизм, например при ВИЧ-инфекции и СПИДе.
Клинические проявления кандидоза разнообразны и зависят от характера предшествующих заболеваний, стадии патологического про-цесса, сопутствующей микробной флоры и т.д. Для урогенитального кандидоза характерны обильные или умеренные творожистые выделения из влагалища, зуд и жжение в области наружных половых органов, усиление зуда во второй половине дня, во время сна, после водных процедур, полового акта, во время менструации, неприятный запах, усиливающийся после половых контактов, частое сочетание с поражением кожных покровов наружных половых органов, зудом в области гениталий, наличием мацерированного эпидермиса.
Наиболее распространенным и доступным методом диагностики урогенитального кандидоза является микроскопическое исследование. В качестве подтверждающего диагностического метода рассматривается культуральное исследование, позволяющее выполнять количественный учет выросших колоний, видовую идентификацию и определять чувствительность выделенной культуры к антимикотикам.
Вирус папилломы человека (ВПЧ) является одним из наиболее распространенных и важных этиологических агентов ИППП. Эпидемиологические и вирусологические исследования подтверждают, что около 95% всех плоскоклеточных раков шейки матки содержат ДНК ВПЧ. Максимум заражений ВПЧ-инфекцией приходится на возраст 18-25 лет и снижается после 30 лет, когда существенно возрастает частота дисплазий и рака шейки матки, пик которого приходится на 45 лет.
Наиболее частым клиническим проявлением ВПЧ-инфекции являются генитальные бородавки. У женщин поражаются: уздечка половых губ, половые губы, клитор, уретра, лобок, промежность, перианальная область, преддверие влагалища, вход во влагалище, влагалище, шейка матки.
У мужчин поражаются: головка полового члена, внутренний листок крайней плоти, венечная борозда, уздечка, тело полового члена, мошонка, паховые области, лобок, промежность, перианальная область.
Клиническая симптоматика ИППП
При заражении ИППП клиническая симптоматика появляется не всегда и не сразу. Каждая инфекция из этой группы имеет свою про-должительность «скрытого периода» (инкубации), в течение которого нет клинической симптоматики, и заразившийся продолжает быть сексуально активным, т.е. ведет привычный образ жизни и служит источником инфекции для своего полового партнера. Даже если заболевание проявляется, клинические признаки могут быть не очень четкими или быстро исчезают. Для этих инфекций характерен полиморфизм клинических симптомов с сочетанием комплекса синдромов.
| Симптом - это какой-либо отдельный признак (проявление) бо-лезни (например, симптом повышения температуры тела, головная боль, зуд, тошнота и др.). Синдром - это совокупность симптомов, которые характерны для определенного болезненного состояния. Один и тот же синдром может наблюдаться при различных болезнях. Например, синдром воспаления может быть при ангине, ушибе, роже и многих других заболеваниях, в том числе и при ИППП. Синдром воспаления составляют следующие симптомы: боль, жар, отек, покраснение, нарушение функции (например ограничение движения конечности как следствие болевого симптома). |
Чаще всего при ИППП могут появляться:
• симптомы и признаки уретрита, сопровождающиеся выделениями из уретры и жжением при мочеиспускании;
• белые, слизистые, зеленые, пенистые, с запахом и без него, выделения из мочеиспускательного канала (уретры);
• зуд и боль в мочеиспускательном канале;
• учащенные позывы на мочеиспускание;
• острый орхоэпиндидимит;
• баланит;
• фимоз;
• дизурия;
• боли внизу живота;
• боли в паховой области;
• изменение характера влагалищных выделений и признаки цервицита (слизисто-гнойные выделения из шейки матки, контактные кровотечения);
• повышение температуры тела;
• возможные нарушения менструального цикла;
• петехиальная, пустулезная или полиморфные сыпи;
• асимметричная артралгия, септический артрит или тензосиновит;
• конъюнктивит.
Более специфичные симптомы некоторых ИППП:
• при сифилисе на месте внедрения бледной трепонемы в кожу или слизистую оболочку через 4-5 недель с момента заражения образуется твердый шанкр. Он представляет собой эрозию или язву округлой или овальной формы с четкими границами, с покатыми краями и плотным основанием, безболезненной при дотрагивании. У женщин язва может находиться на шейке матки, что затрудняет самодиагностику. Заболевший человек не всегда может обнаружить язвы, кроме того, их возникновение может быть обусловлено другими причинами. Диагноз сифилиса под-тверждается исследованием крови. На 5-9 день после появления твердого шанкра у большинства больных формируется второй клинический симптом первичного сифилиса - регионарный склераденит. Этот симптом проявляется увеличением близлежащих лимфатических узлов, безболезненных при пальпации и не спаянных между собой и окружающими тканями. Существует также третий клинический признак первичного сифилиса- специфический лимфангиит (воспаление лимфатических сосудов), однако, по мнению большинства современных авторов, в настоящее время этот симптом не имеет диагностической значимости. Через 10-12 недель после заражения на коже и слизистых оболочках больного появляется сыпь, может начаться выпадение волос (вторичный сифилис). Третичный сифилис развивается после вторичного периода, по данным большинства авторов, спустя 3-4 года с момента заражения. Однако на современном этапе у большинства больных между вторичным и третичным периодами наблюдается скрытый период. При третичном сифилисе наблюдаются дермальные бугорковые элементы, либо формируются гиподермальные узлы - гуммы;
• генитальный герпес характеризуется периодическим появлени-ем на коже и слизистых оболочках пузырьков, которые при расчесывании или во время полового акта лопаются и превращаются в эрозии. Появление высыпаний сопровождается жжением, зудом, болями в области половых органов. Некоторые больные во время обострений ощущают недомогание, головную боль, небольшое повышение температуры.
ИППП могут протекать как в острой, так и в хронической форме, с появлением различных симптомов и синдромов.
Проблема, связанная с ИППП, намного серьезнее, чем только боль и дискомфорт, вызываемые инфекцией. Основная опасность таится в их осложнениях. Например, возбудитель сифилиса - бледная трепонема- проникает в различные органы и системы (нервную систему, сердце, печень, желудок, почки, легкие), вызывая нарушения их функции, что в далеко зашедших случаях может привести к инвалидности и смерти. Хламидийная инфекция может вызвать синдром Рейтера, характеризующийся серонегативным асимметричным олигоартритом с уретритом и/или цервицитом и глазными проявлениями (конъюнктивит, увеит).
У мужчин хроническое воспаление при нелеченных инфекциях мочеполовой системы может стать основой развития сужений (стриктур) мочеиспускательного канала. Проникая в простату, яичко и его придаток, возбудитель вызывает воспаление, что может стать причиной бесплодия и нарушения сексуальной функции. Микоплазмы и уреаплазмы прикрепляются к сперматозоидам, уменьшают их подвижность, что приводит к снижению фертильности.
Находящиеся на поверхности мужских половых клеток микроорганизмы перемещаются вместе с ними из нижележащих участков мочеполовой системы женщины (влагалище) в вышележащие (матка, маточные трубы), вызывая их воспаление. Воспаление эндометрия (слизистой матки) может привести к его атрофии и развитию в дальнейшем осложнений при беременности и родах: к аномалиям прикрепления плаценты, приращению плаценты, преждевременной ее отслойке. Перечисленные состояния могут приводить к выкидышам и преждевременным родам.
Если инфекция проникает в фаллопиевы трубы, в них развивается воспаление, которое со временем ведет к атрофии эпителия, непроходи-мости маточных труб, а это чревато внематочной беременностью, бес-плодием. При атрофии реснитчатого эпителия маточных труб (реснички не в состоянии продвигать яйцеклетку к матке), сужении их просвета яйцеклетка не попадает в полость матки, оплодотворение происходит в маточной трубе и наступает трубная беременность. При значительном сужении просвета маточных труб может развиться бесплодие.
Если беременная женщина больна, то высок риск внутриутробного инфицирования. В тяжелых случаях это приводит к прерыванию беременности на разных сроках, заболеванию новорожденного и даже смерти ребенка в ближайший после рождения период.
Существуют прямые доказательства того, что ИППП повышают риск передачи ВИЧ-инфекции половым путем, так как являются причиной поражения слизистой оболочки генитального тракта, увеличивая вероятность проникновения ВИЧ через них.
| Показания для проведения обследования на ИППП 1. Рискованное в отношении заражения ИППП поведение, в част-ности незащищенные половые контакты с половым партнером, у которого, возможно, имеются другие половые партнеры; особенно с тем, у кого недавно диагностирована ИППП или кто сообщил о наличии у него подозрительных симптомов. 2. Занятие коммерческим сексом (проституция) или пользование услугами работников коммерческого секса. 3. Подозрение на сексуальное насилие. 4. Наличие клинических симптомов (признаков), указывающих на вероятность инфицирования ИППП: • у женщин: симптомы в области верхних отделов генитального тракта, указывающие на возможную инфекцию органов малого таза: боли внизу живота, нарушения менструации; выделения из влагалища; • у мужчин: выделения из уретры, дизурия, кольцевидный баланит, боль в яичках; • у женщин и мужчин: изъязвления в области гениталий, боль в прямой кишке или выделения (при наличии в анамнезе анальных половых контактов), моно- или полиартрит, конъюнктивит. 5. Запланированные инструментальные манипуляции в области шейки матки у женщин, в частности при искусственном аборте, введении внутриматочных контрацептивов или запланированная процедура оплодотворения in vitro. |
Клиническое обследование включает осмотр аногенитальной области у мужчин и женщин; обследование женщин с помощью влагалищного зеркала; бимануальное исследование органов малого таза у женщин при наличии клинических симптомов в верхних отделах генитального тракта; проктоскопия у мужчин и женщин при наличии соответствующей симптоматики или соответствующего сексуального анамнеза; обследование других органов и систем, если это необходимо при наличии определенных клинических симптомов.
Лабораторная диагностика ИППП: микробиологические (посев на питательные среды патологического материала с последующим выделением возбудителя); микроскопические (микроскопия патологического материала из уретры, шейки матки или прямой кишки, например микроскопия в темном поле, микроскопия окрашенных по Грамму, метиленовым синим); серологические и/или иммунологические методы (определение в сыворотке крови антител к возбудителю, антигенного материала или самих возбудителей, например ИФА, иммунофлуоресценция, ПЦР-диагностика и др.).
При решении вопроса о проведении того или иного исследования необходимо учитывать сложившуюся эпидемиологическую ситуацию в отношении ИППП на конкретной территории.
Клинический диагноз должен быть подтвержден тем или иным методом лабораторной диагностики по следующим причинам:
• бессимптомные формы ИППП достаточно широко распростра-нены, и их можно исключить или подтвердить только с помощью соответствующих методов лабораторной диагностики;
• постановка клинического диагноза ВИЧ-инфекции требует по-следующего обязательного лабораторного подтверждения, так как имеет очень серьезные последствия для пациентов, их половых партнеров и/или детей;
• для выбора наиболее рациональной этиотропной терапии, особенно в тех случаях, когда есть возможность определения лекарственной устойчивости микроорганизмов;
• с целью принятия решения о необходимости проведения дополнительного тестирования (так называемого теста на излеченность);
• для повышения достоверности при регистрации ИППП и подаче экстренного извещения в территориальные центры Госсанэпиднадзора.
Лабораторное исследование может быть проведено в присутствии пациента (например микроскопия мазков, отделяемого из уретры). Однако эти методы являются ориентировочными, и практически всегда требуются дополнительные лабораторные исследования. Причем любой лабораторный метод имеет свои ограничения, о чем следует предупреждать пациентов. Кроме этого, необходимо проинформировать их о возможности получения ложноположительных и ложноотрицательных результатов.
В некоторых случаях (например, ВИЧ-инфекция) при постановке диагноза необходимо проведение предтестового и послетестового кон-сультирования для принятия решения пациентом. Консультирования проводит клинический психолог, который объясняет суть проведенного тестирования в понятной и доступной для пациента форме; пациент, в свою очередь, имеет возможность задать все интересующие его вопросы. Помощь клинического психолога требуется и тогда, когда диагноз ИППП поставлен.
Самопроизвольное излечение от ИППП невозможно, а самолечение может быть недостаточным и способно привести к развитию хро-нических форм инфекции.
В настоящее время существуют лекарственные препараты, с по-мощью которых можно достигнуть клинического и микробиологического излечения при большинстве ИППП, вызванных бактериями, простейшими и эктопаразитами. Для вирусных ИППП ситуация иная: терапия противовирусными препаратами помогает уменьшить клинические проявления заболевания, достигнуть клинического излечения, но не приводит к эрадикации вируса из организма. Поэтому для снижения уровня заболеваемости вирусными ИППП рекомендуется использовать вакцины (например вакцины против гепатита В, ВПЧ), однако реально сдерживает распространение ИППП только первичная профилактика, направленная на повышение санитарной грамотности населения, формирование приверженности к здоровому образу жизни.
Профилактика. ИППП, являясь причиной разнообразных сексуальных дисгармоний, нарушения половой и репродуктивной функций, оказывают значительное влияние на ритм жизни и трудоспособность наиболее активной части населения. В связи с этим в современных условиях возрастает роль первичного уровня профилактики ИППП, направленного в первую очередь на выявление факторов риска возможного заболевания с последующим устранением действия этих факторов через принятие решения и изменение модели поведения.
Основные усилия при организации и проведении первичной профилактики ИППП должны быть направлены на половое воспитание молодежи. Строя интимные отношения на принципе взаимного доверия и уважения, следует помнить: если человек имеет более одного полового партнера, то он попадает в группу риска заражения ИППП. Чем больше половых партнеров, тем выше вероятность заражения ИППП. Если один из половых партнеров ведет упорядоченную половую жизнь, а другой - нет, то вероятность заражения ИППП велика для обоих партнеров. Необходимо отметить, что «специфически почувствовать» момент передачи возбудителя инфекции невозможно. Более того, без проведения специальных лабораторных исследований на ИППП даже медикам часто бывает трудно поставить диагноз лишь по внешнему виду наружных половых органов. Поэтому на первое место в профилактике выходит культура сексуального поведения, применение презервативов во время каждого полового акта. Латексные мужские или полиуретановые женские презервативы не только предохраняют от нежелательной беременности, но и служат надежным барьерным средством профилактики ИППП, включая ВИЧ/СПИД.
В связи со всем вышеуказанным система профилактики ИППП включает в себя следующие направления:
• раннее, полное и активное выявление больных ИППП;
• предупреждение перинатальной передачи возбудителей ИППП;
• уменьшение числа половых партнеров;
 • повышение частоты использования презервативов с увеличением степени их доступности и их пропаганда;
• повышение частоты использования презервативов с увеличением степени их доступности и их пропаганда;• предупреждение инфицирования при переливании крови и ее препаратов (гепатиты В, С, ВИЧ-инфекция);
• разработка средств специфической профилактики; организация и проведение лабораторного (серологического, микробиологического, вирусологического, иммунологического) обследования определенных групп населения, имеющих факторы риска заболевания ИППП;
• доступность анонимного обследования на ИППП;
• информирование и просвещение населения о ведущих путях и факторах передачи возбудителей ИППП, возможных осложнениях и последствиях после перенесения ИППП.
Избежать ИППП значительно проще, чем избавиться от них. По-этому не следует пренебрегать правилами профилактики венерических заболеваний и регулярно проходить необходимое обследование, а при малейших подозрениях сразу же обращаться к врачу.
Контрольные вопросы
1. Почему так важно соблюдать меры профилактики и вовремя лечить ИППП?
2. Какие симптомы появляются у человека, заразившегося ИППП?
3. Перечислите основные осложнения ИППП.
4. Какие болезни относятся к заболеваниям, передающимся половым путем?
5.6. Профилактика ВИЧ/СПИДа
ВИЧ-инфекция – антропонозная вирусная хроническая инфекционная болезнь с преобладанием контактного механизма передачи. Характеризуется медленно прогрессирующим дефектом иммунной системы с развитием синдрома приобретенного иммунодефицита (СПИД), который приводит к смерти больного от оппортунистических (вторичных) инфекций, злокачественных новообразований и аутоиммунных процессов.
Возбудитель – РНК-содержащий вирус иммунодефицита человека (ВИЧ) из семейства Retroviridae. Описано два серотипа – ВИЧ-1 и ВИЧ-2. На территории Российской Федерации эпидемиологическое значение имеет ВИЧ-1. ВИЧ-2 распространен преимущественно в странах Запардой и Центральной Африки. ВИЧ- отличается высокой антигенной изменчивостью.
В естественных условиях ВИЧ может сохраняться в высушенном биосубстрате в течение нескольких часов, в жидкостях, содержащих большое количество вирусных частиц, таких как кровь и эякулят, в течение нескольких дней, а в замороженной сыворотке крови сохра няется до нескольких лет.
Нагревание до 560 С в течение 30 минут приводит к снижению инфекционного титра вируса в 100 раз, при 70-800 С вирус гибнет через 10 минут; н
 инактивируется под воздействием 70% этилового спират, 0,5% гипохлорита натрия. ВИЧ устойчив к высушиванию, относительно мало чувствителен к УФ-облучению, ионизирующей радиации.
инактивируется под воздействием 70% этилового спират, 0,5% гипохлорита натрия. ВИЧ устойчив к высушиванию, относительно мало чувствителен к УФ-облучению, ионизирующей радиации.Резервуар и источники возбудителя: особенностью ВИЧ-инфекции является ее длительное бессимптомное течение. Большинство инфицированных ВИЧ могут в течение длительного времени оставаться здоровыми, не иметь каких-либо симптомов иммунодефицита или иметь лишь незначительные, маловыраженные симптомы. Эти люди лишь инфицированы ВИЧ, но не больны СПИДом. Но как ВИЧ-инфицированные, так и больные СПИДом являются источником ВИЧ и потенциально способны заражать им окружающих, т.е. источник — ВИЧ-инфицированные люди, находящиеся на любой стадии болезни, независимо от наличия или отсутствия клинических проявлений, в том числе и в период инкубации.
Механизм передачи возбудителя контактный, вертикальный и искусственный (артифициальный); путь передачи – половой, однако возможен и парентеральный; факторами передачи служат инфицированная кровь, семенная жидкость, влагалищный секрет, грудное молоко.
Вирус иммунодефицита человека может находиться во всех биологических жидкостях (кровь, сперма, вагинальный секрет, грудное молоко, слюна, слезы, спинномозговая жидкость, пот и др.), он преодолевает трансплацентарный барьер. Однако содержание вирусных частиц в биологических жидкостях различно, что и определяет их неодинаковое эпидемиологическое значение.
Пути реализации механизмов передачи возбудителя разнообразны: половой, трансплацентарный, парентеральный (инъекционный, трансфузионный, трансплантационный).
Таким образом, выделяют четыре пути передачи ВИЧ, которые могут реализоваться за счет различных факторов:
1. При половом акте (риск инфицирования варьирует от типа контакта и роли партнера); потенциально любой половой акт без использования презерватива может привести к инфицированию ВИЧ; (вероятность инфицирования при поцелуях практически равна нулю);
2. Через кровь (в т.ч. при порезах, инъекциях, через ранки и трещины на коже), кровепродукты (плазма, цельная кровь, нерекомбинантные факторы свертываемости крови, человеческие интерфероны и т.д.), ткани и органы;
3. Через колющий инструментарий (иглы, шприцы, ножницы, пирсинг и т.д.), контаминированный вирусом;
4. От матери к ребенку, как во время беременности, так и при кормлении грудью.
| ВИЧ не передается: • при рукопожатии; • кашле, чихании; • пользовании общественным телефоном; • посещении больницы; • открывании дверей; • совместной еде, использовании общих столовых приборов; • пользовании питьевыми фонтанчиками; • пользовании туалетами и душевыми комнатами; • пользовании бассейнами; • через укусы комаров или других насекомых |
Естественная восприимчивость людей к ВИЧ практически стопроцентная. Фактором невосприимчивости к заражению ВИЧ может быть отсутствие определенных специфических рецепторов. В настоящее время выделяют гены (CCR5, CCR2 и SDF1), контролирующие синтез молекул, участвующих в проникновении ВИЧ в клетки хозяина.
Люди, имеющие гомозиготный генотип по этим генам устойчивы к заражению ВИЧ половым путем, а люди с гетерозиготным генотипом – менее устойчивы. Экспрессия корецептора CCR5 на поверхности лимфоцитов обнаружена только у 1% европейцев. Однако этот признак не ассоциируют с невосприимчивостью к ВИЧ при переливании крови или при внутривенном введении психоактивных веществ.
Основные эпидемиологические и клинические признаки.
ВИЧ/СПИД остается одной из серьезнейших и значительных проблем общественного здравоохранения в мире, особенно в странах с низким и средним уровнем дохода. Распространение ВИЧ-инфекции носит характер пандемии, однако в наибольшей степени поражено население стран Африки и США.
| Социально-экономические показатели, определяющие глобальное распространение ВИЧ-инфекции: • экономические кризисы, бедность и нищета населения; • недостатки воспитания, просвещения и организации досуга молодежи; • сокращение возможностей бесплатного образования и гарантий трудоустройства молодежи; • нивелирование традиционных морально-этических ценностей с подрывом и снижением роли семьи; • рост распространенность рискованного сексуального поведения, в том числе проституции и гомосексуализма; • массовые вынужденные перемещения населения; • урбанизация, приводящая к разрыву традиционных семейных связей; • развитие транспорта и шоссейных дорог, вдоль которых распространяется проституция, возникает наркотрафик; • развитие международного туризма |
Во всех странах заболеваемость регистрируется преимущественно в крупных городах. Среди заболевших преобладают лица сексуально активного возраста.
В России эпидемиологическая ситуация в отношении ВИЧ-инфекции стала осложняться с конца 90-х годов прошедшего столетия, когда показатели заболеваемости приобрели экспоненциальный характер.
Период до 1995 г. характеризовался стабильными, но очень низкими показателями заболеваемости и пораженности. Начиная с 1996 г. в России отмечалось стремительное увеличение числа новых случаев заражения ВИЧ, связанное с распространением вируса среди потребителей внутривенных психоактивных веществ.
Показатель заболеваемости ВИЧ-инфекцией достиг своего пика в 2001 г., и ВИЧ-инфекция стала выявляться во всех территориальных образованиях Российской Федерации.
| По утверждению Объединенной Программы ООН по СПИДу (UNAIDS), «самый резкий рост случаев ВИЧ-инфекции в 1999 году был зарегистрирован на территории новых независимых государств бывшего Советского Союза: только за период с конца 1997 до конца 1999 года количество людей, живущих с ВИЧ на данной территории, увеличилось в два раза». |
В развитии эпидемического процесса ВИЧ-инфекции важное значение принадлежит смене ведущих путей и факторов передачи возбудителя. Факторы заражения и пути передачи возбудителя в основном (90% и более) можно свести к половым контактам и внутривенному введению психоактивных веществ, доля которых в структуре установленных причин инфицирования ВИЧ на протяжении 20 лет имеет тенденцию к изменению.
| Если в первые годы регистрации ВИЧ-инфекции (1996-1997 гг.) доминировал половой путь инфицирования, то затем в 1999— 2001 гг. его влияние уменьшилось и на первое место в структуре путей инфицирования ВИЧ выходит внутривенное введение психоактивных веществ. С 2000 г. отмечена тенденция роста полового пути передачи ВИЧ на фоне статистически значимого уменьшения удельного веса заражений при внутривенном введении психоактивных веществ. Доклад о неотложных мерах по борьбе с распространением ВИЧ-инфекции в Российской Федерации. – М., 2006 |
Среди всех зарегистрированных ВИЧ-инфицированных, фактором заражения в 79,8% случаев было внутривенное употребление наркотиков, что явилось следствием резко возросших темпов наркотизации населения. До настоящего времени ведущим путем распространения ВИЧ-инфекции продолжает оставаться инфицирование при парентеральном употреблении наркотиков.
Последующий период с 2002 по 2004 гг. характеризовался снижением уровня заболеваемости. В 2005 г. снова зарегистрирован рост заболеваемости ВИЧ-инфекцией и увеличилась доля передачи ВИЧ-инфекции половым путем.
Сложившаяся тенденция к увеличению числа смешанного пути передачи ВИЧ делает прогноз дальнейшего развития эпидемии ВИЧ/СПИД достаточно сложным. В течение последнего десятилетия ВИЧ-инфекция в России распространялась преимущественно в нескольких группах, которые имеют факторы повышенного риска инфицирования ВИЧ. В значительной степени эти группы риска (инъекционные потребители наркотиков, работники секса и заключенные) «накладываются» друг на друга и определяют современные тенденции хода эпидемического процесса ВИЧ-инфекции на территории России. Дополнительными группами населения с высокой концентрацией ВИЧ-инфекции являются мужчины, имеющие сексуальные контакты с мужчинами и рабочие-мигранты, особенно выходцы из Центральной Азии. Будущее российской эпидемии ВИЧ-инфекции будет во многом зависеть от того, в какой степени эти группы повышенного риска послужат «мостом» для передачи вируса в гетеросексуальное население, не потребляющее наркотики.
Ежедневно в России диагностируется до 100 новых случаев заражения ВИЧ. Подавляющее число инфицированных ВИЧ россиян моложе 35 лет. Распространение ВИЧ-инфекции до настоящего времени в 80% случаев связано с внутривенным введением психоактивных веществ.
Созданная система эпидемиологического надзора за ВИЧ-инфекцией в России характеризуется:
• единым систематическим сбором данных о всех случаях ВИЧ-инфекции, СПИДа, обследований на ВИЧ, изменения клинического состояния пациентов и исходов ВИЧ-инфекции во всех регионах Российской Федерации;
• активным выявлением ВИЧ-инфицированных при обязательном и добровольном тестировании населения;
• обязательным проведением эпидемиологического расследования каждого случая ВИЧ-инфекции (для выявления факторов риска заражения и проведения противоэпидемических и профилактических мероприятий).
Федеральным научно-методическим центром по профилактике и борьбе со СПИДом создана и поддерживается единая база данных случаев ВИЧ-инфекции, СПИДа, обследований на ВИЧ и исходов ВИЧ-инфекции. Практически во всех территориальных центрах СПИД и Федеральном центре СПИДа было установлено единое программное компьютерное обеспечение и регистр «АСОДОС», регулярная передача информации ведется по электронным каналам. Персонифицированные данные поступают ежедневно, а суммарные - ежемесячно из территориальных и региональных центров по профилактике и борьбе со СПИДом и Центров гигиены и эпидемиологии Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека.
Всемирной организацией здравоохранения 1 декабря 1988 г. был объявлен Всемирным днём борьбы со СПИДом.
Ежегодно эта дата отмечается многими странами мира для того, чтобы привлечь внимание людей к этой проблеме, выразить солидарность с людьми, затронутыми эпидемией и поддержать усилия в борьбе с ВИЧ-инфекцией во всем мире.
СПИД — сочетание опасных для организма человека инфекций, развитие которых опосредованно индуцируется ВИЧ, так как он реплицируется в определенных видах клеток, несущих CD4+ рецептор. На фоне недостаточной функции иммунной системы более тяжело протекают «обычные» инфекции, кроме того, наблюдается активация оппортунистических инфекций (тех инфекций, которые в норме не поражают человека, но проявляются в случае иммунодефицита). Собственно с развитием вторичных инфекций и (реже) опухолевого процесса связана летальность при ВИЧ-инфекции.
Период от инфицирования ВИЧ до развития СПИД длится в среднем 9 — 11 лет и смерти от вторичных заболеваний 12 лет. Статистические данные многочисленных исследований, проведённых в различных странах за период времени более двух десятилетий, подтверждают это заключение. Эти цифры справедливы лишь для случаев, когда ВИЧ-инфекция не подвергается никакой терапии.
Профилактические мероприятия
Активизация и усиление противодействия эпидемии ВИЧ/СПИД, а также преодоление ее последствий является одной из важнейших задач Российского государства.
• активным выявлением ВИЧ-инфицированных при обязательном и добровольном тестировании населения;
• обязательным проведением эпидемиологического расследования каждого случая ВИЧ-инфекции (для выявления факторов риска заражения и проведения противоэпидемических и профилактических мероприятий).
Федеральным научно-методическим центром по профилактике и борьбе со СПИДом создана и поддерживается единая база данных случаев ВИЧ-инфекции, СПИДа, обследований на ВИЧ и исходов ВИЧ-инфекции. Практически во всех территориальных центрах СПИД и Федеральном центре СПИДа было установлено единое программное компьютерное обеспечение и регистр «АСОДОС», регулярная передача информации ведется по электронным каналам. Персонифицированные данные поступают ежедневно, а суммарные - ежемесячно из территориальных и региональных центров по профилактике и борьбе со СПИДом и Центров гигиены и эпидемиологии Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека.
Всемирной организацией здравоохранения 1 декабря 1988 г. был объявлен Всемирным днём борьбы со СПИДом.
Ежегодно эта дата отмечается многими странами мира для того, чтобы привлечь внимание людей к этой проблеме, выразить солидарность с людьми, затронутыми эпидемией и поддержать усилия в борьбе с ВИЧ-инфекцией во всем мире.
СПИД — сочетание опасных для организма человека инфекций, развитие которых опосредованно индуцируется ВИЧ, так как он реплицируется в определенных видах клеток, несущих CD4+ рецептор. На фоне недостаточной функции иммунной системы более тяжело протекают «обычные» инфекции, кроме того, наблюдается активация оппортунистических инфекций (тех инфекций, которые в норме не поражают человека, но проявляются в случае иммунодефицита). Собственно с развитием вторичных инфекций и (реже) опухолевого процесса связана летальность при ВИЧ-инфекции.
Период от инфицирования ВИЧ до развития СПИД длится в среднем 9 — 11 лет и смерти от вторичных заболеваний 12 лет. Статистические данные многочисленных исследований, проведённых в различных странах за период времени более двух десятилетий, подтверждают это заключение. Эти цифры справедливы лишь для случаев, когда ВИЧ-инфекция не подвергается никакой терапии.
Профилактические мероприятия
Активизация и усиление противодействия эпидемии ВИЧ/СПИД, а также преодоление ее последствий является одной из важнейших задач Российского государства.
| Основными приоритетами в деле борьбы с эпидемией ВИЧ-инфекции в настоящее время являются: - создание на федеральном уровне единой координирующей структуры, обеспечивающей комплексное решение задач организации и проведения эффективных мероприятий по противодействию эпидемии ВИЧ-инфекции; - разработка долгосрочной стратегии по борьбе с распространением эпидемии вируса иммунного дефицита человека и преодолении ее последствий; - организация единой система мониторинга и оценка развития эпидемии ВИЧ-инфекции, ее последствий, эффективности мер, принимаемых на федеральном и региональном уровнях, и прогнозирование развития ситуации В целях реализации этих основных приоритетов необходимо обеспечить: - перевод проблемы из плоскости исключительно медицинской в область борьбы с ее социальными, экономическими и иными последствиями; - координацию работы федеральных министерств и ведомств, в том числе совместную реализация проектов в рамках единой программы по предотвращению развития эпидемии ВИЧ-инфекции; - активизацию участия регионов в разработке и реализации программы по противодействию дальнейшему распространению ВИЧ-инфекции с учетом региональной специфики; - привлечение максимального числа участников, в том числе институтов гражданского общества и самих граждан для достижения наиболее оптимальных результатов в реализации стратегии по борьбе с ВИЧ/СПИДом Доклад «О неотложных мерах по борьбе с распространением ВИЧ-инфекции в Российской Федерации». |
Знание эпидемиологических и клинических особенностей ВИЧ-инфекции позволило разработать комплекс профилактических и противоэпидемических мероприятий.
Эксперты ВОЗ все разнообразие профилактических мер при ВИЧ-инфекции свели к четырем основным:
• профилактика половой передачи ВИЧ;
• профилактика ВИЧ среди пользователей инъекционных наркотиков (ПИН);
• профилактика передачи ВИЧ от матери к ребенку (ПМР);
• контроль переливаемой крови и ее препаратов;
• предупреждение передачи ВИЧ во время хирургических и стоматологических вмешательств;
• оказание медицинской помощи и социальной поддержки ВИЧ-инфицированным, их семьям и окружающим.
Работа по предупреждению распространения ВИЧ регламентируется правовыми документами, и согласно рекомендации ВОЗ должна предусматривать следующие уровни профилактики ВИЧ-инфекции.
Первичный уровень — ограничение числа случаев СПИДа и ВИЧ-инфицирования путем воздействия на специфические причинные факторы, способствующие повышению риска заболевания. На этом этапе профилактики проводят пропаганду безопасного секса, массовый скрининг с использованием ИФА тест-систем.
Вторичный уровень — раннее выявление больных ВИЧ-инфекцией, для чего проводят поисковый скрининг среди групп риска и обследование пациентов по клиническим показаниям (ИФА, иммунный блоттинг); лечение больных ВИЧ инфекцией.
Третичный уровень — диспансерное наблюдение и реабилитация заболевших ВИЧ/СПИДом.
С 1990 г. в России начала функционировать специализированная служба по борьбе и профилактике ВИЧ-инфекции, включающая Центры по профилактике и борьбе со СПИДом (Центры СПИД), скрининговые лаборатории, кабинеты психосоциального консультирования и добровольного (анонимного) обследования на ВИЧ (кабинет профилактики ВИЧ).
Центр-СПИД осуществляет эпидемиологический надзор за ВИЧ- инфекцией, который включает: выявление ВИЧ-инфицированных и больных СПИДом путем скрининга групп риска; проведение эпидемиологического расследования всех выявленных случаев заболевания СПИДом и ВИЧ- инфицирования; верификацию лабораторных исследований на ВИЧ, проведенных в медицинских учреждениях.
Психосоциальное консультирование ВИЧ-инфицированных ведется по трем основным направлениям: в период эмоционального кризиса (кризисное консультирование), по решению проблемы и по принятию решения.
Профилактика полового пути передачи ВИЧ.
Данные о передаче ВИЧ при незащищённом половом контакте по различным источникам сильно отличаются (табл. 5.4). Риск передачи в значительной степени зависит от типа контакта (вагинальный, анальный, оральный и т. д.) и роли партнёра (вводящая сторона/принимающая сторона).
Таблица 5.4. Риск передачи ВИЧ (на 10 000 незащищённых половых контактов)
Эксперты ВОЗ все разнообразие профилактических мер при ВИЧ-инфекции свели к четырем основным:
• профилактика половой передачи ВИЧ;
• профилактика ВИЧ среди пользователей инъекционных наркотиков (ПИН);
• профилактика передачи ВИЧ от матери к ребенку (ПМР);
• контроль переливаемой крови и ее препаратов;
• предупреждение передачи ВИЧ во время хирургических и стоматологических вмешательств;
• оказание медицинской помощи и социальной поддержки ВИЧ-инфицированным, их семьям и окружающим.
Работа по предупреждению распространения ВИЧ регламентируется правовыми документами, и согласно рекомендации ВОЗ должна предусматривать следующие уровни профилактики ВИЧ-инфекции.
Первичный уровень — ограничение числа случаев СПИДа и ВИЧ-инфицирования путем воздействия на специфические причинные факторы, способствующие повышению риска заболевания. На этом этапе профилактики проводят пропаганду безопасного секса, массовый скрининг с использованием ИФА тест-систем.
Вторичный уровень — раннее выявление больных ВИЧ-инфекцией, для чего проводят поисковый скрининг среди групп риска и обследование пациентов по клиническим показаниям (ИФА, иммунный блоттинг); лечение больных ВИЧ инфекцией.
Третичный уровень — диспансерное наблюдение и реабилитация заболевших ВИЧ/СПИДом.
С 1990 г. в России начала функционировать специализированная служба по борьбе и профилактике ВИЧ-инфекции, включающая Центры по профилактике и борьбе со СПИДом (Центры СПИД), скрининговые лаборатории, кабинеты психосоциального консультирования и добровольного (анонимного) обследования на ВИЧ (кабинет профилактики ВИЧ).
Центр-СПИД осуществляет эпидемиологический надзор за ВИЧ- инфекцией, который включает: выявление ВИЧ-инфицированных и больных СПИДом путем скрининга групп риска; проведение эпидемиологического расследования всех выявленных случаев заболевания СПИДом и ВИЧ- инфицирования; верификацию лабораторных исследований на ВИЧ, проведенных в медицинских учреждениях.
Психосоциальное консультирование ВИЧ-инфицированных ведется по трем основным направлениям: в период эмоционального кризиса (кризисное консультирование), по решению проблемы и по принятию решения.
Профилактика полового пути передачи ВИЧ.
Данные о передаче ВИЧ при незащищённом половом контакте по различным источникам сильно отличаются (табл. 5.4). Риск передачи в значительной степени зависит от типа контакта (вагинальный, анальный, оральный и т. д.) и роли партнёра (вводящая сторона/принимающая сторона).
Таблица 5.4. Риск передачи ВИЧ (на 10 000 незащищённых половых контактов)
Уменьшение риска передачи ВИЧ при сексуальных контактах связано:
• с правильным использованием при каждом сексуальном контакте мужских или женских презервативов;
• занятиями только непроникающим сексом;
• привычкой сохранять верность в отношениях с неинфицированным и равным образом верным партнером и избегать каких-либо других форм рискованного поведения;
• воздержанием от секса.
Последние исследования свидетельствуют о том, что мужское обрезание может способствовать снижению риска приобретения ВИЧ во время сексуальных контактов. Однако оно не является эффективным на 100%, и мужчины, сделавшие обрезание, могут быть инфицированы. В случае, если после хирургического вмешательства раны не обработаны надлежащим образом, обрезание может даже повысить риск передачи инфекции. Кроме того, ВИЧ-позитивные мужчины, сделавшие обрезание, могут инфицировать своих сексуальных партнеров.
Несмотря на то, что мужское обрезание не заменяет другие известные способы профилактики ВИЧ, его следует рассматривать в качестве составной части всесторонней стратегии профилактики.
Мужские и женские презервативы гарантированного качества являются единственными продуктами, доступными в настоящее время для защиты от инфекций, передаваемых половым путем (ИППП), включая ВИЧ. При правильном использовании во время каждого сексуального контакта презервативы являются надежным способом профилактики ВИЧ-инфекции у женщин и мужчин. Тем не менее, ни один способ профилактики, кроме воздержания, не эффективен на 100%.
Женский презерватив является единственным контролируемым женщиной контрацептивным барьерным методом, доступным в настоящее время на рынке. Женский презерватив представляет собой прочный, мягкий, прозрачный колпачок из полиуретана, вставляемый во влагалище перед сексуальным контактом. При его правильном использовании при каждом сексуальном контакте он полностью облегает влагалище и обеспечивает защиту как от беременности, так и от ИППП, включая ВИЧ.
• с правильным использованием при каждом сексуальном контакте мужских или женских презервативов;
• занятиями только непроникающим сексом;
• привычкой сохранять верность в отношениях с неинфицированным и равным образом верным партнером и избегать каких-либо других форм рискованного поведения;
• воздержанием от секса.
Последние исследования свидетельствуют о том, что мужское обрезание может способствовать снижению риска приобретения ВИЧ во время сексуальных контактов. Однако оно не является эффективным на 100%, и мужчины, сделавшие обрезание, могут быть инфицированы. В случае, если после хирургического вмешательства раны не обработаны надлежащим образом, обрезание может даже повысить риск передачи инфекции. Кроме того, ВИЧ-позитивные мужчины, сделавшие обрезание, могут инфицировать своих сексуальных партнеров.
Несмотря на то, что мужское обрезание не заменяет другие известные способы профилактики ВИЧ, его следует рассматривать в качестве составной части всесторонней стратегии профилактики.
Мужские и женские презервативы гарантированного качества являются единственными продуктами, доступными в настоящее время для защиты от инфекций, передаваемых половым путем (ИППП), включая ВИЧ. При правильном использовании во время каждого сексуального контакта презервативы являются надежным способом профилактики ВИЧ-инфекции у женщин и мужчин. Тем не менее, ни один способ профилактики, кроме воздержания, не эффективен на 100%.
Женский презерватив является единственным контролируемым женщиной контрацептивным барьерным методом, доступным в настоящее время на рынке. Женский презерватив представляет собой прочный, мягкий, прозрачный колпачок из полиуретана, вставляемый во влагалище перед сексуальным контактом. При его правильном использовании при каждом сексуальном контакте он полностью облегает влагалище и обеспечивает защиту как от беременности, так и от ИППП, включая ВИЧ.
Профилактика ВИЧ среди пользователей инъекционных наркотиков (ПИН)
По данным ВОЗ, в мире насчитывается около 16 миллионов потребителей инъекционных наркотиков и 3 миллиона из них инфицированы ВИЧ. Но во многих странах для потребителей инъекционных наркотиков доступ к лечению наркотической зависимости и службам профилактики и лечения ВИЧ/СПИДа весьма ограничен.
К наиболее значимым профилактическим проектам среди ПИН следует отнести проекты и мероприятия, которые основываются на философии «Снижения вреда». Стратегия снижения вреда направлена на сокращение вредных последствий употребления наркотиков без требований к потребителю полностью отказаться от употребления наркотиков или другого высоко-рискованного поведения (например, предоставление сексуальных услуг за плату). Программы профилактики, которые основывается на принципе «снижения вреда» предоставляют все возможности потребителю ПАВ снизить риск вредных последствий (инфицирования ВИЧ, передозировки) посредством предоставления стерильного инструментария, доступа к экспресс-тестам на ВИЧ, презервативам, информации и т.п. Программы направлены не только на индивидуальный уровень, но и позволяют снизить риск выноса ВИЧ-инфекции из групп риска в базовые социальные слои населения. Самой важной задачей этого проекта является установление и поддержание контакта с потребителями наркотиков с целью оказания им помощи, а также разработки профилактических мероприятий, адекватных ситуации, сложившейся на конкретной территории.
По данным ВОЗ, в мире насчитывается около 16 миллионов потребителей инъекционных наркотиков и 3 миллиона из них инфицированы ВИЧ. Но во многих странах для потребителей инъекционных наркотиков доступ к лечению наркотической зависимости и службам профилактики и лечения ВИЧ/СПИДа весьма ограничен.
К наиболее значимым профилактическим проектам среди ПИН следует отнести проекты и мероприятия, которые основываются на философии «Снижения вреда». Стратегия снижения вреда направлена на сокращение вредных последствий употребления наркотиков без требований к потребителю полностью отказаться от употребления наркотиков или другого высоко-рискованного поведения (например, предоставление сексуальных услуг за плату). Программы профилактики, которые основывается на принципе «снижения вреда» предоставляют все возможности потребителю ПАВ снизить риск вредных последствий (инфицирования ВИЧ, передозировки) посредством предоставления стерильного инструментария, доступа к экспресс-тестам на ВИЧ, презервативам, информации и т.п. Программы направлены не только на индивидуальный уровень, но и позволяют снизить риск выноса ВИЧ-инфекции из групп риска в базовые социальные слои населения. Самой важной задачей этого проекта является установление и поддержание контакта с потребителями наркотиков с целью оказания им помощи, а также разработки профилактических мероприятий, адекватных ситуации, сложившейся на конкретной территории.
| Общепринятые программы «снижения вреда» в области профилактики ВИЧ среди ПИН: • консультирование лиц, употребляющих ПАВ по вопросам профилактики ВИЧ-инфекции; • опиоидная заместительной терапии; • предоставление информационных материалов, презервативов; • предоставление стерильного инъекционного инструментария (игл и шприцев, инъекционной воды, дезинфектантов, приспособлений для приготовления раствора и т.д.). Данные программы могут проводится на базе стационарных или мобильных пунктов, но требуют развитую сеть уличных «аутрич» работников; • утилизация использованного инструментария; • консультирование и направление на обследование (ВИЧ-инфекция, вирусные гепатиты, инфекции передаваемые половым путем); • направление в программы лечения наркозависимости, включая детоксикационные отделения и реабилитационные центры, • профилактика и лечение ИППП. |
Основные принципы эффективной профилактики ВИЧ-инфекции и вирусных гепатитов среди ПИН на национальном и местном уровнях были сформулированы ВОЗ, ЮНЭЙДС и Советом Европы еще в 1998 г. Подчеркивая, что стратегии и программы в этой области должны учитывать специфическую задачу - снижение уровня распространения ВИЧ-инфекции среди ПИН, эксперты определили пять основных компонентов этой деятельности:
• информирование;
• обеспечение доступа к социальным службам и услугам здравоохранения;
• социальная уличная работа среди ПИН;
• обеспечение ПИН стерильными инъекционными инструментами;
• обеспечение возможности получать опиоидную заместительную терапию.
• информирование;
• обеспечение доступа к социальным службам и услугам здравоохранения;
• социальная уличная работа среди ПИН;
• обеспечение ПИН стерильными инъекционными инструментами;
• обеспечение возможности получать опиоидную заместительную терапию.
| «Ведущие российские специалисты в области наркологии не поддерживают применение «заместительной терапии» в рамках реализации программ снижение вреда» (цит. по материалам Доклада о неотложных мерах по борьбе с распространением ВИЧ-инфекции в Российской Федерации. |
Программа «Снижение вреда» предусматривает целую систему помощи ПИН и, в тоже время, контроля за ними. Длительна выдача в терапевтических условиях заменителей «тяжелых» наркотиков более «легкими» позволяет, по мнению авторов программ, удерживать больных в поле зрения социальных и медицинских служб. Однако, существует много противников опиоидной заместительной терапии (Иванец Н.Н., Альтшелер В.Б. 2004; и др.).
Постановлением Правительства Российской Федерации от 30 июня 1998 г. № 681 утвержден Перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю.
Метадон включен в Список I наркотических средств, оборот которых в Российской Федерации запрещен в соответствии с законодательством Российской Федерации и международными договорами Российской Федерации.
Бупренорфин находится в Списке II наркотических средств, оборот которых ограничен и в отношении которых устанавливаются меры контроля в соответствии с законодательством Российской Федерации и международными договорами Российской Федерации. В соответствии с пунктом 6 ст. 31 Федерального закона от 8 января 1998 года № 3-ФЗ « О наркотических средствах и психотропных веществах» запрещается лечение наркомании наркотическими средствами и наркотическими веществами, внесенными в Список II указанного Перечня.
Протоколом заседания Правительственной комиссии Российской Федерации по противодействию злоупотреблению наркотиками и их незаконному обороту от 26.12.2003 года № 4, с учетом тенденции к расширению географии применения «опиоидной заместительной терапии» за рубежом, МИД России и ФСКН России рекомендовано исходить из возможности разработки и принятия в международных организациях и международных форумах рекомендаций об использовании метода «опиоидной заместительной терапии» при лечении наркозависимых в государствах, которые выразили на это согласие и в которых имеются условия (социально-экономические, правовые, и иные) для эффективного применения такого метода, если эти решения не будут носить обязательного характера для других государств.
Крайне важным для реализации профилактических программ среди ПИН является принятие в 2003 г. Федерального закона «О внесении изменений и дополнений в Уголовный кодекс Российской Федерации». Особенно это касается примечания к статье 230 УК РФ, в котором говорится, что: «Действие настоящей статьи не распространяется на случаи пропаганды применения в целях профилактики ВИЧ-инфекции и других опасных заболеваний соответствующих инструментов и оборудования, используемых для потребления наркотических средств и психотропных веществ, если эти деяния осуществлялись по согласованию с органами исполнительной власти в области здравоохранения и органами по контролю за оборотом наркотических средств и психотропных веществ».
ФСКН России разработаны и направлены на согласование с федеральными органами исполнительной власти Методические рекомендации о порядке согласования действий по пропаганде применения соответствующих инструментов и оборудования, используемых для потребления наркотических средств и психотропных веществ. Отсутствие до сих пор соответствующего документа затрудняет работу по профилактике ВИЧ-инфекции среди наркопотребителей.
Учитывая тесную связь между наркопотреблением и распространением ВИЧ-инфекции в России, следует признать важную роль и влияние государственной политики в сфере контроля и противодействия незаконному обороту наркотических средств и психотропных веществ (далее - наркополитика) на эффективность и результативность усилий, предпринимаемых государством в борьбе с ВИЧ/СПИД.
Наркополитика является частью общей политики государства. Она разрабатывается органами законодательной и исполнительной власти Российской Федерации и ее субъектов и, по сути, должна представлять собой комплексную стратегию и тактику контроля наркотических средств и психотропных веществ - от регламентации легальной деятельности с ними до снижения спроса на наркотики и неблагоприятных социальных последствий их незаконного употребления.
Законодательной основой российской наркополитики является
Федеральный закон «О наркотических средствах и психотропных веществах» от 8 января 1998 г. Государственная политика, как следует из ч.1 ст.4 этого Закона, должна быть направлена на:
• установление строгого контроля за оборотом наркотических средств и психотропных веществ;
• сокращение числа больных наркоманией;
• сокращение правонарушений, связанных с незаконным оборотом наркотических средств.
Эти положения можно рассматривать как приоритеты национальной наркополитики, конкретизируемые в федеральных целевых программах. В тоже время одной из ключевых целей соответствующих федеральных целевых программ и нацпроекта в сфере здравоохранения должно быть значительное сокращение передачи ВИЧ-инфекции при инъекционном употреблении наркотиков и профилактика полового пути передачи ВИЧ от наркопотребителей к их сексуальным партнерам. В связи с этим необходимо повышение эффективности профилактических и лечебных мероприятий среди ПИН в сфере усиления мотивационной работы на изменение рискованного поведения в этой когорте людей.
ВИЧ инфекция также поражает заключенных в тюрьмах. Уровень распространенности ВИЧ-инфекции среди заключенных во многих странах значительно выше, чем среди населения в целом. Несмотря на то, что большинство заключенных, живущих с ВИЧ или СПИДом в тюрьме, инфицируются до того, как попали в заключение, риск инфицирования в тюрьме, особенно через использование нестерильного инъекционного инструментария и незащищенный секс, очень высок.
Профилактика передачи ВИЧ от матери к ребенку (ПМР)
Вертикальная передача ВИЧ-инфекции – означает передачу ВИЧ от ВИЧ-инфицированной женщины ее ребенку во время беременности, родов или при грудном вскармливании. По данным ряда авторов, при отсутствии профилактических мероприятий риск передачи ВИЧ от матери к ребенку соответствует 15-25% в развитых странах, и 25-45% - в развивающихся странах.
Профилактика вертикального пути передачи ВИЧ-инфекции (ППМР) - это комплекс мер для профилактики передачи ВИЧ от инфицированной женщины плоду или ребенку во время беременности, родов или при грудном вскармливании. Основные методы ППМР: проведение химиопрофилактики антиретровирусными препаратами (АРВ-профилактика) во время беременности, в родах и ребенку после рождения; плановое кесарево сечение; ограничение инвазивных процедур во время беременности и родов, вскармливание ребенку искусственными смесями. При правильном соблюдении всех указанных мероприятий риск передачи ВИЧ от матери к ребенку составляет менее 2%.
Медицинская помощь беременной в амбулаторно-поликлинических учреждениях.
В амбулаторно-поликлинических учреждениях службы охраны материнства и детства проводится дотестовое консультирование беременных женщин о ВИЧ-инфекции. При добровольном и информированном согласии на проведение ВИЧ теста, проводится забор крови для определения и подтверждения ВИЧ-статуса. При положительном результате теста проводится послетестовое консультирование с разъяснением результатов теста. Если результат теста отрицательный, женщине напоминаются меры по профилактике ВИЧ-инфекции и определятся дата повторного тестирования на ВИЧ в последнем триместре беременности.
Дальнейшее наблюдение и ведение ВИЧ-инфицированной беременной осуществляется совместно в учреждениях службы охраны материнства и детства и Центрах по профилактике и борьбе ВИЧ/СПИД. Участвуют в оказании помощи ВИЧ-инфицированной беременной следующие специалисты: акушеры-гинекологи и/или акушерки территориального амбулаторно-поликлинического учреждения (женской консультации или фельдшерско-акушерского пункта), уполномоченные доверенные врачи территориального ЛПУ по вопросам лечения ВИЧ/СПИД, специалисты городского или областного Центра по профилактике и борьбе со СПИД. Согласно российскому законодательству беременная женщина имеет право выбора медицинского учреждения для наблюдения за беременностью.
Медицинское обследование беременной, включающее определение иммунного статуса, вирусной нагрузки и стадии заболевания ВИЧ, проводится в центре по профилактике и борьбе со СПИД. Специалистом центра определяются, назначаются и выдаются антиретровирусные препараты (АРВ), контролируется соблюдения приверженности к приему препаратов, возможные побочные эффекты. Ведение беременности и родов специалист центра обсуждает с наблюдающим женщину акушером-гинекологом. Определяется учреждение, где будут проводиться роды и метод родоразрешения, и дата плановой госпитализации, проводится консультирование о важности искусственного вскармливания для профилактики ППМР. На этом этапе к обсуждению привлекается акушер-гинеколог стационара, где будут проводиться роды.
Оказание медицинской помощи ВИЧ-инфицированной женщине в родах.
При поступлении в роддом женщины с подтвержденной информацией о положительном ВИЧ-статусе, проводится ее консультирование о проведении АРВ профилактики в родах и методе ведения родов.
Если роженица поступает в родильный дом или родильное отделение больницы без карты дородового наблюдения, или в карте отсутствуют сведения о ВИЧ статусе, после дотестового консультирования, ей предлагают пройти тестирование на ВИЧ, с использованием методики экспресс теста. После получения результатов тестирования роженица получает послетестовое консультирование. Если экспресс-тест показывает положительный результат на ВИЧ, ей предлагается начать АРВ профилактику. В данной ситуации акушер-гинеколог самостоятельно назначает АРВ профилактику, согласно принятому протоколу, выбирает метод и осуществляет ведение родов (консервативно или оперативно) при информированном согласии женщины.
Постановлением Правительства Российской Федерации от 30 июня 1998 г. № 681 утвержден Перечень наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю.
Метадон включен в Список I наркотических средств, оборот которых в Российской Федерации запрещен в соответствии с законодательством Российской Федерации и международными договорами Российской Федерации.
Бупренорфин находится в Списке II наркотических средств, оборот которых ограничен и в отношении которых устанавливаются меры контроля в соответствии с законодательством Российской Федерации и международными договорами Российской Федерации. В соответствии с пунктом 6 ст. 31 Федерального закона от 8 января 1998 года № 3-ФЗ « О наркотических средствах и психотропных веществах» запрещается лечение наркомании наркотическими средствами и наркотическими веществами, внесенными в Список II указанного Перечня.
Протоколом заседания Правительственной комиссии Российской Федерации по противодействию злоупотреблению наркотиками и их незаконному обороту от 26.12.2003 года № 4, с учетом тенденции к расширению географии применения «опиоидной заместительной терапии» за рубежом, МИД России и ФСКН России рекомендовано исходить из возможности разработки и принятия в международных организациях и международных форумах рекомендаций об использовании метода «опиоидной заместительной терапии» при лечении наркозависимых в государствах, которые выразили на это согласие и в которых имеются условия (социально-экономические, правовые, и иные) для эффективного применения такого метода, если эти решения не будут носить обязательного характера для других государств.
Крайне важным для реализации профилактических программ среди ПИН является принятие в 2003 г. Федерального закона «О внесении изменений и дополнений в Уголовный кодекс Российской Федерации». Особенно это касается примечания к статье 230 УК РФ, в котором говорится, что: «Действие настоящей статьи не распространяется на случаи пропаганды применения в целях профилактики ВИЧ-инфекции и других опасных заболеваний соответствующих инструментов и оборудования, используемых для потребления наркотических средств и психотропных веществ, если эти деяния осуществлялись по согласованию с органами исполнительной власти в области здравоохранения и органами по контролю за оборотом наркотических средств и психотропных веществ».
ФСКН России разработаны и направлены на согласование с федеральными органами исполнительной власти Методические рекомендации о порядке согласования действий по пропаганде применения соответствующих инструментов и оборудования, используемых для потребления наркотических средств и психотропных веществ. Отсутствие до сих пор соответствующего документа затрудняет работу по профилактике ВИЧ-инфекции среди наркопотребителей.
Учитывая тесную связь между наркопотреблением и распространением ВИЧ-инфекции в России, следует признать важную роль и влияние государственной политики в сфере контроля и противодействия незаконному обороту наркотических средств и психотропных веществ (далее - наркополитика) на эффективность и результативность усилий, предпринимаемых государством в борьбе с ВИЧ/СПИД.
Наркополитика является частью общей политики государства. Она разрабатывается органами законодательной и исполнительной власти Российской Федерации и ее субъектов и, по сути, должна представлять собой комплексную стратегию и тактику контроля наркотических средств и психотропных веществ - от регламентации легальной деятельности с ними до снижения спроса на наркотики и неблагоприятных социальных последствий их незаконного употребления.
Законодательной основой российской наркополитики является
Федеральный закон «О наркотических средствах и психотропных веществах» от 8 января 1998 г. Государственная политика, как следует из ч.1 ст.4 этого Закона, должна быть направлена на:
• установление строгого контроля за оборотом наркотических средств и психотропных веществ;
• сокращение числа больных наркоманией;
• сокращение правонарушений, связанных с незаконным оборотом наркотических средств.
Эти положения можно рассматривать как приоритеты национальной наркополитики, конкретизируемые в федеральных целевых программах. В тоже время одной из ключевых целей соответствующих федеральных целевых программ и нацпроекта в сфере здравоохранения должно быть значительное сокращение передачи ВИЧ-инфекции при инъекционном употреблении наркотиков и профилактика полового пути передачи ВИЧ от наркопотребителей к их сексуальным партнерам. В связи с этим необходимо повышение эффективности профилактических и лечебных мероприятий среди ПИН в сфере усиления мотивационной работы на изменение рискованного поведения в этой когорте людей.
ВИЧ инфекция также поражает заключенных в тюрьмах. Уровень распространенности ВИЧ-инфекции среди заключенных во многих странах значительно выше, чем среди населения в целом. Несмотря на то, что большинство заключенных, живущих с ВИЧ или СПИДом в тюрьме, инфицируются до того, как попали в заключение, риск инфицирования в тюрьме, особенно через использование нестерильного инъекционного инструментария и незащищенный секс, очень высок.
Профилактика передачи ВИЧ от матери к ребенку (ПМР)
Вертикальная передача ВИЧ-инфекции – означает передачу ВИЧ от ВИЧ-инфицированной женщины ее ребенку во время беременности, родов или при грудном вскармливании. По данным ряда авторов, при отсутствии профилактических мероприятий риск передачи ВИЧ от матери к ребенку соответствует 15-25% в развитых странах, и 25-45% - в развивающихся странах.
Профилактика вертикального пути передачи ВИЧ-инфекции (ППМР) - это комплекс мер для профилактики передачи ВИЧ от инфицированной женщины плоду или ребенку во время беременности, родов или при грудном вскармливании. Основные методы ППМР: проведение химиопрофилактики антиретровирусными препаратами (АРВ-профилактика) во время беременности, в родах и ребенку после рождения; плановое кесарево сечение; ограничение инвазивных процедур во время беременности и родов, вскармливание ребенку искусственными смесями. При правильном соблюдении всех указанных мероприятий риск передачи ВИЧ от матери к ребенку составляет менее 2%.
Медицинская помощь беременной в амбулаторно-поликлинических учреждениях.
В амбулаторно-поликлинических учреждениях службы охраны материнства и детства проводится дотестовое консультирование беременных женщин о ВИЧ-инфекции. При добровольном и информированном согласии на проведение ВИЧ теста, проводится забор крови для определения и подтверждения ВИЧ-статуса. При положительном результате теста проводится послетестовое консультирование с разъяснением результатов теста. Если результат теста отрицательный, женщине напоминаются меры по профилактике ВИЧ-инфекции и определятся дата повторного тестирования на ВИЧ в последнем триместре беременности.
Дальнейшее наблюдение и ведение ВИЧ-инфицированной беременной осуществляется совместно в учреждениях службы охраны материнства и детства и Центрах по профилактике и борьбе ВИЧ/СПИД. Участвуют в оказании помощи ВИЧ-инфицированной беременной следующие специалисты: акушеры-гинекологи и/или акушерки территориального амбулаторно-поликлинического учреждения (женской консультации или фельдшерско-акушерского пункта), уполномоченные доверенные врачи территориального ЛПУ по вопросам лечения ВИЧ/СПИД, специалисты городского или областного Центра по профилактике и борьбе со СПИД. Согласно российскому законодательству беременная женщина имеет право выбора медицинского учреждения для наблюдения за беременностью.
Медицинское обследование беременной, включающее определение иммунного статуса, вирусной нагрузки и стадии заболевания ВИЧ, проводится в центре по профилактике и борьбе со СПИД. Специалистом центра определяются, назначаются и выдаются антиретровирусные препараты (АРВ), контролируется соблюдения приверженности к приему препаратов, возможные побочные эффекты. Ведение беременности и родов специалист центра обсуждает с наблюдающим женщину акушером-гинекологом. Определяется учреждение, где будут проводиться роды и метод родоразрешения, и дата плановой госпитализации, проводится консультирование о важности искусственного вскармливания для профилактики ППМР. На этом этапе к обсуждению привлекается акушер-гинеколог стационара, где будут проводиться роды.
Оказание медицинской помощи ВИЧ-инфицированной женщине в родах.
При поступлении в роддом женщины с подтвержденной информацией о положительном ВИЧ-статусе, проводится ее консультирование о проведении АРВ профилактики в родах и методе ведения родов.
Если роженица поступает в родильный дом или родильное отделение больницы без карты дородового наблюдения, или в карте отсутствуют сведения о ВИЧ статусе, после дотестового консультирования, ей предлагают пройти тестирование на ВИЧ, с использованием методики экспресс теста. После получения результатов тестирования роженица получает послетестовое консультирование. Если экспресс-тест показывает положительный результат на ВИЧ, ей предлагается начать АРВ профилактику. В данной ситуации акушер-гинеколог самостоятельно назначает АРВ профилактику, согласно принятому протоколу, выбирает метод и осуществляет ведение родов (консервативно или оперативно) при информированном согласии женщины.
В зависимости от состояния здоровья и принимаемых медикаментов, беременная ВИЧ-инфицированная женщина может выбрать либо кесарево сечение, либо обычные роды через естественные родовые пути.
Обсудить эти возможности и сделать выбор ей обязательно нужно в беседе с врачом во время беременности.
Очень важно как можно раньше с наступлением беременности обсудить с врачом варианты родов для того, чтобы врач мог помочь выбрать наиболее подходящий вариант. Чтобы максимально надёжно предотвратить передачу вируса, кесарево сечение нужно сделать на 38 неделе беременности до момента разрыва плодных оболочек и излития околоплодных вод.
Роды через естественные родовые пути рекомендуются также в том случае, если у матери повреждены плодные оболочки или процесс родов идёт слишком быстро.
Любые роды представляют собой определённый риск. Риск передачи вируса от матери к ребёнку выше при родах через естественные родовые пути, чем при запланированном кесаревом сечении.
Оказание медицинской помощи новорожденному после рождения.
Ребенку, рожденному от ВИЧ-инфицированной женщины, назначается АРВ профилактика согласно принятому протоколу. После рождения ребенок не прикладывается к груди. Женщина консультируется о необходимости искусственного вскармливания.
Послеродовая помощь ВИЧ инфицированной женщине
В послеродовом отделении или палате совместного пребывания женщине оказывается необходимая медицинская помощь после родов. Она консультируется о методах прекращения лактации, при ее согласии назначаются соответствующие лекарственные средства. Женщина консультируется о методах планирования семьи. Определяется и назначается наиболее предпочтительный метод контрацепции. Женщине оказывается психологическая помощь. Необходимо обеспечить женщине возможность получения консультации социального работника, а также всех других необходимых специалистов.
Женщина и ребенок выписываются из роддома или, по необходимости, переводятся для наблюдения и лечения в другие медицинские учреждения. В дальнейшем ребенок и женщина наблюдаются по месту жительства в детской поликлинике/женской консультации и в Центре по профилактике и борьбе со СПИД. Составляется план наблюдения, и определяются конкретные учреждения, где будет проводиться дальнейшее наблюдение женщины и ребенка.
На всех этапах медицинская помощь ВИЧ-инфицированной женщине оказывается со строгим соблюдением принципов этики и конфиденциальности.
Контроль переливаемой крови и ее препаратов
Карантинизация – гарантия инфекционной безопасности плазмы крови и ее компонентов.
Компоненты крови, применяемые для переливания в клиниках, а также используемые для производства препаратов, сохраняют опасность заражения больных вирусами инфекционных заболеваний. Это связано с тем, что скрытый период вирусоносительства невозможно определить даже современными методами исследования крови доноров.
С целью обеспечения вирусной безопасности гемокомпонентов, в существует метод карантинизации свежезамороженной плазмы.
Метод карантинизации заключается в хранении плазмы при температуре – 30 – 400С с запретом использования ее на протяжении 6 месяцев до повторного обследования крови донора на отсутствие инфекций (ВИЧ, вирусные гепатиты В и С).
Метод карантинизации плазмы является действенным и надежным способом борьбы с распространением ВИЧ-инфекци и парентеральных гепатитов.
Эффективность проведения карантинизации зависит от возврата доноров через 6 месяцев после дачи плазмы для повторного обследования на маркеры инфекционных заболеваний. Только после подтверждения вирусной безопасности, плазма может быть выдана в учреждения здравоохранения.
Повторное обследование позволит донорам проконтролировать состояние своего здоровья и убедиться в том, что они были здоровы во время донации плазмы.
Всех доноров, сдающим кровь для переливания, необходимо проинформировать, что в случае их неявки для повторного обследования - плазма не может быть использована с лечебной целью.
Профилактика ВИЧ-инфекции у медицинского персонала.
Для профилактики профессионального инфицирования ВИЧ медицинских работников необходимо соблюдение следующих нормативных правил:
• при выполнении любых манипуляций медицинского характера сотрудник ЛПУ должен быть одет в халат, шапочку, одноразовую маску (а при необходимости - очки или защитные щитки), сменную обувь, выходить в которых за пределы отделения, лабораторий, манипуляционных кабинетов и др. запрещается;
• все манипуляции, при которых может произойти загрязнение рук кровью, сывороткой крови или другими биологическими жидкостями, проводить в двойных резиновых медицинских перчатках. Резиновые перчатки, снятые единожды, повторно не используют из-за возможности загрязнения рук. В процессе работы перчатки обрабатывают 70% спиртом или любыми другими дезинфицирующими препаратами, обладающими вирулицидным действием;
• работники всех медицинских специальностей должны соблюдать меры предосторожности при выполнении манипуляций с режущими и колющими инструментами (иглы, скальпели, боры, сепарационные диски и камни для препаровки зубов и пр.); следует избегать уколов, порезов перчаток и рук;
• при повреждении кожных покровов необходимо немедленно обработать перчатки дезинфицирующим раствором и снять их, выдавить кровь из ранки; затем под проточной водой тщательно вымыть руки с мылом, обработать их 70% спиртом и смазать ранку 5% раствором йода. При загрязнении рук кровью следует немедленно обработать их в течение не менее 30 сек. тампоном, смоченным кожным антисептиком, разрешенным к применению (70% спирт, 5% раствор хлорамина, йодонат, стериллиум, октенидерм, октенисепт, хлоргексидин и др.), вымыть их двукратно теплой проточной водой с мылом и насухо вытереть индивидуальным полотенцем (салфеткой);
• при попадании крови или других биологических жидкостей на: слизистые глаз их следует сразу же промыть водой или 1% раствором борной кислоты; слизистую носа — обработать 3% раствором протаргола; слизистую рта - прополоскать 70% раствором спирта или 0,005% раствором марганцевого кислого калия или 1 % раствором борной кислоты;
• при наличии ран на руках, экссудативных поражений кожи или мокнущего дерматита, медработник на время заболевания отстраняется от ухода за пациентами и контакта с предметами для ухода за ним. При необходимости выполнения работы все поврежденные участки должны быть закрыты напальчниками, лейкопластырем и др.;
• поверхности рабочих столов в конце рабочего дня (а в случае загрязнения кровью — немедленно) обрабатывают дезинфицирующими средствами, обладающими вирулицидными свойствами. Если поверхность загрязнена кровью или сывороткой крови, процедуры выполняют дважды: немедленно и с интервалом в 15 минут;
• при попадании инфицированного материала на пол, стены, мебель, оборудование загрязненные места заливают дезинфицирующим раствором, затем протирают ветошью, смоченной в дезинфицирующем растворе. Использованную ветошь сбрасывают в емкость с дезинфицирующим раствором или в бак для последующего автоклавирозания;
• употреблять пищу, курить и пользоваться косметикой разрешается только в специально отведенных для этих целей изолированных помещениях.
Все рабочие места (например, в стоматологическом кабинете) должны быть обеспечены дезинфицирующим раствором и аптечкой первой помощи. Для избегания инфицирования медицинского работника и предотвращения заражения пациентов во время стоматологических манипуляций необходимо соблюдать:
• тщательное мытье рук после осмотра каждого больного или каждой процедуры, где приходилось иметь дело с инфицированным материалом;
• после процедур высокой степени риска (парентеральные процедуры и те, при которых происходит контакт с сильно изъязвленными слизистыми оболочками и кожей) необходимо тщательно вымыть руки, применяя хирургические очищающие растворы. При его отсутствии — мытье рук водой с мылом, высушивание и обработка 70 % этиловым спиртом;
• после процедур со средней и низкой степенью риска (контакт с неповрежденными слизистыми оболочками и кожей) достаточно обычного мыла и воды;
• перед работой необходимо надевать защитные очки или пластиковые щиты, защитную маску для лица;
• одноразовые перчатки обязательны;
• врачи с экссудативными поражениями кожи не должны выполнять инвазивных процедур;
• при подозрении на ВИЧ-инфекцию у пациента врач-стоматолог должен надеть хирургический халат и шапочку, закрывающие волосы;
• при выполнении внутриротовых рентгеновских снимков необходимо соблюдать такие же меры предосторожности;
• особые меры предосторожности соблюдают при обращении с острыми инструментами (скальпель, одноразовые иглы, боры, диски, эндодонтический инструментарий);
• использовать одноразовые инструменты только один раз;
• прополаскивание рта пациентом перед процедурой значительно снижает количество микроорганизмов в аэрозолях, рассеиваемых во время процедур; полоскание только одной водой сокращает количество микроорганизмов в аэрозолях на 75%, а применение специальных полосканий для полости рта — на 98%;
• медицинский работник должен относиться к крови и к другим биологическим жидкостям организма как к потенциально заразному материалу.
Права и обязанности ВИЧ-инфицированных
В Российской Федерации создана законодательная и нормативная база в сфере борьбы с ВИЧ-инфекцией, основой которой является принятый в 1995 г. Федеральный закон «О предупреждении распространения в Российской Федерации заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции)». Данный закон определил общие принципы государственной политики в области борьбы с этой инфекцией, государственные гарантии доступности диагностики, лечения и профилактики, а также меры социальной защиты ВИЧ-инфицированных и их семей.
В соответствии с этим законом и принятым в развитие его приказом Минздравсоцразвития России от 30.10.1995 г., установлено обязательное диагностическое обследование на ВИЧ-инфекцию доноров крови, плазмы крови и других биологических жидкостей, тканей и органов. Обязательному медицинскому освидетельствованию на ВИЧ-инфекцию подлежат работники отдельных профессий, производств, предприятий и учреждений, перечень которых утверждается Правительством Российской Федерации, при проведении обязательных предварительных при поступлении на работу и периодических медицинских осмотров, а также предусмотрено добровольное обследование с проведением до и после тестового консультирования по клиническим и эпидемическим показаниям.
В 2005-м году Российское государство кардинально изменило свое отношение к проблеме ВИЧ/СПИДа. Был разработан перечень программ по профилактике, выявлению и лечению ВИЧ на 2006 г. Все эти программы были включены в национальный проект "Здоровье". Было принято беспрецедентное решение о двадцатикратном превышении финансирования, выделявшееся на эти задачи до этого момента.
Разработанные заинтересованными федеральными органами исполнительной власти, органами исполнительной власти субъектов Российской Федерации с участием общественных организаций и с учетом опыта мирового сообщества профилактические программыпо противодействию дальнейшего распространения ВИЧ-инфекции базируются на следующей стратегии и тактики:
• осуществление комплекса организационных, профилактических и противоэпидемических мероприятий, направленных на предупреждение распространения инфекции среди всех слоев населения с обращением особого внимания на наиболее уязвимые его группы;
• достижение максимально низкого уровня распространения ВИЧ-инфекции среди населения и продление жизни ВИЧ инфицированных до средней продолжительности;
• минимизация социальных, экономических и политических последствий эпидемии ВИЧ/СПИД.
В целях осуществления эффективного взаимодействия между государственными, общественными и международными организациями, участвующими в борьбе с ВИЧ/СПИД в Российской Федерации, при Минздравсоцразвития России создан Координационный Совет по проблемам ВИЧ/СПИД. Совет включает в себя представителей 9 министерств, руководителей центров по профилактике и борьбе со СПИД субъектов Федерации, представителей учреждений науки, общественных и неправительственных организаций, работающих в области борьбы с этой инфекцией. Задачами его являются проведение экспертной оценки проектов, развитие и распространение наиболее эффективных технологий по противодействию эпидемии ВИЧ-инфекции в стране.
Заинтересованными федеральными органами исполнительной власти издан ряд организационно-распорядительных и методических документов по различным аспектам борьбы с ВИЧ/СПИД. Главным государственным санитарным врачом Российской Федерации в 2004 и 2005 гг. приняты постановления «Об активизации мероприятий, направленных на предупреждение распространения ВИЧ-инфекции в Российской Федерации». В стране налажена эффективная система эпидемиологического надзора за ВИЧ-инфекцией. В отличие от большинства стран, осуществляется исчерпывающая регистрация всех случаев инфицирования ВИЧ и заболевания СПИДом.
Создана сеть учреждений, включающая в себя Федеральный научно-методический центр по профилактике и борьбе со СПИД, Российский научно-практический центр оказания помощи беременным и детям, рожденным ВИЧ-инфицированными матерями, 6 окружных центров в составе НИИ эпидемиологического профиля, 102 территориальных центра, подчиненных органам управления здравоохранением субъектов Российской Федерации, 1200 специализированных диагностических лабораторий.
Реализация многих организационных и профилактических мероприятий стала возможной в связи с принятием Правительством Российской Федерации в 1993 и 1996 гг. Федеральных целевых программ «Анти-ВИЧ/СПИД» на 1993-1995 гг., 1996-2000 гг. и на период до 2011 г.
В настоящее время в стране реализуется подпрограмма « Неотложные меры по предупреждению распространения в Российской Федерации заболевания, вызываемого вирусом иммунодефицита человека («Анти-ВИЧ/СПИД») в рамках Федеральной целевой программы «Предупреждение и борьба с заболеваниями социального характера (2007-2012 гг.)», подпрограммы: «Вирусные гепатиты», «ВИЧ-инфекция» реализация ведомственных целевых программ «Профилактика инфекционных и паразитарных заболеваний» («Стоп-инфекция»). «Совершенствование профилактики, усиление мер по предупреждению и распространению ВИЧ-инфекции и СПИДа в Российской Федерации» («СПИДу нет»).
Федеральными органами исполнительной власти, в рамках реализации указанной подпрограммы, осуществлялись организационные и практические мероприятия, направленные на предупреждение распространения этой инфекции.
Меры по противодействию распространению ВИЧ-инфекции включены также в новый проект Концепции демографического развития РФ до 2025 года, разработанной по поручению Президента РФ и представленной в 2007 году. Министерством образования и науки Российской Федерации, совместно с Роспотребнадзором, разработана и направлена в органы управления образованием, органы по делам молодежи, органы управления здравоохранением субъектов Российской федерации «Концепция превентивного обучения в области профилактики ВИЧ/СПИД в образовательной среде». Разработаны соответствующие программы и методические пособия для специалистов образовательных учреждений, учащихся и родителей.
Совместно с ФСКН России и МВД России разработаны рекомендации об организации работы по предупреждению и пресечению правонарушений, связанных с незаконным оборотом наркотиков в образовательных учреждениях.
Федеральной службой исполнения наказаний осуществляется тестирование подследственных и осужденных на ВИЧ-инфекцию, до- и послетестовое консультирование. Внедрена информационная обучающая программа для осужденных по вопросам профилактики этой инфекции, информирование немедицинского персонала учреждений исполнения наказаний по вопросам безопасности и снижения риска ВИЧ-инфицирования.
Указанные мероприятия проводятся в сотрудничестве с 40 общественными и международными неправительственными и религиозными организациями. Налажено тесное взаимодействие в этой работе с Русской Православной Церковью, которая в лице своих приходов, монастырей, церковно-общественных организаций, осуществляет в различных регионах многочисленные проекты первичной профилактики ВИЧ среди детей и молодежи, направленные на формирование нравственной ценностной основы, воспитание резистентности к негативным явлениям (в частности, наркотикам, алкоголю, гомосексуализму, добрачным половым связям) как моделям рискованного поведения, которые могут привести к заражению ВИЧ. Церковь оказывает духовную и психологическую поддержку людям, живущим с ВИЧ, их близким, организуя «телефоны доверия», службы очного консультирования, специальные богослужения об их здравии, патронаж над нуждающимися в уходе и пр.
Учитывая серьезность проблемы и невозможность разрешить ее отдельным странам самостоятельно, в 1996 г. была создана Объединенная программа ООН по СПИДу ЮНЭЙДС (UNAIDS). Соучредителями ЮНЭЙДС на сегодняшний день являются ВОЗ, ЮНИСЕФ, ЮНЕСКО, ЮНФПА, (Фонд ООН по народонаселению), ПРООН (Программа ООН по развитию), УНП ООН (Управление по наркотикам и преступности ООН), УВКБ ООН (Управление Верховного комиссара по Беженцам ООН), ВПП (Всемирная продовольственная программа), МОТ (Международная организация труда) и Всемирный банк.
В соответствии с решением совещания руководителей стран «Большой восьмерки» в Генуе в январе 2002 г. создан «Глобальный Фонд по борьбе со СПИДом, туберкулезом и малярией». Следует отметить, что в Российской Федерации реализуется ряд программ и проектов по профилактике ВИЧ/СПИД среди населения в целом и, в особенности, среди групп риска с участием, как государственных органов, так и при поддержке отечественных и международных организаций и фондов.
В решении проблем, связанных с ВИЧ/СПИДом, в последние годы все активнее стала принимать участие Русская Православная Церковь. В сентябре 2005 года состоялась презентация одобренной Священным Синодом «Концепции участия Русской Православной Церкви в борьбе с распространением ВИЧ/СПИДа и работе с людьми, живущими с ВИЧ/СПИДом». В концепции отражены богословские и этические аспекты болезни, задачи по организации церковной работы и вопросы сотрудничества с государством и обществом в деле нравственного воспитания подрастающего поколения и оказании помощи людям, живущим с ВИЧ/СПИДом.
С точки зрения Русской Православной Церкви, подлинной первопричиной и источником стремительного распространения эпидемии является утрата обществом фундаментальных духовных ценностей, нравственных устоев и ориентиров. Все эти разрушительные процессы свидетельствуют о тяжких духовно-нравственных недугах, поразивших общество, которые, в случае их последовательного развития, могут привести к национальной катастрофе.
В России действует Федеральный закон «О предупреждении распространения в Российской Федерации заболевания, вызванного вирусом иммунодефицита человека (ВИЧ-инфекция)» от 1995 года. В нем указаны права, гарантии и обязанности заинтересованных лиц. Государство ВИЧ-инфицированным гарантирует: доступность медицинского освидетельствования для выявления ВИЧ-инфекции, в том числе и анонимно; бесплатное предоставление всех видов квалифицированной и специализированной медицинской помощи. Государство гарантирует регулярное информирование населения, в том числе через средства массовой информации, о доступных методах профилактики ВИЧ-инфекции. Гарантируется соблюдение всех прав и свобод для ВИЧ-инфицированных без ограничения перемещения их по стране, приема на учебу и работу.
Очерчен круг обязанностей ВИЧ-инфицированного. Статья 13 этого закона предусматривает уголовную ответственность за заражение ВИЧ-инфекцией.
Во многих странах мира, в т.ч. и в нашей, отмечается дискриминация лиц, инфицированных ВИЧ. ООН считает это недопустимым. Дискриминация ВИЧ-инфицированных является прямым нарушением прав человека. Каждый инфицированный ВИЧ имеет те же гражданские права, что и неинфицированный.
Инфицирование ВИЧ не может служить поводом для отстранения от работы, за исключением тех случаев, когда инфицированный человек в силу характера своей работы может инфицировать большое количество других людей. Так, медики, особенно хирурги, гинекологи, акушеры и стоматологи должны регулярно (не реже 1 раза в год) проходить обследова-ние на ВИЧ-инфицирование. При положительных результатах анализов они должны отстраняться от работы.
Помимо общегражданских прав, инфицированные ВИЧ имеют право на заботу и поддержку. В развитых странах мира больные СПИДом имеют право на бесплатную или льготную медицинскую помощь.
| 10 фактов о ВИЧ/СПИДЕ (ВОЗ) 1. ВИЧ (вирус иммунодефицита человека) инфицирует клетки иммунной системы. Инфекция приводит к прогрессирующему истощению иммунной системы, разрушая способность организма давать отпор инфекциям и болезням. СПИД (синдром приобретенного иммунодефицита) относится к самым поздним стадиям ВИЧ-инфекции, на которых появляются какие-либо из более чем 20 оппортунистических инфекций или характерных для этой болезни раковых заболеваний. 2. Есть несколько путей передачи ВИЧ. ВИЧ может передаваться следующими путями: • незащищенный секс (вагинальный или анальный) или оральный секс с инфицированным человеком; • переливание зараженной крови; • использование зараженных игл, шприцев или других острых инструментов; • передача от матери ребенку во время беременности, родов и грудного вскармливания. 3. В мире живет 34 миллиона человек с ВИЧ/СПИДом. Подавляющее большинство из них живет в странах с низким и средним уровнем дохода. По оценкам, в 2010 году ВИЧ-инфекцию приобрели 2,7 миллиона человек. 4. ВИЧ/СПИД является основной инфекционной причиной смерти в мире. На сегодняшний день эта болезнь унесла жизни более чем 30 миллионов человек. По оценкам, ежегодно от ВИЧ/СПИДа умирает 1,8 миллиона человек. 5. Комбинированная антиретровирусная терапия (АРТ) предотвращает репликацию ВИЧ в организме. При прекращении репродукции вируса иммунные клетки организма способны жить в течение более длительного времени, обеспечивая защиту организма от инфекций. 6. В конце 2010 г. около 6,65 миллиона ВИЧ-позитивных людей в странах с низким и средним уровнем дохода имели доступ к АРТ. Это означает 16-кратное расширение доступа с 2003 года. В целом, охват АРТ в странах с низким и средним уровнем дохода продолжал расширяться и к концу 2010 года достиг 47% из 14,2 миллиона людей, соответствующих критериям для лечения. 7. По оценкам, 3,4 миллиона детей имеют ВИЧ/СПИД. По данным за 2010 г., большинство из этих детей живет в Африке к югу от Сахары, и были инфицированы своими ВИЧ-позитивными матерями во время беременности, родов или грудного вскармливания. Ежедневно около 1100 детей приобретают ВИЧ-инфекцию. Число детей, получающих АРТ, возросло с 75 000 в 2005 году до 456 000 в 2010 г. 8. Передача инфекции от матери ребенку почти полностью предотвратима. Однако в странах с низким и средним уровнем дохода доступ к профилактическим мероприятиям остается на низком уровне. Тем не менее, достигнут прогресс. В 2010 г. 48% беременных женщин с ВИЧ получали наиболее эффективные схемы лечения для предотвращения передачи вируса от матери ребенку. 9. ВИЧ является основным фактором риска развития активной формы туберкулеза. В 2010 году среди людей с ВИЧ произошло более 350 000 случаев смерти от туберкулеза. Это пятая часть из предположительно 1,9 миллиона случаев смерти от ВИЧ за этот год. Большинство людей с сочетанными ВИЧ и ТБ проживает в Африке к югу от Сахары (около 82% всех случаев в мире). 10. Есть несколько способов предотвращения передачи ВИЧ. Основные способы предотвращения передачи ВИЧ: - практика безопасного секса с использованием презервативов; - тестирование и лечение инфекций, передаваемых половым путем, включая ВИЧ; - воздержание от потребления инъекционных наркотиков или, в случае их потребления, использование всегда новых и одноразовых игл и шприцев; - обеспечение того, чтобы используемые кровь или продукты крови, были протестированы на ВИЧ. |
1. Как передается и как не передается ВИЧ?
2. Какие методы профилактики ВИЧ/СПИДа Вы знаете?
3. В чем особенности прав ВИЧ-инфицированных?
4. Какие меры защиты от ВИЧ-инфекции используются в повседневной работе медицинского персонала?
5.7. Профилактика туберкулеза
 Туберкулез - антропонозная бактериальная инфекционная болезнь с аспирационным механизмом передачи возбудителя. Характеризуется хроническим волнообразным течением с преимущественным поражением легких, интоксикацией и аллергизацией организма.
Туберкулез - антропонозная бактериальная инфекционная болезнь с аспирационным механизмом передачи возбудителя. Характеризуется хроническим волнообразным течением с преимущественным поражением легких, интоксикацией и аллергизацией организма.Возбудитель - различные виды микобактерий из семейства Mycobacteriaceae рода Mycobacterium, среди которых основное эти-ологическое значение имеют Mycobacterium tuberculosis (и, по-видимому, M.africanum), выделяемая от человека, на втором месте стоит М.bovis (бычий тип), выделяемая от крупного рогатого скота и других домашних животных, и лишь единичные случаи заболевания людей обусловлены М.avium (птичий тип). Последний тип отнесен к III группе атипичных микобактерий.
Микобактерии - неподвижные грамположительные кислото-, спирто- и щелочеустойчивые палочки.
Туберкулезные микобактерий обладают устойчивостью к физическим и химическим агентам; во влажной мокроте выдерживают нагревание до +75°С в течение 30 мин, при кипячении погибают через 5 мин; в высушенной мокроте при +100°С погибают через 45 мин; в условиях комнатной температуры (темном месте) остаются жизнеспособными в течение 4 мес, при рассеянном свете - до 1,5 мес; под действием прямых солнечных лучей погибают через несколько часов; чувствительны к хлорсодержащим дезинфицирующим растворам. Важное эпидемиологическое значение имеет способность микобактерий сохраняться в молоке и масле до 10 мес, в мягком сыре - до 19 мес, в твердом - более 8 мес, в замороженном мясе – до 1 года.
Резервуар и источники возбудителя. Основным источником возбудителя является человек, больной легочной формой туберкулеза и выделяющий микобактерий из дыхательных путей. Больные животные (крупный рогатый скот, свиньи и др.) и птицы, а также больные люди, выделяющие микобактерий с мочой и калом, имеют второстепенное эпидемиологическое значение.
Период заразительности источника равен всему периоду заболевания, способного длиться годами и даже десятилетиями. Интенсивность выделения микобактерий больным человеком увеличивается в период клинических обострений (чаще весной и осенью), животными - в период лактации.
Механизм передачи возбудителя. Наибольшую эпидемиологическую значимость имеет аспирационный механизм с воздушно-капельным (факторы передачи - частички мокроты и носоглоточной слизи, выделяющиеся в воздух при кашле, чиханье, разговоре и др.) и воздушно-пылевым (факторы передачи - контаминированная микобактериями взвешенная в воздухе пыль) путями передачи. Заражение от животных и птиц обычно происходит пищевым путем, когда факторами передачи служат молоко и молочные продукты, мясо, яйца. Возможна передача возбудителя через различные предметы бытовой обстановки и обихода.
Естественная восприимчивость людей высокая. Наиболее под-вержены заболеванию дети в возрасте до 3 лет. Заболеванию способствуют различные виды иммунодефицита, в частности ВИЧ-инфекция.
Основные эпидемиологические и клинические признаки.
Болезнь распространена повсеместно. Условиями, благоприятствующими распространению туберкулеза, являются низкий социально-экономический уровень жизни, скученность в быту и на производстве, низкий уровень санитарной культуры, недостаточность доступной и квалифицированной медицинской помощи. Вместе с тем в конце 90-х годов наметился рост заболеваемости туберкулезом во многих экономически развитых странах.
Заболеваемость туберкулезом оценивают по четырем показателям:
• инфицированности (процент зараженных к числу обследуемых);
• собственно заболеваемости (число вновь выявлен¬ных больных в данном году на 100 тыс. населения);
• болезненности (число состоящих на учете на начало года больных активным туберкулезом на 100 тыс. населения);
• смертности (число умерших от туберкулеза в данном году на 100 тыс. населения).
Чаще болеют дети первых двух лет жизни, подростки и пожилые люди в возрасте 60 лет и старше. Выраженная сезонность отсутствует, но рецидивы и обострения обычно наблюдаются ранней весной. Мужчины болеют чаще, чем женщины. Заболеваемость зоонозным туберкулезом преобладает среди сельских жителей, у которых он нередко носит профессиональный характер (животноводы, птичницы и др.).
По данным ВОЗ, в мире ежегодно заболевают туберкулезом более 8 млн. человек, 95% из них – это жители развивающихся стран, и 3 млн. умирает от него. Треть населения мира (около 200 млн. человек) уже инфицировано микобактерией туберкулёза (МБТ). В последние годы наблюдается рост заболеваемости во всех возрастных группах, но особенно эта тенденция характерна для населения трудоспособного возраста 25 — 44 лет. Можно ожидать, что в ближайшие 10 лет от туберкулеза погибнет 30 млн. человек; между тем 12 млн. из них могли бы быть спасены при хорошей организации раннего выявления и лечения больных. Сложившуюся ситуацию ВОЗ характеризует как кризис глобальной политики в области туберкулеза.
Совсем недавно туберкулез рассматривали как исчезающую болезнь. Рассчитывали сроки его ликвидации на Земле, и в первую очередь — в экономически развитых странах. По заключению экспертов ВОЗ, задача ликвидации туберкулёза как существенной проблемы здравоохранения могла быть решена, если инфицированность микобактериями туберкулёза детей до 14 лет не будет превышать 1%, а риск инфицирования, т.е. число подвергшихся заражению микобактериями туберкулёза в течение года из числа неинфицированных – будет ниже 0,05%. В настоящее время выдвинут новый критерий ликвидации туберкулёза как распространенного заболевания – 0,1 случая бациллярного больного туберкулёзом на 1 млн. жителей (Хоменко А.Г).
Оценка реальной эпидемиологической ситуации в экономически высокоразвитых странах, в том числе в странах Центральной, Восточной Европы и бывшего СССР, дает возможность выделить следующие основные причины увеличения заболеваемости и смертности от туберкулеза:
• ухудшение жизненного уровня большой группы населения, в частности ухудшение питания с резким снижением потребления белковых продуктов; наличие стрессов в связи с неустойчивой политической ситуацией, военными столкновениями и войнами в ряде регионов;
• резкое увеличение миграции больших групп населения, практически выпадающих из поля зрения лечебно-профилактических учреждений и не охваченных оздоровительными мероприятиями в целом и противотуберкулезными в частности;
• сокращение масштабов противотуберкулезных мероприятий, особенно в части профилактики и раннего выявления туберкулеза у взрослого населения, в частности у социально-дезадаптированных групп и групп высокого риска;
• увеличение числа больных с тяжелыми формами заболевания, особенно вызванными лекарственно-устойчивыми микобактериями, что затрудняет проведение эффективного лечения, способствует развитию необратимых хронических форм, высокой летальности.
В сложившейся ситуации неотложной задачей является усиление и расширение противотуберкулезных мероприятий. Особое значение приобретает определение их приоритетности с учетом эффективности и способности повлиять на эпидемиологическую ситуацию, вернуть утраченные возможности «управления» туберкулезной инфекцией.
Туберкулез с множественной лекарственной устойчивостью
Стандартные противотуберкулезные лекарства используются на протяжении целого ряда десятилетий, и устойчивость к лекарствам растет. В каждой стране, где проводятся исследования, зарегистрированы штаммы, устойчивые к какому-либо одному противотуберкулезному препарату.
Туберкулез с множественной лекарственной устойчивостью (МЛУ-ТБ) – это форма ТБ, вызываемая бактерией, не реагирующей, по меньшей мере, на изониазид и рифампицин, два самых мощных противотуберкулезных препарата первой линии (или стандартных).
Основной причиной развития МЛУ-ТБ является ненадлежащее лечение. Ненадлежащее или неправильное использование противотуберкулезных препаратов или использование лекарств плохого качества может приводить к лекарственной устойчивости.
Болезнь, вызванная устойчивыми бактериями, не поддается обычному лечению препаратами первой линии. МЛУ-ТБ можно лечить и излечивать, используя препараты второй линии. Однако выбор препаратов второй линии ограничен, а рекомендуемые лекарства не всегда доступны. Требуемая экстенсивная химиотерапия (лечение длительностью до двух лет) дороже и может вызывать тяжелые побочные реакции у пациентов.
В некоторых случаях может развиваться более тяжелая лекарственная устойчивость. ТБ с широкой лекарственной устойчивостью (ШЛУ-ТБ) является формой туберкулеза с множественной лекарственной устойчивостью, реагирующей на еще более ограниченное число имеющихся препаратов, включая самые эффективные противотуберкулезные препараты второй линии.
В 2010 г. в мире произошло около 650 000 случаев МЛУ-ТБ. По оценкам, примерно в 9% из этих случаев был ШЛУ-ТБ. Ежегодно около 440 000 человек заболевают МЛУ-ТБ и 150 000 человек умирают от этой формы туберкулеза.
Противотуберкулезная помощь ВИЧ-инфицированным пациентам включает три раздела:
• осуществление скринингового обследования ВИЧ-инфициро-ванных пациентов на туберкулез и проведение профилактического лечения;
• проведение интенсивной фазы лечения туберкулеза, лечение оппортунистических инфекций у больных с сочетанной патологией;
• диспансеризация и амбулаторное лечение туберкулеза у ВИЧ-инфицированных пациентов.
Профилактические мероприятия включают общегосударственные и специальные медицинские. К первым относятся: улучшение жилищных условий, предоставление больным туберкулезом изолированных квартир, оздоровление условий труда, благоустройство населенных мест, озеленение городов и др. Вторые проводятся лечебно-профилактическими и санитарно-эпидемиологическими учреждениями под руководством и при участии специализированных противотуберкулезных НИИ (диспансеров) и включают раннее выявление и лечение больных с начальными формами туберкулеза.
Рекомендации Международного союза борьбы с туберкулезом и болезнями легких и ВОЗ в качестве основного направления противотуберкулезной работы называют выявление бациллярных больных, у которых микобактерии обнаруживаются в мокроте методом микроскопии, и их химиотерапию. Эффективное лечение позволяет предотвратить смерть таких больных при прогрессирующем течении заболевания, что ведет к уменьшению смертности; прекратить распространение туберкулезной инфекции; предупредить развитие хронического туберкулезного процесса с постоянным выделением микобактерий, часто обладающих лекарственной устойчивостью, и, наконец, добиться излечения больного.
Выявление бациллярных больных рекомендуется осуществлять среди лиц, обратившихся за медицинской помощью в связи с бронхолегочными симптомами: кашлем с выделением мокроты, одышкой, кровохарканьем, а также с синдромом интоксикации с повышением температуры тела, снижением массы тела. В нашей стране принято одновременно с исследованием мокроты проводить в противотуберкулезных диспансерах рентгенофлюорографическое исследование.
Массовые обследования методом флюорографии проводятся в городах ежегодно, в сельской местности - каждые два года. Детям, начиная с 3-месячного возраста, ставят аллергическую пробу с туберкулином (проба Манту); при отрицательной реакции пробу повторяют 2 раза в год; в возрасте до 4 лет - одни раз в год, а в дальнейшем - до появления положительной реакции. Рентгенологическому исследованию подлежат лица, часто и длительно болеющие гриппом, пневмониями, острыми респираторными заболеваниями, бронхитами, лица с неустановленным диагнозом. Обследованию на туберкулез подвергаются беременные.
Обязательно обследование (1-2 раза в год) работников детских учреждений (детские ясли, детские сады, ясли-сады, дома ребенка, детские дома, школы-интернаты, лесные школы, детские оздоровительные учреждения), детских лечебно-профилактических и санаторно-курортных учреждений (детские больницы, детские санатории, родильные дома), связанных с обслуживанием и питанием детей; педагогов и воспитателей школ, учебно-воспитательньж учреждений для детей и подростков.
При поступлении на работу (в дальнейшем один раз в год) обследованию подлежат работники общественного питания и лица, к ним приравненные; работники лечебно-профилактических учреждений для взрослых, санаториев, домов отдыха, связанные с питанием и обслуживанием больных и отдыхающих; стоматологи, работники сферы обслуживания населения (банщики, педикюрши, маникюрши, работники душевых, парикмахеры и подсобный персонал парикмахерских, работники прачечных, бельевых, горничные, уборщицы, работники общежитий, плавательных бассейнов, работники пассажирского транспорта и др.). Больные туберкулезом к работе в эти учреждения не допускаются (направляются в противотуберкулезный диспансер или специализированное отделение поликлиники).
Важное значение в профилактике туберкулеза имеют соблюдение санитарно-противоэпидемического режима на промышленных пред-приятиях, в детских дошкольных учреждениях, школах, предприятиях общественного питания, торговли, бытового обслуживания и санитарно-просветительная работа среди населения.
Выделены следующие факторы, которые оказывают влияние на способность организма противостоять туберкулезной инфекции:
1. Возраст и пол. Новорожденные и маленькие дети обоих полов обладают слабыми защитными силами. Инфицирование в возрасте до 2 лет часто приводит к развитию наиболее тяжелых форм милиарного туберкулеза и туберкулезного менингита при гематогенном распространении инфекции. До 17 лет заболеваемость девочек выше, чем у мальчиков. В Европе и Северной Америке в те времена, когда туберкулез был распространен, пик заболеваемости легочным туберкулезом обычно приходился на молодых взрослых людей.
Заболеваемость среди мужчин довольно высока во всех возрастных группах; среди женщин этот показатель резко снижается после репродуктивного периода. Женщины часто заболевают туберкулезом после родов. Общая заболеваемость женщин ниже и подъем ее с возрастом менее крутой, чем у мужчин. Максимальных величин она достигает среди женщин в возрасте 40 - 50 лет и затем падает. Среди мужчин она продолжает расти по меньшей мере до 60 лет.
2. Состояние питания. Существуют веские доказательства того, что голодание или недостаточность питания снижают сопротивляемость организма этой болезни. Этот фактор имеет важное значение у детей и взрослых в бедных странах.
3. Потребление токсичных продуктов. Курение табака и употребление большого количества алкоголя значительно снижают защитные силы организма. Такое же влияние оказывают кортикостероиды и другие иммунодепрессанты, применяемые для лечения некоторых заболеваний.
4. Другие заболевания. Во многих странах сейчас остро стоит проблема ВИЧ-инфекции. Поражение защитных механизмов организма часто оборачивается развитием туберкулеза. Туберкулезу также подвержены больные диабетом, лейкозами или лепрой. У детей милиарный туберкулез может развиваться после инфицирования ВИЧ, после кори, коклюша и других острых инфекций. Важными факторами, предрасполагающими к заболеванию туберкулезом в тропических странах, являются хроническая малярия и глистная инвазия.
5. Нищета. Нищета сопряжена с плохими жилищными и рабочими условиями, а также со скученностью населения. Эти факторы ослабляют защитные силы организма и способствуют распространению инфекции. Люди, живущие в таких условиях, обычно плохо питаются. Все эти составляющие облегчают заболевание туберкулезом инфицированных ТБ людей.
Кто подвергается наибольшему риску?
Туберкулез поражает, главным образом, молодых людей в их самые продуктивные годы. Однако риску подвергаются все возрастные группы. Более 95% случаев заболевания и смерти происходит в развивающихся странах.
При наличии сочетанной инфекции ВИЧ и ТБ вероятность того, что человек заболеет ТБ, возрастает в 21-34 раза (см. раздел о ТБ и ВИЧ). Люди, страдающие от других нарушений здоровья, ослабляющих иммунную систему, также подвергаются более высокому риску развития активного ТБ.
В 2010 году около полумиллиона детей (0-14 лет) заболели ТБ и 64 000 (от 58 000 до 71 000) детей умерли от этой болезни.
Употребление табака значительно повышает риск заболевания ТБ и смерти от него. Более 20% случаев заболевания ТБ в мире связано с курением.
| 10 фактов о туберкулезе (по данным ВОЗ) 1. В 2010 г. 8,8 миллиона человек заболели туберкулезом. Но туберкулез излечим и предотвратим. 2. В 2010 г. от туберкулеза умерло, в общей сложности, 1,4 миллиона человек (в том числе 350 000 людей с ВИЧ). Туберкулез остается одной из основных инфекционных причин смерти в мире. Около 95% случаев смерти от этой болезни происходит в странах с низким и средним уровнем дохода, и она входит в число трех основных причин смерти женщин в возрасте от 15 до 44 лет. 3. В 2010 г. в мире от туберкулеза умерло до 70 000 детей. Туберкулез у детей часто остается невыявленным медицинскими работниками, и его бывает сложно диагностировать и лечить. В мире насчитывается около 10 миллионов детей, осиротевших в результате смерти взрослых от туберкулеза. 4. Туберкулез – основная причина смерти людей с ВИЧ. Примерно каждый четвертый случай смерти среди людей с ВИЧ происходит в результате туберкулеза. Но благодаря координированным действиям служб ТБ и ВИЧ в области выявления, профилактики и лечения двойных инфекций за шесть лет (с 2005 по 2010 гг.) было спасено около 910 000 человеческих жизней. 5. Число людей, заболевающих туберкулезом, уменьшается, а смертность от него снизилась на 40% по сравнению с уровнем 1990 года. Например, на протяжении последних 20 лет Бразилия и Китай демонстрировали устойчивое уменьшение числа случаев заболевания туберкулеза. За этой период смертность в Китае снизилась на 80%.
6. В 2010 г. около 80% зарегистрированных случаев заболевания произошло в 22 странах. Туберкулез распространен в каждой части мира. В 2010 году 40% новых случаев заболевания туберкулезом произошло в Юго-Восточной Азии. Самый высокий показатель новых случаев на душу населения был отмечен в Африке к югу от Сахары. Нет ни одной страны, где туберкулез когда-либо был ликвидирован. 7. Туберкулез с множественной лекарственной устойчивостью (МЛУ-ТБ) не поддается стандартным типам лечения, лечить его сложно и дорого. МЛУ-ТБ – это форма ТБ, присутствующая практически во всех странах, где ВОЗ проводит исследования. Основной причиной развития множественной лекарственной устойчивости является ненадлежащее или неправильное использование противотуберкулезных препаратов. 8. По оценкам, в 2010 г. насчитывалось 650 000 людей с МЛУ-ТБ. В некоторых случаях при плохом лечении может развиваться еще более тяжелая форма туберкулеза с множественной лекарственной устойчивостью. Такая форма называется туберкулез с широкой лекарственной устойчивостью устойчивостью (ШЛУ-ТБ), она реагирует на еще более ограниченное число имеющихся лекарств. 9. С 1995 г. во всем мире проведено успешное лечение около 46 миллионов пациентов. С 1995 г. в рамках проведения ДОТС и Стратегии «Остановить ТБ» спасено до 7 миллионов человеческих жизней. 10. Мир продвигается к достижению двух глобальных целей, намеченных на 2015 год. Цель тысячелетия в области развития, направленная на то, чтобы остановить распространение туберкулеза и положить начало тенденции к снижению глобальной заболеваемости. Цель Партнерства «Остановить ТБ», направленная на двукратное сокращение числа случаев смерти от туберкулеза (по сравнению с уровнем 1990 года). |
Профилактика туберкулеза
Профилактика туберкулёза является важным звеном в борьбе с инфекцией и состоит из:
• Раннего и своевременного выявления и лечения больных туберкулёзом – стратегии, которая является важнейшим элементом профилактики, так как позволяет изолировать источник инфекции и лечить его как можно раньше, что предотвращает заражение здоровых людей от этого источника и позволяет лечить туберкулёз в самых начальных его стадиях с хорошим эффектом.
• Социальной профилактики – совокупность мероприятий по укреплению здоровья населения (улучшение материального и культурного уровня жизни, благоустройство улиц, здоровая экология, оздоровление условий труда, охрана матери и ребенка, физическая культура и др.).
• Санитарной профилактики – система мероприятий, направленных на борьбу с туберкулёзом, как инфекционным (заразным) заболе-ванием. Целью является предотвращение заражения здоровых людей в семье, на производстве, в местах общественного пользования
• Специфической профилактики – меры по предупреждению заражения и заболевания туберкулёзом при помощи вакцинопрофилактики вакциной БЦЖ и превентивного лечения (химиопрофилактики) групп риска.
Раннее и своевременное выявление и лечение больных туберкулёзом
Еще в доантибактериальный период были сформулированы основные принципы массовой флюорографии, когда более 50% всех больных деструктивным туберкулёзом легких с бактериовыделением умирали в течение 5 лет после установления диагноза. Именно флюорография является методом, который позволяет ограниченные формы туберкулёза без выявления МБТ. Несомненно, что многие жизни были спасены благодаря этому методу.
Общими симптомами активного легочного туберкулеза являются кашель иногда с мокротой и кровью, боль в груди, слабость, потеря веса, лихорадка и ночной пот.
Для диагностирования туберкулеза многие страны до сих пор полагаются на давно используемый метод, называемый микроскопией мазка мокроты. Специально подготовленные лаборанты исследуют мазки мокроты под микроскопом с целью обнаружения ТБ бактерий. При проведении трех таких тестов диагноз может быть поставлен в течение одного дня, но этот тест не выявляет многочисленные случаи менее инфекционных форм туберкулеза.
Диагностирование МЛУ-ТБ и ВИЧ-ассоциированного туберкулеза может быть более сложным. В настоящее время во многих странах используется новый двухчасовой тест, который оказался высокоэффективным в диагностировании ТБ и выявлении лекарственной устойчивости.
Особенно сложно диагностировать туберкулез у детей.
Туберкулез можно лечить и излечивать. В случае активной, чувствительной к лекарствам формы туберкулеза проводится стандартный шестимесячный курс лечения четырьмя противомикробными препаратами при обеспечении для пациента информации, наблюдения и поддержки со стороны работника здравоохранения или прошедшего специальную подготовку добровольного помощника. Без такого наблюдения и поддержки могут возникать сложности в соблюдении медицинских предписаний в отношении такого лечения, и болезнь может распространяться дальше. Подавляющее большинство случаев туберкулеза можно излечивать при условии надлежащего обеспечения и приема лекарств.
Всемирная организация здравоохранения всегда следила за ситуацией, складывающейся в мире по эпидемическим и социально значимым заболеваниям, и применительно к туберкулезу разработала стратегию лечения ДОТС (DOTS).
DOTS (Directly Observed Treatment Short-course) – это строго контролируемое лечение коротким курсом химиотерапии.
ДОТС – это базовый пакет, состоящий из 5 пунктов, который является первым компонентом Стратегии «Остановить ТБ»:
• политическая приверженность при надлежащем и устойчивом финансировании;
• раннее выявление случаев заболевания и постановка диагноза на основе бактериологии гарантированного качества;
• стандартизированное лечение при наблюдении за пациентами и оказании им поддержки;
• эффективное снабжение и управление лекарствами;
• мониторинг и оценка эффективности деятельности и воздействия
DOTS - единственная признанная стратегия контроля за туберкулезом, дающая не менее 85% излечения. При этом DOTS - одна из наиболее рентабельных методик в мировом здравоохранении.
ДОТС остается основой стратегии «Остановить ТБ». Для преодоления известных препятствий и решения новых проблем необходимо дальнейшее усиление основных пяти элементов стратегии ДОТС.
В настоящее время ВОЗ разработала новую состоящую из 6 пунктов стратегию «Остановить ТБ», основанную на успехах ДОТС и в то же время открыто направленную на решение основных проблем в области борьбы с туберкулезом. Ее целью является значительное уменьшение глобального бремени туберкулеза к 2015 году путем обеспечения для всех пациентов с туберкулезом, включая пациентов с сопутствующей ВИЧ-инфекцией и пациентов с туберкулезом с лекарственной устойчивостью, всеобщего доступа к высококачественной диагностике и ориентированному на пациента лечению. Стратегия также поддерживает разработку новых и эффективных инструментов для профилактики, выявления и лечения туберкулеза. Стратегия «Остановить ТБ» лежит в основе Глобального плана Партнерства «Остановить ТБ» по борьбе с туберкулезом на 2006-2015 годы.
| Шесть компонентов Стратегии «Остановить ТБ» 1. Продолжение распространения эффективно реализуемой стратегии DOTS 2. Борьба с ТБ-ВИЧ, МЛУ-ТБ с учетом потребностей больных из малоимущих и уязвимых групп населения 3. Содействие укреплению систем здравоохранения на основе развития первичной медико-санитарной помощи 4. Привлечение всех поставщиков медицинских услуг 5. Расширение прав и возможностей лиц с туберкулезом и общественных организаций через партнерское сотрудничество 6. Поддержка и развитие научных исследований |
С 1995 г. в рамках проведения ДОТС и стратегии «Остановить ТБ», рекомендуемых ВОЗ и описываемых ниже, более 46 миллионов человек прошли успешное лечение и, по оценкам, 7 миллионов человеческих жизней было спасено.
Туберкулез и ВИЧ-инфекция
По меньшей мере, одна треть из 34 миллионов людей с ВИЧ в мире инфицированы ТБ бактерией, однако еще не больны активной формой туберкулеза. Вероятность того, что у людей с ВИЧ, инфицированных туберкулезом, разовьется активная форма туберкулеза, в 21-34 раза превышает аналогичный показатель среди людей, неинфицированных ВИЧ.
ВИЧ-инфекция и туберкулез представляют собой смертельное сочетание, компоненты которого ускоряют развитие друг друга. Вероятность развития активной формы туберкулеза у человека, инфицированного ВИЧ и туберкулезом, возрастает во много раз. В 2010 г. около 350 000 человек умерли от ВИЧ-ассоциированного туберкулеза. Почти 35% случаев смерти среди людей с ВИЧ вызваны туберкулезом. По оценкам, в 2010 г. произошло 1,1 миллиона новых случаев заболевания туберкулезом среди ВИЧ-позитивных людей, 82% из которых имели место в Африке.
ВОЗ рекомендует применять 12-компонентный подход к интегрированным службам ТБ-ВИЧ, включая действия для профилактики и лечения инфекции и болезни и для уменьшения смертности.
Клинические проявления туберкулеза у ВИЧ-инфицированных:
1. Внелегочное заболевание. Особенно часто отмечается поражение лимфатических узлов. Нередко наблюдается генерализованное увеличение лимфатических узлов, не характерное для других форм туберкулеза.
2. Часто встречается милиарный процесс. ТБ могут быть выделены при культивировании крови (чего никогда не бывает при обычном туберкулезе).
3. Рентгенограмма. При легочном процессе часто отмечается увеличение тени медиастинальных лимфатических узлов. Нередко процесс локализуется в нижней доле легкого. Образование каверн встречается реже, хотя, по сообщениям из разных мест их частота варьируется. Чаще бывают плевральные выпоты. Тени в легких очень динамичны.
4. Туберкулез может развиться в необычных местах (туберкуломы мозга, абсцессы грудной стенки или других мест).
5. Бактериоскопические анализы мокроты отрицательны, несмотря на наличие значительных изменений в легких на рентгенограмме (хотя некоторые исследователи в Африке считают, что бактериовыделение в мокроте методом бактериоскопии выявляется так же часто, как и у больных, не инфицированных ВИЧ).
6. Туберкулиновая проба часто отрицательна.
Если у больного туберкулезом имеются следующие признаки, нельзя исключить сопутствующую ВИЧ-инфекцию:
• генерализованное увеличение лимфатических узлов
• грибковая инфекция (болезненные, белые пятна гриба в полости рта)
• хроническая диарея, продолжающаяся более месяца
• опоясывающий лишай
• саркома Капоши: ищите мелкие красные, сосудистые узелки на коже и особенно на небе.
Детский туберкулез
Масштабы детского туберкулеза неизвестны. По оценкам, на него приходится 6% всех случаев заболевания, а большинство случаев происходит в странах с тяжелым бременем туберкулеза. Среди многих проблем, препятствующих оценке бремени туберкулеза среди детей, можно перечислить следующие:
• трудности постановки точного диагноза;
• наличие дополнительного легочного заболевания (при котором необходима консультация у специалиста);
• низкая приоритетность для общественного здравоохранения (детский туберкулез редко бывает положительным по мазку);
• и отсутствие связей между педиатрами частного сектора и национальной программой по туберкулезу.
По данным ВОЗ, дети могут заболевать туберкулезом в любом возрасте, но наиболее часто в возрасте от 1 до 4 лет. Регистрация случаев детского туберкулеза зависит от интенсивности эпидемии, возрастной структуры населения, имеющихся диагностических методик и масштабов регулярного отслеживания контактов.
Стратегия «Остановить ТБ», в основе которой лежит стратегия ДОТС, разработанная ВОЗ и Международным союзом по борьбе против туберкулеза и Союзом легочных заболеваний, играет решающую роль в уменьшении бремени болезни во всем мире и, таким образом, защите детей от инфекции и болезни. Лечение детей с туберкулезом должно осуществляться в соответствии со стратегий «Остановить ТБ» с учетом особой эпидемиологии и клинической картины туберкулеза у детей.
Основные мероприятия по борьбе с туберкулезом у детей
1. Мобилизация приверженности делу борьбы с туберкулезом у детей на глобальном и национальном уровнях.
2. Содействие созданию стратегических партнерств и успешному взаимодействию в рамках системы здравоохранения, особенно между программами по туберкулезу, охране здоровья матери и ребенка и иммунизации и соответствующими заинтересованными сторонами, с целью установления приоритетов и содействия раннему выявлению и ведению детей с туберкулезом.
3. Отстаивание необходимости проведения дополнительных исследований и разработки новых диагностических средств, лекарственных препаратов и вакцин для детей с туберкулезом.
4. Проведение расследования контактов и предоставление иммунопрофилактики туберкулеза детям в возрасте до 5 лет на основе специальной подготовки и повышения осведомленности работников здравоохранения и местных сообществ в отношении туберкулеза у детей.
5. Содействие включению подходов, ориентированных на семью, в мероприятия в области туберкулеза и ВИЧ.
Подгруппа по детскому туберкулезу в составе Рабочей группы по расширению ДОТС была создана в 2003 году для содействия научным исследованиям, разработке политики, формулированию и осуществлению руководящих принципов, мобилизации трудовых и финансовых ресурсов, а также сотрудничеству с партнерами, работающими в соответствующих областях (включая здоровье матерей и детей, иммунизацию и ВИЧ), для достижения цели по снижению смертности и заболеваемости детским туберкулезом.
Санитарная профилактика (гигиена среды обитания)
В течение 123 лет, прошедших со времени открытия возбудителя туберкулёза, гигиенистами и фтизиатрами была разработана система санитарно-профилактических мероприятий, имеющих непосредственной целью предупреждение заражения людей туберкулёзом. Научной основой санитарной профилактики является эпидемиология туберкулёза, учение о возбудителе этого заболевания, об источниках инфекции и путях распространения туберкулёзной инфекции, учение о противотуберкулёзном иммунитете.
Основным методом, направленным на разрыв механизма передачи возбудителя, является дезинфекция, основными способами обеззараживания при которой являются:
• средства и приемы механической дезинфекции (мытье, влажная уборка, стирка, чистка, вентиляция и др.);
• физические методы (кипячение белья, посуды, игрушек, сжигание мусора), которые обладают также достаточно сильным действием на МБТ;
• химический способ, обеспечивающий уничтожение МБТ дезинфицирующими растворами.
Каждый больной туберкулёзом должен иметь отдельную комнату, ему необходимо иметь отдельную посуду, которая хранится и моется отдельно. Больной туберкулёзом должен соблюдать культуру кашля - закрывать рот при кашле одноразовой салфеткой или тыльной стороной кисти, собирать мокроту в специальный контейнер для сбора мокроты (плевательницу).
Посуду больного необходимо тщательно очищать от остатков пищи, а затем обеззараживать путем кипячения в 2% содовом растворе в течение 15 минут с момента закипания, либо погружения в вертикальном положении на 1 час в 0,5% активированный раствор хлорамина.
Постельное и нательное белье больного собирают в специальный мешок и хранят его до обеззараживания и стирки. Обеззараживание белья производят путем замачивания в 2% растворе соды с последующим 15-минутным кипячением, либо путем погружения в 1% активированный раствор хлорамина (при норме расхода 5 л дезраствора на 1 кг сухого белья) на 1-2 часа при температуре не ниже 14ºС.
Носильную одежду больных следует по возможности чаще проветривать на солнце, гладить горячим утюгом.
Подушки, одеяла, матрацы подвергают камерной дезинфекции не реже 4 раз в год, проветривают и просушивают под прямыми солнечными лучами.
Книги, тетради, игрушки и т.п. должны быть в индивидуальном пользовании больного и без предварительной камерной дезинфекции другим людям передаваться не могут.
Уборка помещений больного производится ежедневно влажным способом горячим 2% мыльно-содовым раствором при открытых окнах или форточках в зависимости от сезона. При этом следует пользоваться отдельными предметами уборки.
С целью предупреждения передачи инфекции необходимо проводить борьбу с мухами. С этой целью необходимо соблюдать санитарно-гигиенический режим, ликвидировать субстраты, пригодные для размножения мух, уничтожать личинок и куколок в местах их выплода и защищать жилые помещения при помощи металлических сеток (размер ячеек не более 1,5 мм) или марлей.
Специфическая профилактика
Бацилла Кальметта—Герена или БЦЖ (Bacillus Calmette—Guérin, BCG) — вакцина против туберкулёза, приготовленная из штамма ослабленной живой коровьей туберкулёзной палочки (лат. Mycobacterium bovis BCG), которая практически утратила вирулентность для человека, будучи специально выращенной в искусственной среде.
Контролируемые исследования, проведенные в ряде западных стран, показали, что БЦЖ может в 80% случаев предотвратить развитие туберкулеза в течение 15 лет.
В повышении невосприимчивости организма к туберкулезу боль¬шую роль играет плановая специфическая иммунизация населения живой вакциной БЦЖ и БЦЖ-М, которой подлежат неинфицированные микобактериями дети и взрослые. Новорожденные получают вакцину БЦЖ-М однократно на 3-7-й день после рождения. Вакцину вводят внутрикожно на наружную поверхность верхней трети плеча левой руки по 0,025 мг живой сухой вакцины. Однако на территориях с заболеваемостью туберкулезом превышающей показатель 80 на 100 тыс. населения, а также при наличии в окружении новорожденного больного туберкулезом новорожденных вакцинируют вакциной БЦЖ.
Ревакцинации БЦЖ вакциной в дозе 0,05 мг внутрикожным методом подлежат неинфицированные туберку¬лезом туберкулинотрицательные дети и подростки в возрасте 7 лет (в 1-м классе школы) и 14 лет.
Туберкулинодиагностика, применяется для отбора контингентов подлежащих ревакцинации, а также первичной вакцинации, проводимой в возрасте старше 2 месяцев. Используют внутрикожную туберкулиновую пробу Манту с 2 туберкулиновыми единицами (2ТЕ) очищенного туберкулина. Реакция считается отрицательной (нет папулы, гиперемии, только уколочная реакция 0-1 мм), сомнительной (папула 2-4 мм или гиперемия любого размера без инфильтрата) или положительной (папула более или равна 5 мм или везикула, лимфангоит или некроз независимо от размера инфильтрата). Вакцину БЦЖ вводят только детям с отрицательной р. Манту.
В настоящее время разработаны стандарты химиотерапии больных туберкулёзом. Их своевременное выявление и эффективная химиотерапия — основные методы уменьшения резервуара туберкулёзной инфекции.
гиперемия не учитывается).
Многолетние наблюдения за вакцинированными и ревакцинированными, показали, что БЦЖ снижает заболеваемость, смертность, первичное инфицирование, а также предупреждает развитие тяжелых форм туберкулёза (менингит, милиарный туберкулёз, казеозная пневмония).
ВОЗ и Международный союз по борьбе с туберкулезом и другими болезнями легких рекомендуют в странах с высокой заболеваемостью туберкулезом обязательно делать прививки БЦЖ всем детям в возрасте до 1 года.
Длительность эффекта БЦЖ составляет примерно 15 лет, по крайней мере в хорошо питающейся популяции. Она обеспечивает защиту от туберкулеза в детстве, но постепенно теряет свою силу, поэтому необходимо проводить ревакцинацию (повторную прививку).
Превентивное лечение (химиопрофилактика)
Под химиопрофилактикой туберкулеза понимают введение туберкулостатических препаратов здоровым людям с целью предупреждения заражения или развития у них заболевания туберкулезом. При этом химиопрофилактика не только не нарушает естественный и сформированный иммунитет к туберкулёзной инфекции, но и стимулирует последний, уменьшая возможность развития эндогенной реактивации туберкулёза.
Химиопрофилактика как эффективный метод специфической профилактики туберкулеза применяется в нашей стране с 1962 г. в группах повышенного риска заболевания туберкулезом.
Профилактическое лечение должно применяться только по определенным, четко обозначенным показаниям и у ограниченного контингента лиц. Его значение заключается в том, чтобы предупредить заболевание туберкулезом у тех групп населения, которые подвергаются наибольшему риску заболеть. Согласно данным ВОЗ, плацебо-контролируемые рандомизированные клинические исследования продемонстрировали, что 6-12 месячный профилактический курс изониазида сокращает риск развития активного туберкулёза у инфицированных лиц до 80%.
Химиопрофилактике ( превентивному лечению) подлежат:
1. Взрослые лица, состоящие в бытовом, производственном и профессиональном контакте с источником инфекции, а также дети и подростки из семейных, родственных и квартирных очагов активного туберкулёза, из контактов с сотрудниками детских и подростковых учреждений, больных активным туберкулёзом, из неблагополучных по туберкулёзу животноводческих хозяйств.
2. Дети и подростки, у которых при постановке ежегодной пробы Манту с 2 ТЕ ППД-Л выявляется первичное инфицирование («вираж» туберкулиновой пробы), гиперергическая реакция на туберкулин и резкое увеличение размеров пробы (размер папулы вырос на 6 мм и более по сравнению с предыдущей пробой).
3. Больные силикозом и другими производственными заболеваниями легких.
4. Лица, относящиеся к группам повышенного риска по заболеванию туберкулезом (проходящие курс иммунодепрессивной терапии, страдающие ретикулоэндотелиозами), а также лица после гастрэктомии и др.
Уроки для профилактики
Многие из факторов, упомянутых выше, можно устранить, приняв лишь меры экономического характера или предприняв правительственные действия по улучшению качества жизни населения. В развитых странах эти меры, видимо, сыграли наиважнейшую роль в долговременном снижении заболеваемости туберкулезом. Врачебное сообщество, вероятно, не может что-либо сделать в этом плане. Однако в последние годы широкомасштабное эффективное лечение ускорило это снижение за счет уменьшения числа бактериовыделителей среди населения. Задача первостепенной важности состоит в раннем выявлении и лечении больных туберкулезом, распространителей заболевания.
Сокращение потребления табака будет способствовать предотвращению туберкулеза, рака легких (и других видов рака), ишемической болезни сердца, хронического бронхита и т.д. Для врача очень важно не курить самому и никогда в присутствии больных.
Снижение национального потребления никотина и алкоголя также помогает снизить заболеваемость туберкулезом, поэтому врачам следует активно поддерживать общенациональные антитабачные и антиалкогольные программы, которые послужат профилактике других серьезных заболеваний, помимо туберкулеза.
Контрольные вопросы
1. Что такое туберкулез?
2. Назовите возбудителя туберкулеза
3. Какие факторы сопутствуют заболеванию туберкулезом?
4. Каковы факторы, снижающие сопротивляемость организма туберкулезной инфекции?
5. Из каких компонентов состоит профилактика туберкулёза?
6. Какие клинические проявления туберкулёза у ВИЧ-инфицированных?
Корь — острая антропонозная вирусная инфекционная болезнь с аспирационным механизмом передачи возбудителя. Характеризуется лихорадкой, интоксикацией, этапным высыпанием пятнисто-папулезной сыпи, энантемой, катаральными явлениями со стороны конъюнктивы, носоглотки и верхних дыхательных путей.
Заболевание нередко осложняется поражением бронхолегочной системы, могут возникать коревые энцефалиты и менингоэнцефалиты с тяжелыми последствиями. При внутриутробном инфицировании возможно формирование медленной инфекции с прогредиентным течением по типу подострого склерозирующего панэнцефалита.
Возбудитель - РНК-содержащий вирус из семейства Paramyxoviridae рода Morbilivirus. Вирус малоустойчив во внешней среде: быстро инактивируется под влиянием солнечного света, ультрафиолетовых лучей. При комнатной температуре сохраняет активность около 1-2 сут, при низкой температуре – в течение нескольких недель. В высушенном состоянии при температуре -20°С вирус не теряет активности в течение года. При температуре 37°С инактивация половины популяции вируса наступает через 2 ч, при 56°С вирус гибнет в течение 30 мин, при 60°С - мгновенно.
Резервуар и источники возбудителя: больной человек, выделяющий вирус с последних 1-2 сут инкубационного периода, в течение всего продромального периода (за 3-4 дня до появления сыпи) и в первые 4 дня высыпания. При осложнениях, иногда сопровождающих болезнь, возможно удлинение заразного периода до 10 суток с момента появления сыпи.
Механизм передачи возбудителя аспирационный; путь передачи - воздушно-капельный. В составе носоглоточной слизи вирус выделяется из организма при кашле, чихании, разговоре и даже дыхании. С потоком воздуха может разноситься на значительные расстояния.
Входными воротами инфекции служит слизистая оболочка верхних дыхательных путей. Вирус размножается в эпителии респираторного тракта, а также в других эпителиальных клетках. В отдельных случаях вирус может заноситься в головной мозг, обусловливая развитие специфического коревого энцефалита. При заболевании беременной корью возможна реализация вертикальной передачи инфекции.
Естественная восприимчивость людей чрезвычайно высокая: обычно заболевают все не иммунные лица, общавшиеся с больным; материнский иммунитет защищает до 6 мес. Дети первого года жизни обычно защищены материнскими антителами, при условии, если мать ранее переболела корью или была вакцинирована против нее. Постинфекционный иммунитет, как правило, пожизненный, хотя известны случаи повторных заболеваний.
Основные эпидемиологические и клинические признаки. Развитие эпидемического процесса при кори определяют следующие основные факторы:
• абсолютная восприимчивость людей;
• пожизненная невосприимчивость у переболевших корью;
• аспирационный легкореализуемый механизм передачи вируса;
• слабая устойчивость вируса во внешней среде;
• антигенная стабильность вируса;
• интенсивность и характер общения людей.
Начальный (продромальный) период при кори характеризуется повышением температуры тела до 38-39°С, общим недомоганием, насморком, кашлем, гиперемией конъюнктив, пурпурной энантемой в виде мелких красных пятен на слизистой оболочке мягкого и твердого нёба, а также мелкими белесоватыми пятнышками с узкой красноватой каемкой на слизистой оболочке щек (пятна Вельского - Филатова - Коплика). На 3-4-й день появляется коревая медно-красная макулезная сыпь, характеризующаяся этапностью высыпания: вначале на лице и шее, на туловище, руках и бедрах и наконец - на нижних конечностях, после чего сыпь бледнеет и исчезает в той же последовательности.
Распространение кори носит повсеместный характер. Имевшая ранее место поголовная заболеваемость в последние годы во многих странах резко снижена за счет массовой специфической иммунизации.
С 2002 года Европейским региональным бюро ВОЗ разработана и реализуется «Стратегическая программа элиминации кори и краснухи и профилактики врожденной краснушной инфекции в европейской регионе ВОЗ в 2010 г.».
На 60-ой сессии ЕРБ ВОЗ (сентябрь 2010 г., г. Москва) было отмечено, что не смотря на прекращение циркуляции возбудителей кори и краснухи во многих странах, региональные цели элиминации этих инфекций к 2010 г. не достигнуты, о чем свидетельствуют факты эпидемиологического неблагополучия по кори в ряде европейских стран.
Срок элиминации кори в европейском регионе перенесен с 2010 на 2015 г.
Программа ликвидации кори на территории Российской Федерации была утверждена в 2002 г. она осуществлялась в три этапа. Первые два этапа (2002-2004гг. и 2005-2007гг.) предусматривали создание условий для предупреждения возникновения случаев кори на всех территориях страны и в основном были выполнены.
Целью третьего этапа Программы (2008-2010гг.) было подтверждение статуса территории, свободной от местных случаев заболевания корью.
Однако, со второй половины 2007г. на фоне значительного снижения заболеваемости корью произошло изменение спектра циркулирующих генотипов вируса, которые ранее в России не циркулировали, что привело к возникновению крупных вспышек кори.
Исходя из стратегии ликвидации кори, основное внимание должно быть направлено на достижение стабильно высокого (не менее 95%) уровня охвата прививками декретированных контингентов и проведение эффективного надзора, предусматривающего полное выявление клинических случаев кори среди людей с экзантемными заболеваниями с обязательным лабораторным подтверждением диагноза.
Вакцинопрофилактика и эффективный эпидемиологический надзор существенно повлияли на уровень заболеваемости кори. Был достигнут показатель заболеваемости менее 1 случая на миллион населения, что соответствовало критерию элиминации кори, определенному ВОЗ и это дало основание приступить в 2010 году к процедуре сертификации в России, подтверждающей элиминацию кори.
Профилактические мероприятия.
Наиболее эффективна массовая плановая специфическая иммунопрофилактика живой коревой вакциной не болевших корью детей в возрасте до 12 мес и их ревакцинация в 6 лет.
В случае выявления больного корью информация о заболевшем направляется в территориальный центр Роспотребнадзора в виде Экстренного извещения не позже чем через 12 ч после выявления больного. Лечебно-профилактическое учреждение, уточнившее, изменившее или отменившее диагноз, обязано в течение 24 ч отослать новое извещение.
В очаге кори устанавливают медицинское наблюдение за не болевшими корью детьми. По эпидемическим показаниям проводят экстренную профилактику кори. Она проводится в эпидемических очагах контактным детям и взрослым (без ограничения возраста), не болевшим и не имеющим прививок против кори или имеющим одну прививку.
Иммунитет после перенесенной естественной коревой инфекции стойкий. Повторные заболевания корью встречаются крайне редко.
Вакцинация против кори
Контрольные вопросы
1. Что такое туберкулез?
2. Назовите возбудителя туберкулеза
3. Какие факторы сопутствуют заболеванию туберкулезом?
4. Каковы факторы, снижающие сопротивляемость организма туберкулезной инфекции?
5. Из каких компонентов состоит профилактика туберкулёза?
6. Какие клинические проявления туберкулёза у ВИЧ-инфицированных?
5.8 Профилактика кори
Корь — острая антропонозная вирусная инфекционная болезнь с аспирационным механизмом передачи возбудителя. Характеризуется лихорадкой, интоксикацией, этапным высыпанием пятнисто-папулезной сыпи, энантемой, катаральными явлениями со стороны конъюнктивы, носоглотки и верхних дыхательных путей.
Заболевание нередко осложняется поражением бронхолегочной системы, могут возникать коревые энцефалиты и менингоэнцефалиты с тяжелыми последствиями. При внутриутробном инфицировании возможно формирование медленной инфекции с прогредиентным течением по типу подострого склерозирующего панэнцефалита.
Возбудитель - РНК-содержащий вирус из семейства Paramyxoviridae рода Morbilivirus. Вирус малоустойчив во внешней среде: быстро инактивируется под влиянием солнечного света, ультрафиолетовых лучей. При комнатной температуре сохраняет активность около 1-2 сут, при низкой температуре – в течение нескольких недель. В высушенном состоянии при температуре -20°С вирус не теряет активности в течение года. При температуре 37°С инактивация половины популяции вируса наступает через 2 ч, при 56°С вирус гибнет в течение 30 мин, при 60°С - мгновенно.
Резервуар и источники возбудителя: больной человек, выделяющий вирус с последних 1-2 сут инкубационного периода, в течение всего продромального периода (за 3-4 дня до появления сыпи) и в первые 4 дня высыпания. При осложнениях, иногда сопровождающих болезнь, возможно удлинение заразного периода до 10 суток с момента появления сыпи.
Механизм передачи возбудителя аспирационный; путь передачи - воздушно-капельный. В составе носоглоточной слизи вирус выделяется из организма при кашле, чихании, разговоре и даже дыхании. С потоком воздуха может разноситься на значительные расстояния.
Входными воротами инфекции служит слизистая оболочка верхних дыхательных путей. Вирус размножается в эпителии респираторного тракта, а также в других эпителиальных клетках. В отдельных случаях вирус может заноситься в головной мозг, обусловливая развитие специфического коревого энцефалита. При заболевании беременной корью возможна реализация вертикальной передачи инфекции.
Естественная восприимчивость людей чрезвычайно высокая: обычно заболевают все не иммунные лица, общавшиеся с больным; материнский иммунитет защищает до 6 мес. Дети первого года жизни обычно защищены материнскими антителами, при условии, если мать ранее переболела корью или была вакцинирована против нее. Постинфекционный иммунитет, как правило, пожизненный, хотя известны случаи повторных заболеваний.
Основные эпидемиологические и клинические признаки. Развитие эпидемического процесса при кори определяют следующие основные факторы:
• абсолютная восприимчивость людей;
• пожизненная невосприимчивость у переболевших корью;
• аспирационный легкореализуемый механизм передачи вируса;
• слабая устойчивость вируса во внешней среде;
• антигенная стабильность вируса;
• интенсивность и характер общения людей.
Начальный (продромальный) период при кори характеризуется повышением температуры тела до 38-39°С, общим недомоганием, насморком, кашлем, гиперемией конъюнктив, пурпурной энантемой в виде мелких красных пятен на слизистой оболочке мягкого и твердого нёба, а также мелкими белесоватыми пятнышками с узкой красноватой каемкой на слизистой оболочке щек (пятна Вельского - Филатова - Коплика). На 3-4-й день появляется коревая медно-красная макулезная сыпь, характеризующаяся этапностью высыпания: вначале на лице и шее, на туловище, руках и бедрах и наконец - на нижних конечностях, после чего сыпь бледнеет и исчезает в той же последовательности.
Распространение кори носит повсеместный характер. Имевшая ранее место поголовная заболеваемость в последние годы во многих странах резко снижена за счет массовой специфической иммунизации.
С 2002 года Европейским региональным бюро ВОЗ разработана и реализуется «Стратегическая программа элиминации кори и краснухи и профилактики врожденной краснушной инфекции в европейской регионе ВОЗ в 2010 г.».
На 60-ой сессии ЕРБ ВОЗ (сентябрь 2010 г., г. Москва) было отмечено, что не смотря на прекращение циркуляции возбудителей кори и краснухи во многих странах, региональные цели элиминации этих инфекций к 2010 г. не достигнуты, о чем свидетельствуют факты эпидемиологического неблагополучия по кори в ряде европейских стран.
Срок элиминации кори в европейском регионе перенесен с 2010 на 2015 г.
Программа ликвидации кори на территории Российской Федерации была утверждена в 2002 г. она осуществлялась в три этапа. Первые два этапа (2002-2004гг. и 2005-2007гг.) предусматривали создание условий для предупреждения возникновения случаев кори на всех территориях страны и в основном были выполнены.
Целью третьего этапа Программы (2008-2010гг.) было подтверждение статуса территории, свободной от местных случаев заболевания корью.
Однако, со второй половины 2007г. на фоне значительного снижения заболеваемости корью произошло изменение спектра циркулирующих генотипов вируса, которые ранее в России не циркулировали, что привело к возникновению крупных вспышек кори.
Исходя из стратегии ликвидации кори, основное внимание должно быть направлено на достижение стабильно высокого (не менее 95%) уровня охвата прививками декретированных контингентов и проведение эффективного надзора, предусматривающего полное выявление клинических случаев кори среди людей с экзантемными заболеваниями с обязательным лабораторным подтверждением диагноза.
Вакцинопрофилактика и эффективный эпидемиологический надзор существенно повлияли на уровень заболеваемости кори. Был достигнут показатель заболеваемости менее 1 случая на миллион населения, что соответствовало критерию элиминации кори, определенному ВОЗ и это дало основание приступить в 2010 году к процедуре сертификации в России, подтверждающей элиминацию кори.
Профилактические мероприятия.
Наиболее эффективна массовая плановая специфическая иммунопрофилактика живой коревой вакциной не болевших корью детей в возрасте до 12 мес и их ревакцинация в 6 лет.
В случае выявления больного корью информация о заболевшем направляется в территориальный центр Роспотребнадзора в виде Экстренного извещения не позже чем через 12 ч после выявления больного. Лечебно-профилактическое учреждение, уточнившее, изменившее или отменившее диагноз, обязано в течение 24 ч отослать новое извещение.
В очаге кори устанавливают медицинское наблюдение за не болевшими корью детьми. По эпидемическим показаниям проводят экстренную профилактику кори. Она проводится в эпидемических очагах контактным детям и взрослым (без ограничения возраста), не болевшим и не имеющим прививок против кори или имеющим одну прививку.
Иммунитет после перенесенной естественной коревой инфекции стойкий. Повторные заболевания корью встречаются крайне редко.
Вакцинация против кори
Вакцинацию против кори проводят не болевшим корью детям в возрасте 12-15 месяцев. Вторая прививка вводится в возрасте 6 лет (перед школой). Использование второй дозы вакцины позволяет защитить детей, которые не были вакцинированы, а также тех, кто не выработал иммунитет после первой дозы вакцины. В рамках Национального календаря профилактических прививок вакцина против кори вводится одновременно с вакцинами против паротита, краснухи и гепатита В. Согласно Национальному календарю профилактических прививок иммунизацию против кори также проводят в возрасте 15-17 лет включительно и взрослым, не привитым ранее, не имеющим сведений о прививках против кори и не болевшим корью двукратно с интервалом не менее 3-х мес. Людей, имеющих одну прививку против кори, прививают однократно.
Экстренная профилактика
В первые 3 дня от момента контакта с больным, необходимо введение вакцины не болевшим корью и не привитым детям старше 12 месяцев, подросткам и взрослым. При наличии противопоказаний к введению вакцины в качестве экстренной профилактики используют противокоревой иммуноглобулин или нормальный иммуноглобулин человека до 4-го дня от момента контакта.
Контрольные вопросы:
1. Каковы особенности коревой инфекции?
2. Какие методы профилактики кори Вы знаете?
Краснуха — антропонозная острая вирусная инфекционная болезнь с аспирационным механизмом передачи возбудителя. С клинической точки зрения характеризуется мелкой пятнисто-папулезной сыпью, генерализованной лимфаденопатией, умеренной интоксикацией и поражением плода у беременных.
Различают постнатальную (приобретенную) и антенатальную (врожденную) краснуху.
Постнатальная (приобретенная) краснуха — источником инфекции является больной с манифестной или бессимптомной формой течения инфекционного процесса. Заболевание обычно протекает гладко, но иногда может осложняться энцефалитом или менингоэнцефалитом и очень редко тромбоцитопенией.
Антенатальная (врожденная) краснуха проявляется пороками развития сердца (дефекты предсердной или желудочковой перегородки, стеноз легочной артерии, незаращение боталлова протока), глаз (катаракта, микрофтальмия, глаукома, хориоретинит), центральной нервной системы (менингоэнцефалит, микроцефалия, задержка умственного развития) и глухотой. Возможны также отставание в росте, гепатоспленомегалия, тромбоцитопения, желтуха, поражение трубчатых костей и др. Течение болезни длительное, с персистированием вируса от нескольких месяцев до 1,5 лет и больше. Врожденная краснуха у плода может развиться и после бессимптомной краснухи у беременной.
Возбудитель - РНК-содержащий вирус из семейства Togaviridae рода Rubivirus. Проявляет тератогенную активность. Малоустойчив к действию физических и химических факторов: при температуре 37°С 90% вирусов инактивируется за 4 мин, при 100°С - за 2 мин; вирус быстро разрушается под действием органических растворителей, хлорактивных соединений, формалина, УФ-лучей.
Резервуар и источники возбудителя: человек с клинически выраженной или бессимптомно протекающей инфекцией. Больной выделяет вирус во внешнюю среду за 1 нед до появления сыпи и в течение 5-7 дней после появления высыпаний. Большое эпидемиологическое значение имеют дети с врожденной краснухой, в организме которых вирус может сохраняться до 1,5 года и более, а также больные скрытой формой инфекции, которых среди взрослых в 6 раз больше, чем больных типичной манифестной формой.
Механизм передачи возбудителя аспирационный; путь передачи - воздушно-капельный. Вирус выделяется из организма больного с секретом слизистой оболочки верхних дыхательных путей (наиболее интенсивно за сутки до появления клинических симптомов заболевания). Для реализации механизма передачи необходимо более тесное общение с больным, чем при кори или ветряной оспе. Самостоятельное значение имеет вертикальный механизм передачи возбудителя плоду от матери, заболевшей в первые 4 мес беременности.
Естественная восприимчивость людей высокая.
Основные эпидемиологические и клинические признаки. ВОЗ относит краснуху к инфекциям, ликвидация которых возможна в ближайшем будущем. С учетом значения для здравоохранения синдрома врожденной краснухи, 48-я сессия Регионального комитета ВОЗ для Европы (1998) включила краснуху в число инфекций, борьба с которыми будет определять цели программы «Здоровье для всех в ХХI веке». К 2010 г частота синдрома врожденной краснухи должна быть снижена до уровня менее 0,01 на 1000 новорожденных.
В довакцинальный период краснуху с высокой заболеваемостью регистрировали повсеместно. По данным ВОЗ, из всех случаев краснухи, регистрируемых в Европе, 83% приходилось на страны СНГ, причем 57% из них на Российскую Федерацию. В большинстве стран мира к 6-10 годам жизни более половины детей имеют противокраснушные антитела в крови, а к 20 годам - 80-95%. В последние годы отмечается сдвиг заболеваемости на женщин детородного возраста. Характерны выраженные периодические подъемы заболеваемости с интервалом в 3 - 4 года, особенно выраженные через 7-10 лет, перемежающиеся периодами спорадической заболеваемости. Основная заболеваемость регистрируется среди детей 3-9 лет, главным образом посещающих дошкольные детские учреждения и начальные классы школ. Характерна выраженная зимне-весенняя сезонность с пиком в апреле - мае.
Краснуху принять считать легким заболеванием. В целом у детей краснуха протекает легко, осложнения наблюдаются редко. Наиболее грозным осложнением является краснушный энцефалит, его частота достаточно редка и составляет, по данным ряда авторов 1:5000-1:6000 случаев.
Краснуха во взрослом и подростковом возрасте протекает значительно тяжелее. Более выражена лихорадка, явления интоксикации (недомогание, разбитость), отмечаются поражения глаз (конъюнктивит). Характерным в клинике краснухи у взрослых (с большей частотой у женщин) является поражение мелких (фаланговые, пястно-фаланговые) и реже крупных (коленные, локтевые) суставов.
Большинство больных не нуждаются в специальном лечении. Проводят в основном симптоматическое лечение. После перенесенного заболевания развивается пожизненный противокраснушный иммунитет, однако его напряженность с возрастом и под воздействием различных факторов, может падать. Таким образом, перенесенное в детстве заболевание краснухой не может служить 100% гарантией от повторного заболевания.
Заболевание беременной женщины приводит к инфицированию плода. В зависимости от срока беременности, на котором происходит заражение, у плода c различной вероятностью (в первом триместре вероятность достигает 90%, во втором - до 75%, в третьем - 50%) формируются множественные пороки развития, входящие в понятие «Синдром врожденной краснухи (СВК)». К СВК также относят дефекты формирования костей черепа, головного мозга (малый размер мозга, умственная отсталость), внутренних органов (желтуха, увеличение печени, миокардит и др.) и костей (участки разрежения костной ткани длинных трубчатых костей). В 15% случаев краснуха у беременных приводит к выкидышу, мертворождению. При выявлении краснухи всегда осуществляется искусственное прерывание беременности. По оценкам ВОЗ всего на планете краснуха ежегодно калечит около 300 тыс. детей.
Профилактические мероприятия.
Существует три принципиальных подхода (стратегии) к профилактике и искоренению краснухи: вакцинация детей, вакцинация девушек-подростков и вакцинация женщин детородного возраста, планирующих иметь детей.
Первая стратегия эффективна против борьбы с самой краснухой, но полностью не решает проблемы СВК (для этого потребуется 20-30 лет), поскольку по имеющимся данным, вакцинация защищает на срок около 20 лет, а значит, теоретически она способна сдвинуть заболеваемость краснухой на детородный возраст.
Вторая стратегия, вакцинация девушек-подростков (в 11-14 лет) эффективна в плане искоренения СВК (однако, для достижения этой цели потребуется 10-20 лет), но не решает проблемы искоренения заболеваемости краснухой (в России пик приходится на возраст 7-14 лет).
Вакцинация женщин крайне эффективна в плане борьбы с СВК (хотя добиться 100% охвата взрослого населения прививками против краснухи практически не реально), но также не решает проблемы искоренения краснухи.
Ввиду вышеприведенных обстоятельств ВОЗ рекомендует сочетать по мере возможности все три стратегии. Примером такого сочетания является США, где помимо вакцинации детей, вакцинация проводится в колледжах и вооруженных силах. Интересный выход из проблемы вакцинации женщин детородного возраста нашли во Франции - отказ в регистрации брака при отсутствии отметки о прививке против краснухи, либо записи о перенесенной инфекции.
Вакцинация потив краснухи
В России прививка против краснухи в Национальный календарь профилактических прививок включена в 1997 г. Вакцинацию проводят детям в возрасте 12 мес однократно, ревакцинацию - в 6 лет. Для иммунизации возможно применение ассоциированных вакцин, содержащих краснушный, коревой и паротитный компоненты.
Для профилактики врожденной краснухи при заболевании женщин в первые 16 нед. беременности рекомендуют ее прерывание.
Информация о заболевшем краснухой (в том числе врожденной) направляется в территориальный центр Роспотребнадзора в виде экстренного извещения не позже чем через 12 ч после выявления больного. Лечебно-профилактическое учреждение, уточнившее, изменившее или отменившее диагноз, обязано в течение 24 ч отослать новое извещение.
Беременных женщин изолируют от больных на 10 дней от начала заболевания (временный переезд на другую квартиру, перевод на другую работу из детского учреждения и др.).
Экстренная профилактика: детям и беременным, общавшимся с больным, вводят нормальный иммуноглобулин человека.
Контрольные вопросы:
1. Каковы особенности краснушной инфекции?
2. Какие методы по профилактике краснухи Вы знаете?
Вирусные гепатиты – общее название острых инфекционных заболеваний человека, которые имеют клинически сходные проявления, полиэтиологичны, но различны по эпидемиологическим характеристикам.
В настоящее время описано, по меньшей мере, пять нозологических форм вирусных гепатитов: А, В, С, D, Е. Кроме того, существует группа недифференцированных вирусных гепатитов, обозначаемых прежде как - гепатит ни А ни В. Именно из этой группы были выделены гепатиты С и Е.
В последние годы идентифицированы вирусы G и TTV, изучается их роль в поражении печени. Известно, что после перенесения гепатитов возможно развитие неблагоприятных исходов. Часто формируется хронический гепатит (особенно при гепатите С), в дальнейшем у части этих больных возможно развитие цирроза печени. Доказана также этиологическая связь между первичной гепатоцеллюлярной карциномой и вирусами гепатитов В и С. Кроме того, несмотря на использование современных методов лечения, в большинстве случаев не удается предотвратить летальные исходы при фульминантном течении гепатита.
Вирусный гепатит А (ВГА)- антропонозная вирусная инфекционная болезнь с фекально-оральным механизмом передачи возбудителя. Характеризуется преимущественным поражением печени, циклическим доброкачественным течением, может сопровождаться желтухой.
Возбудитель - hepatitis A virus с однонитчатой РНК, без оболочки, из семейства Picornaviridae рода Hepatovirus. Относительно устойчив во внешней среде. Он обладает способностью к сохранению при комнатной температуре в течение нескольких недель, при +4°С – месяцами, при -20°С– остается жизнеспособным несколько лет. При температуре 100°С инактивируется в течение 5 мин, под воздействием хлора в дозе 0,5-1,0 мл/л, при рН 7,0 выживает в течение 30 мин и более, что определяет его способность сохраняться определенное время в водопроводной воде.
Резервуар и источники возбудителя: человек, больной вирусным гепатитом А. Вирус выделяют больные с различными формами заболевания, в том числе, наиболее частыми (особенно у детей) - безжелтушной и стертой, которые обычно не диагностируют, соответственно заболевших этими формами не госпитализируют, они ведут активный образ жизни и могут заражать окружающих.
Механизм передачи возбудителя фекалъно-оральный; пути передачи - водный (основной), пищевой, бытовой; факторы передачи - питьевая вода, продукты питания, грязные руки.
Период заразительности источника. В фекалиях и в крови вирус обнаруживается начиная со второй половины инкубационного периода с пиком в течение первой недели желтухи и спустя месяц от начала желтухи, хотя в отдельных случаях выделение вируса может длиться месяцами.
Естественная восприимчивость людей высокая. Относительно низкая заболеваемость детей младшего возраста, по-видимому, является следствием перенесенного ими заболевания в виде легкой или безжелтушной формы.
Основные эпидемиологические и клинические признаки.
Экстренная профилактика
В первые 3 дня от момента контакта с больным, необходимо введение вакцины не болевшим корью и не привитым детям старше 12 месяцев, подросткам и взрослым. При наличии противопоказаний к введению вакцины в качестве экстренной профилактики используют противокоревой иммуноглобулин или нормальный иммуноглобулин человека до 4-го дня от момента контакта.
Контрольные вопросы:
1. Каковы особенности коревой инфекции?
2. Какие методы профилактики кори Вы знаете?
5.9. Профилактика краснухи
Краснуха — антропонозная острая вирусная инфекционная болезнь с аспирационным механизмом передачи возбудителя. С клинической точки зрения характеризуется мелкой пятнисто-папулезной сыпью, генерализованной лимфаденопатией, умеренной интоксикацией и поражением плода у беременных.
Различают постнатальную (приобретенную) и антенатальную (врожденную) краснуху.
Постнатальная (приобретенная) краснуха — источником инфекции является больной с манифестной или бессимптомной формой течения инфекционного процесса. Заболевание обычно протекает гладко, но иногда может осложняться энцефалитом или менингоэнцефалитом и очень редко тромбоцитопенией.
Антенатальная (врожденная) краснуха проявляется пороками развития сердца (дефекты предсердной или желудочковой перегородки, стеноз легочной артерии, незаращение боталлова протока), глаз (катаракта, микрофтальмия, глаукома, хориоретинит), центральной нервной системы (менингоэнцефалит, микроцефалия, задержка умственного развития) и глухотой. Возможны также отставание в росте, гепатоспленомегалия, тромбоцитопения, желтуха, поражение трубчатых костей и др. Течение болезни длительное, с персистированием вируса от нескольких месяцев до 1,5 лет и больше. Врожденная краснуха у плода может развиться и после бессимптомной краснухи у беременной.
Возбудитель - РНК-содержащий вирус из семейства Togaviridae рода Rubivirus. Проявляет тератогенную активность. Малоустойчив к действию физических и химических факторов: при температуре 37°С 90% вирусов инактивируется за 4 мин, при 100°С - за 2 мин; вирус быстро разрушается под действием органических растворителей, хлорактивных соединений, формалина, УФ-лучей.
Резервуар и источники возбудителя: человек с клинически выраженной или бессимптомно протекающей инфекцией. Больной выделяет вирус во внешнюю среду за 1 нед до появления сыпи и в течение 5-7 дней после появления высыпаний. Большое эпидемиологическое значение имеют дети с врожденной краснухой, в организме которых вирус может сохраняться до 1,5 года и более, а также больные скрытой формой инфекции, которых среди взрослых в 6 раз больше, чем больных типичной манифестной формой.
Механизм передачи возбудителя аспирационный; путь передачи - воздушно-капельный. Вирус выделяется из организма больного с секретом слизистой оболочки верхних дыхательных путей (наиболее интенсивно за сутки до появления клинических симптомов заболевания). Для реализации механизма передачи необходимо более тесное общение с больным, чем при кори или ветряной оспе. Самостоятельное значение имеет вертикальный механизм передачи возбудителя плоду от матери, заболевшей в первые 4 мес беременности.
Естественная восприимчивость людей высокая.
Основные эпидемиологические и клинические признаки. ВОЗ относит краснуху к инфекциям, ликвидация которых возможна в ближайшем будущем. С учетом значения для здравоохранения синдрома врожденной краснухи, 48-я сессия Регионального комитета ВОЗ для Европы (1998) включила краснуху в число инфекций, борьба с которыми будет определять цели программы «Здоровье для всех в ХХI веке». К 2010 г частота синдрома врожденной краснухи должна быть снижена до уровня менее 0,01 на 1000 новорожденных.
В довакцинальный период краснуху с высокой заболеваемостью регистрировали повсеместно. По данным ВОЗ, из всех случаев краснухи, регистрируемых в Европе, 83% приходилось на страны СНГ, причем 57% из них на Российскую Федерацию. В большинстве стран мира к 6-10 годам жизни более половины детей имеют противокраснушные антитела в крови, а к 20 годам - 80-95%. В последние годы отмечается сдвиг заболеваемости на женщин детородного возраста. Характерны выраженные периодические подъемы заболеваемости с интервалом в 3 - 4 года, особенно выраженные через 7-10 лет, перемежающиеся периодами спорадической заболеваемости. Основная заболеваемость регистрируется среди детей 3-9 лет, главным образом посещающих дошкольные детские учреждения и начальные классы школ. Характерна выраженная зимне-весенняя сезонность с пиком в апреле - мае.
Краснуху принять считать легким заболеванием. В целом у детей краснуха протекает легко, осложнения наблюдаются редко. Наиболее грозным осложнением является краснушный энцефалит, его частота достаточно редка и составляет, по данным ряда авторов 1:5000-1:6000 случаев.
Краснуха во взрослом и подростковом возрасте протекает значительно тяжелее. Более выражена лихорадка, явления интоксикации (недомогание, разбитость), отмечаются поражения глаз (конъюнктивит). Характерным в клинике краснухи у взрослых (с большей частотой у женщин) является поражение мелких (фаланговые, пястно-фаланговые) и реже крупных (коленные, локтевые) суставов.
Большинство больных не нуждаются в специальном лечении. Проводят в основном симптоматическое лечение. После перенесенного заболевания развивается пожизненный противокраснушный иммунитет, однако его напряженность с возрастом и под воздействием различных факторов, может падать. Таким образом, перенесенное в детстве заболевание краснухой не может служить 100% гарантией от повторного заболевания.
Заболевание беременной женщины приводит к инфицированию плода. В зависимости от срока беременности, на котором происходит заражение, у плода c различной вероятностью (в первом триместре вероятность достигает 90%, во втором - до 75%, в третьем - 50%) формируются множественные пороки развития, входящие в понятие «Синдром врожденной краснухи (СВК)». К СВК также относят дефекты формирования костей черепа, головного мозга (малый размер мозга, умственная отсталость), внутренних органов (желтуха, увеличение печени, миокардит и др.) и костей (участки разрежения костной ткани длинных трубчатых костей). В 15% случаев краснуха у беременных приводит к выкидышу, мертворождению. При выявлении краснухи всегда осуществляется искусственное прерывание беременности. По оценкам ВОЗ всего на планете краснуха ежегодно калечит около 300 тыс. детей.
Профилактические мероприятия.
Существует три принципиальных подхода (стратегии) к профилактике и искоренению краснухи: вакцинация детей, вакцинация девушек-подростков и вакцинация женщин детородного возраста, планирующих иметь детей.
Первая стратегия эффективна против борьбы с самой краснухой, но полностью не решает проблемы СВК (для этого потребуется 20-30 лет), поскольку по имеющимся данным, вакцинация защищает на срок около 20 лет, а значит, теоретически она способна сдвинуть заболеваемость краснухой на детородный возраст.
Вторая стратегия, вакцинация девушек-подростков (в 11-14 лет) эффективна в плане искоренения СВК (однако, для достижения этой цели потребуется 10-20 лет), но не решает проблемы искоренения заболеваемости краснухой (в России пик приходится на возраст 7-14 лет).
Вакцинация женщин крайне эффективна в плане борьбы с СВК (хотя добиться 100% охвата взрослого населения прививками против краснухи практически не реально), но также не решает проблемы искоренения краснухи.
Ввиду вышеприведенных обстоятельств ВОЗ рекомендует сочетать по мере возможности все три стратегии. Примером такого сочетания является США, где помимо вакцинации детей, вакцинация проводится в колледжах и вооруженных силах. Интересный выход из проблемы вакцинации женщин детородного возраста нашли во Франции - отказ в регистрации брака при отсутствии отметки о прививке против краснухи, либо записи о перенесенной инфекции.
Вакцинация потив краснухи
В России прививка против краснухи в Национальный календарь профилактических прививок включена в 1997 г. Вакцинацию проводят детям в возрасте 12 мес однократно, ревакцинацию - в 6 лет. Для иммунизации возможно применение ассоциированных вакцин, содержащих краснушный, коревой и паротитный компоненты.
Для профилактики врожденной краснухи при заболевании женщин в первые 16 нед. беременности рекомендуют ее прерывание.
Информация о заболевшем краснухой (в том числе врожденной) направляется в территориальный центр Роспотребнадзора в виде экстренного извещения не позже чем через 12 ч после выявления больного. Лечебно-профилактическое учреждение, уточнившее, изменившее или отменившее диагноз, обязано в течение 24 ч отослать новое извещение.
Беременных женщин изолируют от больных на 10 дней от начала заболевания (временный переезд на другую квартиру, перевод на другую работу из детского учреждения и др.).
Экстренная профилактика: детям и беременным, общавшимся с больным, вводят нормальный иммуноглобулин человека.
Контрольные вопросы:
1. Каковы особенности краснушной инфекции?
2. Какие методы по профилактике краснухи Вы знаете?
5.10. Профилактика вирусных гепатитов
Вирусные гепатиты – общее название острых инфекционных заболеваний человека, которые имеют клинически сходные проявления, полиэтиологичны, но различны по эпидемиологическим характеристикам.
В настоящее время описано, по меньшей мере, пять нозологических форм вирусных гепатитов: А, В, С, D, Е. Кроме того, существует группа недифференцированных вирусных гепатитов, обозначаемых прежде как - гепатит ни А ни В. Именно из этой группы были выделены гепатиты С и Е.
В последние годы идентифицированы вирусы G и TTV, изучается их роль в поражении печени. Известно, что после перенесения гепатитов возможно развитие неблагоприятных исходов. Часто формируется хронический гепатит (особенно при гепатите С), в дальнейшем у части этих больных возможно развитие цирроза печени. Доказана также этиологическая связь между первичной гепатоцеллюлярной карциномой и вирусами гепатитов В и С. Кроме того, несмотря на использование современных методов лечения, в большинстве случаев не удается предотвратить летальные исходы при фульминантном течении гепатита.
Вирусный гепатит А (ВГА)- антропонозная вирусная инфекционная болезнь с фекально-оральным механизмом передачи возбудителя. Характеризуется преимущественным поражением печени, циклическим доброкачественным течением, может сопровождаться желтухой.
Возбудитель - hepatitis A virus с однонитчатой РНК, без оболочки, из семейства Picornaviridae рода Hepatovirus. Относительно устойчив во внешней среде. Он обладает способностью к сохранению при комнатной температуре в течение нескольких недель, при +4°С – месяцами, при -20°С– остается жизнеспособным несколько лет. При температуре 100°С инактивируется в течение 5 мин, под воздействием хлора в дозе 0,5-1,0 мл/л, при рН 7,0 выживает в течение 30 мин и более, что определяет его способность сохраняться определенное время в водопроводной воде.
Резервуар и источники возбудителя: человек, больной вирусным гепатитом А. Вирус выделяют больные с различными формами заболевания, в том числе, наиболее частыми (особенно у детей) - безжелтушной и стертой, которые обычно не диагностируют, соответственно заболевших этими формами не госпитализируют, они ведут активный образ жизни и могут заражать окружающих.
Механизм передачи возбудителя фекалъно-оральный; пути передачи - водный (основной), пищевой, бытовой; факторы передачи - питьевая вода, продукты питания, грязные руки.
Период заразительности источника. В фекалиях и в крови вирус обнаруживается начиная со второй половины инкубационного периода с пиком в течение первой недели желтухи и спустя месяц от начала желтухи, хотя в отдельных случаях выделение вируса может длиться месяцами.
Естественная восприимчивость людей высокая. Относительно низкая заболеваемость детей младшего возраста, по-видимому, является следствием перенесенного ими заболевания в виде легкой или безжелтушной формы.
Основные эпидемиологические и клинические признаки.
Гепатит А относится к числу наиболее распространенных в мире кишечных инфекций, однако заболеваемость преобладает в развивающихся странах, где уровень санитарно-коммунального благоустройства недостаточно высок.
Выражена летняя сезонность.
В мире ежегодно регистрируют около 1,4 млн случаев ВГА. В разных странах показатели заболеваемости имеют существенное отличие в зависимости, прежде всего, от санитарно-гигиенических условий жизни населения. В России имеются регионы с высокой заболеваемостью ВГА, что обусловлено, прежде всего, недостатками в обеспечении населения доброкачественной питьевой водой.
Начало болезни обычно острое с выраженной интоксикацией, тяжестью в эпигастральной области и правом подреберье, появлением желтухи. Возможны и безжелтушные варианты течения гепатита.
Профилактические мероприятия, как и при других кишечных инфекциях, направлены на нейтрализацию источника и факторов передачи возбудителя.
Выражена летняя сезонность.
В мире ежегодно регистрируют около 1,4 млн случаев ВГА. В разных странах показатели заболеваемости имеют существенное отличие в зависимости, прежде всего, от санитарно-гигиенических условий жизни населения. В России имеются регионы с высокой заболеваемостью ВГА, что обусловлено, прежде всего, недостатками в обеспечении населения доброкачественной питьевой водой.
Начало болезни обычно острое с выраженной интоксикацией, тяжестью в эпигастральной области и правом подреберье, появлением желтухи. Возможны и безжелтушные варианты течения гепатита.
Профилактические мероприятия, как и при других кишечных инфекциях, направлены на нейтрализацию источника и факторов передачи возбудителя.
| Комплекс профилактических мер включает: • приведение источников водоснабжения в соответствие санитарными нормами и правилами, поддержание водопроводных сооружений в надлежащем санитарно-техническом состоянии, проведение очистки и обеззараживания питьевой воды; • очистка и обеззараживание сточных вод перед их сбросом в водоемы, регулярная очистка и дезинфекция помойных ям, надворных уборных, ликвидация неорганизованных свалок; • соблюдение санитарных и противоэпидемических норм и правил при сборе, обработке, приготовлении, транспортировке, хранении и реализации продуктов питания; • создание условий для выполнения правил личной гигиены в местах общественного питания, сосредоточения людей (вокзалы, аэропорты, школы), массового отдыха населения (культурно-зрелищные учреждения); • санитарное просвещение населения, овладение работниками общественного питания и торговли пищевыми продуктами санитарным минимумом. |
Неспецифическая профилактика ВГА, как и других кишечных инфекций, включает санитарно-гигиенические мероприятия, обеспечение населения доброкачественной питьевой водой и продуктами питания. Ранняя диагностика ВГА и изоляция заболевших ещё до появления у них желтухи может предотвратить заражение окружающих. В отделениях для больных вирусными гепатитами необходима раздельная госпитализация больных ВГА и другими гепатитами во избежание внутрибольничного заражения.
Лица, контактировавшие с больными ВГА, должны находиться под наблюдением в течение 35 дней с момента последнего контакта (термометрия, опрос, определение размеров печени и селезёнки, осмотр кожи и слизистых оболочек и т.д.). При наличии у контактных лиц лихорадки, диспепсических явлений, потемнения мочи и т.д. проводят лабораторные исследования. По решению врача эпидемиолога в зависимости от конкретной ситуации в очаге ВГА может быть назначено также обследование контактных, не имеющих каких-либо явных признаков заболевания, с целью выявления безжелтушного, стертого и инаппарантного вариантов ВГА.
Вирусный гепатит Е(ВГЕ) - антропонозная вирусная инфекционная болезнь с фекально-оральным механизмом передачи возбудителя, для которого характерны циклическое течение с преимущественным поражением печени; проявляется интоксикацией и желтухой с частым развитием острой печеночной энцефалопатии у беременных. По клиническому течению сходен с вирусным гепатитом А.
Возбудитель по своим морфологическим свойствам близок к калицивирусам (семейство Caliciviridae). Геном вируса представлен однонитчатой РНК. Вирус быстро разрушается под действием хлорсодержащих дезинфицирующих средств. Он менее устойчив в окружающей среде, чем вирус гепатита А.
Резервуар и источники возбудителя: больной с острой формой ВГЕ.
Механизм передачи возбудителя фекально-оральный; путь передачи - преимущественно водный. Вирус гепатита Е может передаваться плоду от матери в III триместре беременности.
Естественная восприимчивость людей высокая.
Основные эпидемиологические и клинические признаки те же, что при вирусном гепатите А. Особенностью является преимущественное поражение взрослых. В отличие от других гепатитов наблюдаются гемолиз эритроцитов и гемоглобинурия, острая печеночная недостаточность и геморрагический синдром.
Профилактические мероприятия такие же, как при вирусном гепатите А.
Вирусный гепатит В (ВГВ) - антропонозная вирусная инфекционная болезнь с контактным и вертикальным механизмами передачи возбудителя. Характеризуется циклически протекающим паренхиматозным гепатитов с наличие в части случаев желтухи и возможной хронизацией.
Возбудитель - сложноорганизованный ДНК-содержащий вирус (HBV), относящийся к семейству гепаднавирусов (Hepadnavirus); имеет три специфических антигена: HBsAg («австралийский»), HBcAg и HBeAg.
Вирус устойчив во внешней среде. Сохраняет жизнеспособность в сыворотке крови при комнатной температуре в течение трех месяцев, при -20°С – 15 лет, в высушенной плазме – до 25 лет. Не погибает при действии многих дезинфицирующих средств и консервантов крови. Вирус теряет способность вызывать заражение при автоклавировании (при температуре 120°С через 45 мин), стерилизации сухим паром (при температуре 180°С в течение 60 мин), кипячении (в течение 30 мин), а также при прогревании при температуре 60°С в течение 10 ч. Вирус не чувствителен к кислым значениям рН, но разрушается в щелочной среде. Губительно действуют на вирус перекись водорода, УФ-облучение.
Резервуар и источники возбудителя: больной острым или хроническим гепатитом человек или вирусоноситель.
Механизм передачи возбудителя – естественные (контактный, вертикальный) и искусственный (артефициальный). Пути реализации механизмов передачи возбудителя разнообразны: половой, трансплацентарный, парентеральный (инъекционный, трансфузионный, трансплантационный). Из естественных механизмов передачи реализуется контактный (половой путь), а также посредством контаминированных вирусом различных предметов обихода (бритвы, зубные щетки, полотенца), когда он проникает в организм через микротравмы на коже и наружных слизистых оболочках. Возможен также вертикальный (перинатальный) механизм передачи возбудителя.
Естественная восприимчивость людей высокая. Известно, что переливание инфицированной вирусом гепатита В крови приводит к развитию заболевания у 50-90 % реципиентов.
Основные эпидемиологические и клинические признаки. Гепатит В распространен повсеместно. По оценкам экспертов ВОЗ, в мире регистрируют ежегодно 50 млн заболевших и насчитывают 300-350 млн вирусоносителей, являющихся источниками инфекции. Ежегодно от гепатита В погибают около 7 млн человек.
К эпидемиологическим особенностям гепатита В относят наличие разнообразных источников инфекции и множество путей и факторов передачи возбудителя, что определяет широчайшую территориальную распространенность этого гепатита.
На территориях с высоким уровнем заболеваемости среди заболевших преобладают дети раннего возраста, с умеренным и низким - взрослые. В эпидемический процесс в первую очередь вовлекаются лица, подвергаемые гемотрансфузии и другим медицинским парентеральным манипуляциям, медицинские работники, в процессе своей профессиональной деятельности, соприкасающиеся с кровью и ее препаратами (хирурги, стоматологи, акушеры-гинекологи и др.), а также наркоманы (при пользовании общим шприцем), гомосексуалисты (половой путь передачи) и т.п.
Отмечаются весенний и осенний подъемы заболеваемости. Характерны семейные очаги болезни. В целом особенности эпидемического процесса определяются феноменом широко распространенного бессимптомного носительства вируса.
Профилактика.
С целью профилактики ВГВ проводят тщательный отбор доноров. В последние годы максимально ограничено число показаний к переливанию крови, так как вероятность заражения вирусным гепатитом сохраняется даже при тщательном скрининге донорской крови. В целях профилактики ВГВ необходимо соблюдение правил обработки медицинских инструментов, соблюдение правил работы медицинскими сотрудниками (использование перчаток, масок, защитных очков), санитарно-просветительная работа среди населения (информация о риске полового заражения, риске заражения при внутривенном употреблении наркотиков), обследование беременных на наличие HBsAg.
| Для профилактики ВГВ помимо общих для всех гемоконтактных инфекций, используют мероприятия, подробно рассмотренные в разделе 5.6: • использование презервативов при половых контактах со случайными партнерами; • избегание пирсинга, татуировок; • неиспользование внутривенных наркотиков; • карантинизация донорской крови; • контроль за медицинским инструментарием |
Специфическую профилактику осуществляют с помощью генноинженерных вакцин против ВГВ, содержащих в качестве иммуногена рекомбинантный HBsAg. Вакцины против ВГВ могут применяться в целях экстренной профилактики инфекции среди медицинских работников при случайной травме предметами, загрязнёнными кровью больных или носителей HBsAg. Медицинским работникам после контакта с кровью больного или носителя первую дозу вакцины вводят в первые сутки и не позднее 72 ч после контакта. В целях экстренной профилактики в ряде случаев сочетают с пассивной иммунизацией специфическим иммуноглобулином — иммуноглобулином человека против ВГВ. Протективный эффект иммуноглобулина сохраняется 1-6 нед.
Вирусный гепатит D (гепатит дельта, гепатит В с дельта агентом) – вирусный гепатит с контактным механизмом передачи возбудителя, вызываемый дефектным вирусом, репликация которого возможна только при наличии в организме HBsAg. Заболевание характеризуется тяжелым течением и неблагоприятным прогнозом.
Возбудитель – дельта агент с однонитчатой молекулой РНК, внешняя оболочка которого сформирована поверхностным антигеном вируса гепатита В (HBsAg).
Резервуар и источник возбудителя – при отсутствии в организме человека вируса гепатита В, заражением вирусом гепатита D не происходит, источники гепатитов D и B общие. Основное эпидемиологическое значение имеют носители HBsAg и больные хроническими формами гепатита В, инфицированные вирусом гепатита D.
Механизм передачи возбудителя – аналогичен таковому при гепатите В.
Естественная восприимчивость людей к вирусу гепатита D, определяется наличием больных гепатитом В и/или носителей возбудителей этой инфекции.
Основные эпидемиологические и клинические признаки.
Эпидемиологические проявления гепатита D такие же, как при гепатите В. Однако имеются и определенные различия, в частности, это касается территориальной распространенности. Зоны гиперэндемичности гепатитов D и B в основном совпадают. В Российской Федерации максимум регистрации гепатита D приходится на Туву, Якутию.
Профилактика такая же, что и при ВГВ-инфекции. Вакцинация здоровых людей против ВГВ обеспечивает защиту и от дельта-вирусной инфекции.
Особенно тщательно от возможного присоединения дельта-вирусной инфекции следует оберегать носителей НВs-антигена и больных хроническим вирусным гепатитом В. Проводят разъяснительную работу, родственники больного и сам больной ВГВ должны знать о путях зараже-ния дельта-инфекцией и необходимости соблюдения мер безопасности.
Вирусный гепатит С (ВГС) - антропонозная вирусная инфекционная болезнь с контактным механизмом передачи возбудителя, характеризуемая легким или субклиническим течением острого периода болезни, частым формированием хронического гепатита С, возможным развитием цирроза печени и гепатоцеллюлярной карциномы.
Возбудитель - РНК-содержащий вирус, относящийся к семейству Flaviviridae. Отличительной особенностью является способность к длительной персистенции в организме, что обуславливает высокий уровень хронизации.
Резервуар и источники возбудителя: человек с желтушной, безжелтушной или субклинической формой заболевания.
Механизм передачи возбудителя такие же, как и при гепатите В, однако структура путей, реализующих механизм передачи имеет свои особенности, что связывают с относительно невысокой устойчивостью возбудителя в о внешней среде и большой инфицирующей дозой при заражении. Главный путь распространения возбудителя – парентеральный, реализуемый при внутривенном введении психоактивных веществ. Половой и бытовой пути передачи имеют меньшее значение вследствие низкого уровня виремии.
Естественная восприимчивость людей к гепатиту С неодинаковая и в большей степени определяется инфицирующей дозой.
Основные эпидемиологические и клинические признаки те же, что и вирусного гепатита В.
Профилактические мероприятия такие же, как в отношении вирусного гепатита В.
Специфическая профилактика отсутствует, поскольку выраженная изменчивость генома вируса гепатита С создаёт серьёзные трудности для создания вакцины.
Неспецифическая профилактика ВГС, как и других парентеральных гепатитов, включает совершенствование комплекса мероприятий, направленных на предупреждение парентерального заражения в медицинских учреждениях и учреждениях немедицинского профиля, усиление борьбы с наркоманией, улучшение информированности населения о путях передачи возбудителя ВГС и мерах профилактики заражения этим вирусом.
| Памятка для пациентов Вы перенесли острый вирусный гепатит, и Вам необходимо знать, что исчезновение желтухи, удовлетворительные лабораторные показатели и хорошее самочувствие не служат показателями полного выздоровления, так как полное восстановление здоровья печени наступает в течение 6 мес. С целью предупреждения обострения заболевания и перехода в хроническую форму важно строго соблюдать врачебные рекомендации, относящиеся к последующему наблюдению и обследованию в условиях поликлиники, режиму дня, диете, а также к условиям труда. Режим Возвращение к трудовой деятельности, связанной с большим физическим напряжением или профессиональными вредностями, допустимо не ранее чем через 3-6 мес после выписки. До этого возможно продолжение трудовой деятельности в облегчённых условиях.
После выписки из стационара следует остерегаться переохлаждения и избегать перегревания на солнце, не рекомендуют поездки на южные курорты на протяжении первых 3 мес. Также следует остерегаться приёма медикаментов, оказывающих побочное (токсическое) влияние на печень. После нормализации биохимических показателей крови на протяжении 6 мес запрещается участие в спортивных соревнованиях. Переболевшие ОГВ освобождаются от профилактических прививок на 6 мес. Занятия спортом ограничиваются лишь комплексом лечебной гимнастики. Диета На протяжении 6 мес после выписки необходимо обращать особое внимание на питание, которое должно быть достаточно полноценным, при полном исключении вредных для печени веществ. Алкогольные напитки (в том числе пиво) категорически запрещаются. Питаться в течение дня необходимо регулярно через каждые 3-4 ч, избегая переедания. Разрешено • Молоко и молочные продукты во всех видах. • Отварное и тушёное мясо — говядина, телятина, куры, индейка, кролик. • Отварная свежая рыба — щука, карп, судак и морская рыба: треска, окунь, ледяная. • Овощи, овощные блюда, фрукты, квашеная капуста. • Крупяные и мучные изделия. • Супы овощные, крупяные, молочные. Ограничено • Мясные бульоны и супы — нежирные, не чаще 1-2 раз в неделю. • Сливочное масло (не более 50-70 г/сут, для детей — 30-40 г), сливки, сметана. • Яйца — не более 2-3 раз в неделю, белковые омлеты. • Сыр в небольшом количестве, только не острый. • Сосиски говяжьи, колбаса докторская, диетическая, столовая. • Икра лососёвых и осетровых, сельдь. • Помидоры. Запрещено • Алкогольные напитки. • Все виды жареных, копчёных и маринованных продуктов. • Свинина, баранина, гуси, утки. • Острые приправы — хрен, перец, горчица, уксус. • Кондитерские изделия — торты, пирожные. • Шоколад, шоколадные конфеты, какао, кофе. • Томатный сок. Цит. по Инфекционные болезни: национальное руководство.-М.:ГЭОТАР-Медиа, 2009. |
Контрольные вопросы:
1. Какие основные виды вирусных гепатитов Вы знаете?
2. Каковы меры по профилактике вирусных гепатитов?
3. Для каких вирусных гепатитов эффективна профилактика?
5.11. Профилактика кишечных гельминтозов
Гельминты (глисты) представляют собой большую опасность для организма человека, так как продукты их жизнедеятельности поражают центральную нервную систему, угнетают пищеварительную функцию, препятствуют всасыванию ряда витаминов и минеральных веществ, вызывают развитие аллергических реакций, повышение температуры тела, кожный зуд и т.д. Подобные симптомы часто воспринимаются как признаки других болезней, что приводит к поздней диагностике и несвоевременному началу лечения гельминтозов.
Проблема глистных инвазий всегда была, есть и будет сопутствовать человечеству. Это связано с тем, что гельминты имеют повсеместное распространение. Они попадают в организм с немытыми овощами, фруктами, недостаточно термически обработанными мясом, рыбой, а также через грязные руки. В ряде случаев возможен перенос гельминтов через укусы насекомых.
При гельминтозах снижается общая сопротивляемость организма, более тяжело протекают другие заболевания, создаются благоприятные условия для развития инфекционных процессов в различных органах и тканях.
Распространению гельминтозов способствует несоблюдение элементарных правил личной гигиены. Особенно распространены гельминты в детской среде. Многие дети «без разбору всё тащат в рот», что также способствует заражению гельминтозами.
Существует более 60 видов гельминтозов, поражающих человека. Наиболее часто встречающиеся приведены ниже.
Энтеробиоз — антропонозный контагиозный гельминтоз человека, характеризующийся перианальным зудом и кишечными расстройствами.
Возбудитель — острица (Enterobius Vermicularis), относящаяся к типу Nemathelminthes, классу Nematoda, отряду Rhabditida, семейству Oxyuridae.
Источником заражения служит только инвазированный человек. Механизм заражения фекально-оральный. Основной фактор передачи – загрязненными яйцами остриц руки, а также предметы домашнего обихода, игрушки, также переносчиками яиц остриц могут являться мухи.
Болеют люди всех возрастов, но чаще дошкольники. В толстой кишке больного одновременно могут обитать сотни остриц. Самки откладывают яйца вокруг анального отверстия, вызывая сильный зуд. Яйца остриц в течение нескольких часов дозревают на теле и на белье. Наблюдается повторный занос яиц через рот немытыми руками. У девочек при неправильном подмывании (по направлению от анального отверстия к половому) эти яйца могут быть занесены в мочеполовые пути, вызывая развитие вульвита и вульвовагинита.
Главный симптом энтеробиоза — зуд в анальной области. Зуд чаще появляется в вечерние и ночные часы. Дети становятся капризными, теряют в весе, жалуются на головные боли, у них нарушается сон. В ряде случаев на первый план выходят кишечные симптомы: учащенный стул, урчание в животе, запор.
Профилактика. В профилактике энтеробиоза значение придают выявлению источника инвазии и устранению путей передачи возбудителя. С этой целью один раз в год (после летнего периода при формировании детского коллектива или по эпидемическим показаниям) проводят плановые профилактические обследования детей и обслуживающего персонала. Детей, больных энтеробиозом, в период лечения и проведения контрольного обследования отстраняют от посещения дошкольных и образовательных учреждений. Если выявлены 20% и более зараженных энтеробиозом при проведении плановых профилактических обследований в организованных коллективах, в соответствии с нормативными документами одновременно всем детям и персоналу проводят противогельминтное лечение (двукратно с интервалом в 2 недели). В очаге энтеробиоза необходимо строго соблюдать чистоту жилища, служебных, школьных помещений. Лица, соприкасающиеся с больными должны соблюдать чистоту тела, одежды, мыть руки перед едой и после посещения туалета.
Аскаридоз – гельминтоз из группы кишечных нематодозов, вызываемых аскаридами, характеризующийся в ранней стадии явлениями аллергии, а в поздней – диспептическими явлениями и осложнениями при проникновении гельминтов в другие органы и также в результате закупорки или спазма кишечника. Аскариды паразитирует в тонкой кишке, питаясь ее содержимым. Источник заражения окружающей среды – только больной аскаридозом человек. Аскаридоз относится к геогельминтозам. Больной человек выделяет яйца аскарид, которые попадают во внешнюю среду. В дальнейшем яйца аскарид поступают в организм человека с немытыми овощами и фруктами, некипяченой водой, через грязные руки. Аскаридоз переносится мухами и передается через предметы личного обихода. Чаще заражение происходит в летний период, когда создаются благоприятные условия для развития яиц аскарид в почве.
Больные аскаридозом дети - бледные, плохо едят, жалуются на тошноту, рвоту, понос или запор, боль в животе. Ребенок становится рассеянным, раздражительным, плохо спит.
Профилактика. В профилактике аскаридоза основное значение имеют санитарное благоустройство населенных мест и охрана почвы от фекального загрязнения. В индивидуальной профилактике важно строго соблюдать правила личной гигиены, тщательно промывать употребляемые в пищу сырые овощи, ягоды и фрукты.
Описторхоз — природно-очаговый биогельминтоз с фекально-оральным механизмом передачи возбудителя, характеризующийся длительным течением, и преимущественным поражением гепато-билиарной системы и поджелудочной железы. Возбудитель – Opisthorchus felineus (кошачая двуустка), принадлежит к типу плоских червей (трематоды), классу сосальщиков.
Основной источник описторхоза в населенных пунктах человека, домашние животные (кошки, свиньи) или синантропные грызуны. Механизм передачи фекально-оральный, путь передачи пищевой. Источник заражения для человека – рыбы семейства карповых, инвазированные метацеркариями кошачьего сосальщика и употребляемые в сыром или полусыром виде. Более других заражены язь, елец, плотва. Заболевание передается при употреблении в пищу недостаточно термически обработанной рыбы.
Описторхоз широко распространен на Евроазиатском континенте. Его регистрируют в ряде стран восточной и центральной Европы. В России и странах СНГ наиболее обширные очаги инфекции обнаружены на территории Западной Сибири, Северного Казахстана (бассейн рек Оби и Иртыша), Пермской и Кировской областей и бассейнов рек Камы, Вятки, Днепра, Десны, Сейма, Северного Донца, Южного Буга. Самую напряженную ситуацию отмечают в Западной Сибири, где расположен крупнейший Обь-Иртышский очаг инвазии.
Профилактика. Комплекс мер по борьбе с описторхозом включает следующие направления:
• обнаружение очагов и лечение больных описторхозом;
• проведение широкой санитарно-просветительной работы среди населения в очагах;
• дегельминтизация домашних плотоядных животных;
• охрана окружающей среды от фекального загрязнения;
• качественная термическая обработка рыбы карповых пород перед употреблением ее в пищу;
• борьба с промежуточными хозяевами описторхов и свободно плавающими стадиями паразита.
| В домашних условиях обеззараживать рыбу рекомендуют следующими способами: • прожаривать небольшие куски не менее 20 минут; • варить 20 минут с момента закипания; • выпекать рыбные пироги 40-60 минут; • применять крепкий посол (20% соли к массе рыбы) с 10 дневной выдержкой; • вялить мелкие карповые породы (плотва, елец) в течение трех недель с 2-3-дневным предварительным посолом; • холодное копчение рыбы проводить после крепкого посола или промораживания в течение 3-4 недель. |
Заражение человека происходит пищевым путем при употреблении недостаточно термически обработанного мяса крупного рогатого скота или свиней. Кроме этого, например, при эхинококкозе инфицирование человека может произойти при сборе ягод и трав, употреблении воды из источников, загрязненных яйцами гельминта, а также онкосферами эхинококка, которые в обилии могут находиться на шерсти инвазированных собак.
Профилактика состоит в соблюдении личной гигиены. Основные меры профилактики – выявление и лечение больных, санитарное просвещение населения, благоустройство населенных мест, санитарный надзор за содержанием и убоем свиней, ветеринарный контроль мяса (приложение 21). Для профилактики кишечных цестодозов необходимо соблюдать правила кулинарной обработки пищи. Особая настороженность необходима при содержании собак в доме и уходе за животными. Проводят плановую дегельминтизацию собак.
Несмотря на проводимые профилактические программы, заболеваемость основными гельминтозами на территории РФ остается достаточно высокой. При этом на долю детей до 14 лет приходится порядка 80% общего числа ежегодно регистрируемых случаев гельминтозов.
Контрольные вопросы:
1. Какие основные виды гельминтозов Вы знаете?
2. Как осуществляется профилактика гельминтозов?
Здоровый образ жизни и профилактика заболеваний
Под редакцией Ющука Н.Д., Маева И.В., Гуревича К.Г.
Москва,2012
(голосов:0) Просмотров: 11753
|
Похожие новости
Профилактика ОРВИ - лучше лечения!Эффективная профилактика ОРВИ и гриппа поможет сохранить здоровье даже с сезон простуд, она заключается не только в здоровом образе жизни, но и в применении современных средств на основе интерферона. Такая профилактика является не чуждой организму, а значит безопасной.ВПЧ - инфекция «берёт за горло»Ситуация с распространением папилломавирусной инфекции во всём мире с каждым годом накаляется. Одной из самых распространённых форм локализации ВПЧ (после аногенитальной) является папилломатоз гортани и голосовых связок. Насколько опасны и агрессивны данные типы ВПЧ? Реальные факты перемешиваются со слухами и домыслами. Некоторые светила от медицины считают, что ВПЧ (ВПЧ - инфекция: так ли уж всё серьёзно?Что мы знаем о ВПЧ – инфекции? Длительное время вирус папилломы человека (ВПЧ) не вызывал особо пристального внимания медицины. С вирусом напрямую связывали появление крайне неприятного заболевания — аногенитальных кондилом (бородавок), приносящих немалый физический и эстетический дискомфорт. Соответственно, лечение было направлено на устранение&nbsРотавирусные вакциныВо всем мире ротавирусы являются наиболее распространенной причиной тяжелых диарей у младенцев в возрасте до 1 года и детей младшего возраста. По расчетным данным в 2004 г. приблизительно 527 000 (475 000 – 580 000) случаев смерти, преимущественно в развивающихся странах, были связаны с ротавирусными инфекциями.Профилактика ротавирусной инфекции"МУ 3.1.1.2957-11. 3.1.1. Профилактика инфекционных болезней. Кишечные инфекции. Эпидемиологический надзор, лабораторная диагностика и профилактика ротавирусной инфекции. Методические указания" (утв. Главным государственным санитарным врачом РФ 29.07.2011) |
Комментарии
Информация
Посетители, находящиеся в группе Гости, не могут оставлять комментарии к данной публикации.